-
已知反应:①Cl2+2KBr=2KCl+Br2,②KClO3+6HCl=3Cl2+KCl +3H2O,③2KBrO3+Cl2=Br2+ 2KClO3,下列说法正确的是
A. 上述三个反应都有单质生成,所以都是置换反应
B. 氧化性由强到弱顺序为 KBrO3>KClO3>Cl2>Br2
C. 反应②中还原剂与氧化剂的物质的量之比为6:1
D. ③中lmol还原剂反应则氧化剂得到电子的物质的量为2mol
难度: 中等查看答案及解析
-
下列叙述正确的是( )
A. 1 mol H2O的质量为18g/mol
B. CH4的摩尔质量为16g
C. 3.01×1023个SO2分子的质量为32g
D. 标准状况下,1 mol任何物质体积均为22.4L
难度: 中等查看答案及解析
-
下列物质分类的正确组合是( )
碱
酸
盐
酸性氧化物
A
纯碱
盐酸
烧碱
二氧化硫
B
烧碱
硫酸
食盐
一氧化碳
C
苛性钠
醋酸
石灰石
水
D
苛性钾
碳酸
苏打
三氧化硫
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
在KCl、MgCl2、Mg(NO3)2形成的混合溶液中,c(K+)=0.1mol/L,c(Mg2+)=0.25mol/L,c(Cl-)=0.2mol/L,则c(NO3-)为 :
A. 0.15 mol/L
B. 0.20 mol/L
C. 0.25 mol/L
D. 0.40 mol/L
难度: 中等查看答案及解析
-
同温同压下,等质量的下列气体所占有的体积最大的是
A. SO2 B. CH4 C. CO2 D. O2
难度: 中等查看答案及解析
-
配制一定物质的量浓度的KOH溶液时,下列操作对实验结果没有影响的是( )
A. 容量瓶中原有少量蒸馏水 B. 洗涤烧杯和玻棒的溶液未转入容量瓶中
C. 定容时观察液面俯视 D. 定容时观察液面仰视
难度: 简单查看答案及解析
-
工业制取ClO2的化学反应:2NaClO3+ SO2+ H2SO4= 2ClO2+ 2NaHSO4 ,下列说法正确的
A. SO2在反应中被还原 B. NaClO3在反应中失去电子
C. H2SO4在反应中做氧化剂 D. 1 mol 氧化剂在反应中得到1 mol电子
难度: 中等查看答案及解析
-
氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于阴影部分的是
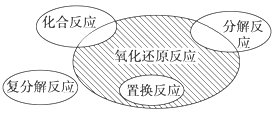
A. Cl2+2KBr===Br2+2KCl
B. 2NaHCO3Na2CO3+H2O+CO2↑
C. 4Fe(OH)2+O2+2H2O===4Fe(OH)3
D. 2Na2O2+2CO2===2Na2CO3+O2
难度: 简单查看答案及解析
-
下列玻璃仪器能直接加热的是
A. 烧杯 B. 试管 C. 容量瓶 D. 圆底烧瓶
难度: 简单查看答案及解析
-
胶体与溶液的本质区别是( )
A. 是否有丁达尔现象 B. 分散质粒子的大小
C. 分散质粒子能否通过滤纸 D. 是否无色透明
难度: 简单查看答案及解析
-
下列反应中,水作还原剂的是
A.CO2+H2O=H2CO3 B.Na2O+H2O=2NaOH
C.2Na+2H2O=2NaOH+H2↑ D.2F2+2H2O=4HF+O2
难度: 中等查看答案及解析
-
下列实验操作中错误的是
A. 过滤操作时,玻璃棒应靠在三层滤纸的一侧
B. 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C. 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D. 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
难度: 中等查看答案及解析
-
下列离子方程式中,正确的是
A. 氨气通入醋酸溶液中:CH3COOH+NH3 =CH3COONH4
B. 氢氧化钡溶液跟盐酸反应:H++OH-=H2O
C. 稀硫酸与氢氧化钡溶液反应:Ba2++SO42― =BaSO4↓
D. 石灰石溶解在稀HCl中:CO32-+2H+=CO2↑+H2O
难度: 中等查看答案及解析
-
下列溶液中,跟100mL 0.5mol/L CaCl2溶液所含的Cl-物质的量浓度相同的是
A. 100mL 1mol/L MgCl2溶液
B. 200mL 0.25mol/L AlCl3溶液
C. 200ml 1mol/L NaCl溶液
D. 200ml 0.5mol/L HCl溶液
难度: 中等查看答案及解析
-
224mL某气体在标准状况下的质量为0.32g,该气体的摩尔质量约为
A. 32g·mol-1
B. 32
C. 64g·mol-1
D. 64
难度: 中等查看答案及解析
-
实现下列变化,一定要加入氧化剂的是
A. CaCO3 → CO2
B. NaCl → NaNO3
C. Zn → ZnCl2
D. Cl2→HCl
难度: 困难查看答案及解析
-
下列说法正确的是(NA表示阿伏加德罗常数的值)
A. 28g氮气所含有的原子数目为NA
B. 在常温常压下,32克氧气含有的分子数为NA
C. 标准状况下,22.4L水中含有NA个水分子
D. 标准状况下,22.4L氧气和氢气混合物所含的分子数为2NA
难度: 中等查看答案及解析
-
下图所示是分离混合物时常用的主要仪器,从左至右,可以进行的混合物分离操作分

A. 蒸馏、蒸发、萃取、过滤 B. 蒸馏、过滤、萃取、蒸发
C. 萃取、过滤、蒸馏、蒸发 D. 过滤、蒸发、萃取、蒸馏
难度: 简单查看答案及解析
-
在某无色酸性溶液中能大量共存的一组离子是
A. Na+、K+、HCO3-、NO3- B. Mg2+、SO42-、Al3+、NO3-
C. Na+、Ca2+、 NO3-、CO32- D. K+、MnO4-、CH3COO-、NO3-
难度: 困难查看答案及解析
-
为了除去某粗盐样品中的Ca2+,Mg2+及SO42-,得到纯净的NaCl,可将粗盐溶于水,然后在下列操作中选取必要的步骤和正确的操作顺序:①过滤②加过量NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液,正确的是
A. ④②⑤①③
B. ⑤④②③①
C. ②④⑤①③
D. ⑤②④①③
难度: 困难查看答案及解析