-
饱和氯水长期放置后,下列微粒在溶液中不减少的是
A. HClO B. ClO- C. Cl2 D. Cl-
难度: 简单查看答案及解析
-
下列氯化物中,既能由金属和氯气直接化合制得,又能由金属和盐酸反应制得的是
A. CuCl2 B. MgCl2 C. FeCl3 D. FeCl2
难度: 简单查看答案及解析
-
在空气中长时间放置少量金属钠,最终的产物是
A. Na2O B. NaOH C. Na2CO3 D. Na2O2
难度: 中等查看答案及解析
-
下列化学方程式中,不能用离子方程式Ba2+ + SO42- = BaSO4↓表示的是
A. Ba(NO3)2 +H2SO4= BaSO4↓+2HNO3 B. BaCl2+ Na2SO4= BaSO4↓+2 NaCl
C. BaCO3 + H2SO4= BaSO4↓+ H2O+CO2↑ D. BaCl2+ H2SO4= BaSO4↓+2HCl
难度: 中等查看答案及解析
-
24 mL浓度为0.05 mol·L-1的Na2SO3溶液恰好与20 mL浓度为0.02 mol·L-1的K2Cr2O7溶液完全反应。已知Na2SO3被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中的化合价为
A. +2 B. +3 C. +4 D. +5
难度: 简单查看答案及解析
-
下列说法中正确的是( )
A. 摩尔既是物质的数量单位又是物质的质量单位
B. 常温常压下,48 g O2所占的体积是33.6 L
C. 阿伏加德罗常数的数值就是0.012 kg 12C中含有的碳原子数目
D. 氧气的摩尔质量是16 g/mol
难度: 中等查看答案及解析
-
在KCl、FeCl3、Fe2(SO4)3三种盐配成的混合溶液中,若K+为0.15 mol,Fe3+为0.25 mol,Cl-为0.2 mol,则SO42-为
A. 0.1 mol B. 0.15 mol C. 0.25 mol D. 0.35 mol
难度: 中等查看答案及解析
-
一些装有化学物质的容器上贴有危险化学品的标志,装有氢氧化钠的容器上应贴的标志是
A.
 B.
B. 
C.
 D.
D. 
难度: 简单查看答案及解析
-
若612C原子的质量为a g,A原子的质量为b g,NA为阿伏加德罗常数,则A元素的相对原子质量为
A. 12 a/b B. 12 b/a C. aNA D. 不能确定
难度: 简单查看答案及解析
-
下列各组物质,按化合物、单质、混合物顺序排列的是
A. 干冰、氢气、冰水共存物 B. 洁净的空气、液态氧、天然气
C. 纯碱、氦气、漂白粉 D. 酒精、氯水、氢氧化铁胶体
难度: 中等查看答案及解析
-
《本草纲目》记载了烧酒的制造工艺:“凡酸坏之酒,皆可蒸烧”以烧酒复烧二次..... 价值数倍也。”这里用到的实验方法可用于分离
A. 酒精和水 B. 苯和水 C. 食盐水和泥沙 D. 硝酸钾和氯化钠
难度: 简单查看答案及解析
-
下列化学反应中,属于氧化还原反应的是
A. CaCO3 + 2HCl = CaCl2 + H2O + CO2↑ B. KCl+AgNO3=AgCl↓+KNO3
C. 4NH3+5O2
4NO+6H2O D. CaCO3
CaO+CO2↑
难度: 简单查看答案及解析
-
实验室中,通常将金属钠保存在
A. 煤油中 B. 四氯化碳中 C. 水中 D. 汽油中
难度: 简单查看答案及解析
-
下列关于铁与水反应的描述不正确的是( )
A. 铁与水蒸气反应的产物是黑色的Fe2O3
B. 红热的铁能与水蒸气反应,放出的气体点燃时能发出爆鸣声
C. 铁与水蒸气的反应是氧化还原反应
D. 常温下,Fe与H2O不反应,但在空气中O2、CO2、H2O的共同作用下能发生反应
难度: 中等查看答案及解析
-
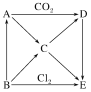
有A、B、C、D四种物质,已知它们能发生下列变化:
①2A2++B2=2B2++A2 ②2A2++C2=2C2++A2
③2B2++C2=2C2++B2 ④2C2++D2=2D2++C2
由此可推知,各物质的氧化性、还原性强弱顺序正确的是
①氧化性:A2+>B2+>C2+>D2+ ②氧化性:D2+>C2+>B2+>A2+
③还原性:A2>B2>C2>D2 ④还原性:D2>C2>B2>A2
A. ①③ B. ①④ C. ②③ D. ②④
难度: 简单查看答案及解析
-
下列有关化学实验操作正确的是
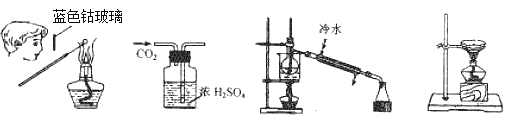
A. 检验K+的存在 B. 干燥CO2 C. 分离溴与CCl4 D. 蒸发食盐水
难度: 简单查看答案及解析
-
氯气是一种重要的工业原料,工业上利用反应3Cl2+2NH3=N2+6HCl检查氯气管道是否漏气。下列说法错误的是
A. 若管道漏气遇氨就会产生白烟
B. 该反应利用了氯气的强氧化性
C. 该反应属于复分解反应
D. 该反应生成1mol氮气时有6mol电子发生转移
难度: 简单查看答案及解析
-
在碱性溶液中能大量共存且溶液为无色透明的离子组是
A. K+、MnO4-、Na+、Cl- B. Na+、H+、NO3-、SO42-
C. K+、Na+、NO3-、CO32- D. HCO3-、Na+、Cl-、SO42-
难度: 简单查看答案及解析
-
苹果汁是人们喜爱的饮料。由于此饮料中含有Fe2+,现榨的苹果汁在空气中会由淡绿色变为棕黄色,其原因可能是苹果汁中Fe2+变成Fe3+。若榨汁时加入维生素C,可有效防止这种现象发生,这说明维生素C具有
A. 氧化性 B. 还原性 C. 碱性 D. 酸性
难度: 简单查看答案及解析
-
同温同压下,等质量的 SO2气体和 SO3气体相比较,正确的说法是( )
A. 密度比为
B. 物质的量之比为
C. 体积比为
D. 原子数之比为
难度: 困难查看答案及解析