-
下列有关生活、环境、资源等问题叙述不正确的是
A. pH<5.6的雨水称为酸雨
B. “温室效应”主要是由CO2等气体引起的
C. 地球表面约71%被水覆盖,因此淡水资源丰富
D. PM2.5专用口罩中使用了活性炭,是利用了活性炭的吸附性
难度: 中等查看答案及解析
-
下列物质在应用中,只应用其化学性质的是:( )
A. 将活性炭放入冰箱中除去异味
B. 用铅笔芯粉末使锁的开启变的更灵活
C. 用二氧化碳灭火
D. 用一氧化碳来冶炼生铁
难度: 中等查看答案及解析
-
银杏果中含有银杏酸(化学式:C22H34O3),下列有关银杏酸说法正确的是( )
A. 从类别上看:银杏酸不属于氧化物
B. 从含量上看:银杏酸中氢元素的质量分数最大
C. 从宏观上看:银杏酸分子由碳、氢、氧三种元素组成
D. 从微观上看:银杏酸由 22 个碳原子、34 个氢原子和 3 个氧原子构成
难度: 中等查看答案及解析
-
下列对生产、生活现象的解释正确的是( )
A. 石油气加压后贮存在钢瓶中,因为气体分子体积很小
B. 冬天水管里的水结成冰后不再流动,因为分子停止运动
C. 10mL酒精和10mL水混合后,总体积小于20mL,因为分子之间有间隔
D. 温度计里的汞柱下降,因为原子随温度的降低而变小
难度: 简单查看答案及解析
-
正确的实验操作对实验结果、人身安全都非常重要。下列实验操作正确合理的是( )
A.
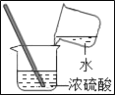 稀释浓硫酸 B.
稀释浓硫酸 B. 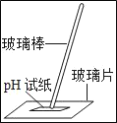 测定溶液的pH
测定溶液的pHC.
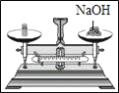 称量氢氧化钠质量 D.
称量氢氧化钠质量 D. 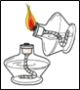 点燃酒精灯
点燃酒精灯难度: 简单查看答案及解析
-
小明的早餐搭配:豆浆、奶油面包、盐水火腿。从营养均衡角度考虑,该食谱中还缺少的营养素是
A. 糖类 B. 油脂
C. 维生素 D. 蛋白质
难度: 简单查看答案及解析
-
下列涉及学科观点的有关说法正确的是( )
A. 微粒观:
和
两个粒子核外电子数相同,属于同种元素
B. 转化观:任何不饱和溶液降低温度后,一定会转化为饱和溶液
C. 能量观:硝酸铵固体溶于水放出热量,天然气燃烧吸收热量
D. 结构观:金刚石和石墨物理性质存在较大差异是由于碳原子排列方式不同
难度: 中等查看答案及解析
-
生活生产中处处离不开化学知识,下列说法中,正确的是( )
A. 煤矿矿井中要严禁烟火,防止爆炸的发生
B. 用甲醛浸泡海产品可保鲜
C. 煤炉上方放一盆水可防止煤气中毒
D. 随意丢弃废旧电池不会污染环境
难度: 中等查看答案及解析
-
如图是不含结晶水的a、b、c 三种物质的溶解度曲线,下列说法正确的是 ( )
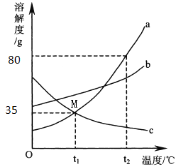
A.t2℃时,将50g a 物质加入到50g 水中充分搅拌,得到100g a的饱和溶液
B.用等质量的a、b、c 三种固体配制成t2℃时的饱和溶液,所得溶液质量的大小关系是:c溶液 > b溶液 > a溶液
C.将t1℃时三种物质的饱和溶液升温到t2℃时,所得溶液中溶质的质量分数的大小关系是: b > a = c
D.将t2℃时a、b 两种物质的饱和溶液降温到t1℃时,析出晶体的质量: a > b
难度: 中等查看答案及解析
-
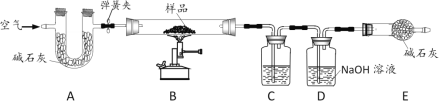
下列实验装置进行的相应实验,达不到实验目的是( )
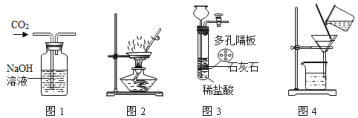
A. 用图1所示装置除去CO2中含有的少量HCl气体
B. 用图2所示的装置加热蒸发NaCl饱和溶液制备NaCl晶体
C. 用图3所示装置可以控制反应的发生和停止
D. 在实验室中,用图4所示装置除去少量河水中的泥沙
难度: 简单查看答案及解析
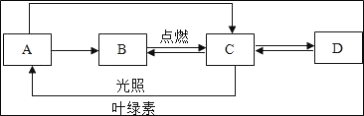

 ”分别表示 N2、H2、NH3,观察下列微观图,选出符合合成氨化学反应过程的微观顺序图(将下面三张图用序号排列)_____。
”分别表示 N2、H2、NH3,观察下列微观图,选出符合合成氨化学反应过程的微观顺序图(将下面三张图用序号排列)_____。