-
《本草衍义》中对精制砒霜过程有如下叙述:“取砒之法,将生砒就置火上,以器覆之,令砒烟上飞着覆器,遂凝结累然下垂如乳,尖长者为胜,平短者次之.”文中涉及的操作方法是( )
A. 蒸馏 B. 干馏 C. 升华 D. 萃取
难度: 简单查看答案及解析
-
下列关于物质或离子检验的叙述正确的是
A. 在溶液中加KSCN,溶液显红色,证明原溶液中有Fe3+,无Fe2+
B. 气体通过无水硫酸铜,粉末变蓝,证明原气体中含有水蒸气
C. 灼烧白色粉末,火焰成黄色,证明原粉末中有Na+,无K+
D. 将气体通入澄清石灰水,溶液变浑浊,证明原气体是CO2
难度: 中等查看答案及解析
-
化学在生活中有着广泛的应用,下列对应关系错误的是
选项
化学性质
实际应用
A
ClO2具有强氧化性
自来水消毒杀菌
B
SO2具有还原性
用作漂白剂
C
NaHCO3受热易分解并且生成气体
焙制糕点
D
Al(OH)3分解吸收大量热量并有H2O生成
阻燃剂
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
广口瓶被称为气体实验的“万能瓶”,是因为它可以配合玻璃管和其他简单仪器组成各种功能的装置。下列各图中能用作防倒吸安全瓶的是( )
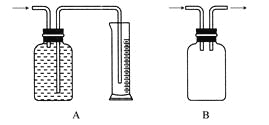
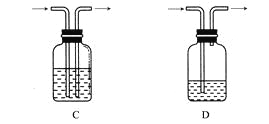
难度: 中等查看答案及解析
-
类推是中学化学中重要的思维方法。下列类推结论正确的是
A. 电解熔融NaCl制取Na,故电解熔融MgCl2也能制取Mg
B. Fe与CuSO4溶液反应置换出Cu,故Na也能从CuSO4溶液中置换出Cu
C. 铝和硫加热得到Al2S3,故铁和硫加热得到Fe2S3
D. 次氯酸钙溶液和CO2反应生成CaCO3和HClO,故次氯酸钙和SO2反应生CaSO3和HClO
难度: 中等查看答案及解析
-
下列溶液中,溶质的物质的量浓度不是1 mol·L-1的是( )
A. 10g NaOH固体溶解在水中配成250mL溶液
B. 将80g SO3溶于水并配成1L的溶液
C. 将0.5mol·L-1的NaNO3溶液100mL加热蒸发掉50g水的溶液
D. 标况下,将22.4L氯化氢气体溶于水配成1L溶液
难度: 简单查看答案及解析
-
由硫酸钾、硫酸铝和硫酸组成的混合溶液,其中c(H+)=0.1 mol·L-1,c(Al3+)=0.4 mol·L-1,c(SO42-)=0.8 mol·L-1,则c(K+)为
A. 0.15 mol·L-1 B. 0.2 mol·L-1
C. 0.3 mol·L-1 D. 0.4 mol·L-1
难度: 中等查看答案及解析
-
如图表示1 g O2与1 g X气体在相同容积的密闭容器中压强(p)与温度(T)的关系,则X气体可能是
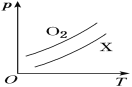
A. C2H4 B. CH4
C. CO2 D. NO
难度: 中等查看答案及解析
-
下列实验设计能够达到实验目的的是
选项
实验目的
实验设计
A
除去CO2中少量的SO2
将混合气体通过饱和Na2CO3溶液
B
除去Cu粉中混有的CuO
向混合物中滴加适量稀硝酸
C
检验溶液中是否含有Fe2+
向溶液中滴入氯水后,再滴加KSCN溶液
D
证明H2CO3的酸性比H2SiO3强
将CO2通入Na2SiO3溶液中
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
下列物质不能通过化合反应生成的是
A. FeCl2 B. H2SiO3 C. CuCl2 D. Fe(OH)3
难度: 中等查看答案及解析
-
设NA代表阿伏加德罗常数的值,下列说法正确的是
A. 在标准状况下,22.4 L氨气分子所含原子总数为4NA
B. 在标准状况下,11.2 L二氯甲烷含氯原子总数为2NA
C. 32g氧气作氧化剂时转移电子数目一定为2NA
D. 1 mol环己烷(
)含非极性键数目为5NA
难度: 中等查看答案及解析
-
“酸化”是实验中经常采用的方法,下列“酸化”错误的是
A. 提高高锰酸钾的氧化能力,用浓盐酸酸化
B. 抑制Fe2(SO4)3的水解,用稀硫酸酸化
C. 确认溶液中含有Cl-时,先用硝酸酸化,再加Ag+检验
D. 确认溶液中含有SO42-时,先用盐酸酸化,再加Ba2+检验
难度: 简单查看答案及解析
-
制备纯净、干燥的氯气,并试验它与金属的反应。每个虚线框表示一个单元装置,其中有错误的是
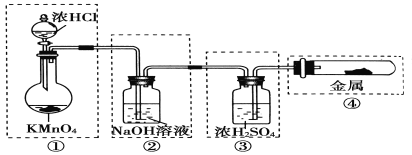
A. ①② B. ② C. ②③ D. ②③④
难度: 中等查看答案及解析
-
下列反应的离子方程式书写正确的是
A. 将铜屑加入含Fe3+的溶液中:2Fe3++Cu=2Fe2++Cu2+
B. 将磁性氧化铁溶于盐酸中:Fe3O4+8H+=3Fe3++4H2O
C. 向硫酸亚铁溶液中加入过氧化氢溶液:Fe2++2H2O2+4H+=Fe3++4H2O
D. 将铁粉加入稀硫酸中:2Fe+6H+=2Fe3++3H2↑
难度: 中等查看答案及解析
-
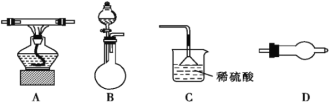
下列图中所示的实验方法、装置或操作正确的是( )
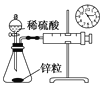
A.测量锌与稀硫酸反应的速率
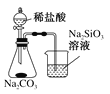
B.证明非金属性:Cl>C>Si
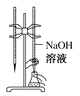
C.进行酸碱中和滴定实验
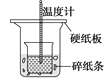
D.测定中和热
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
短周期主族元素W、X、Y、Z、R 原子序数依次增大。由W、X、Y、R组成的一种化合物a在加热时完全分解为三种产物,其中一种产物b是能使品红溶液褪色的气体,另一种产物c是能使湿润的红色石蕊试纸变蓝的气体。金属单质Z在空气中燃烧生成的化合物可与水发生反应生成气体。下列说法正确的是
A. 简单离子的半径: X < Z < R
B. X的简单氢化物比Y的稳定
C. a、b、c中均含有极性共价健,且 a属于电解质,b和c都属于非电解质
D. W、X、Y、R四种元素形成的化合物一定会促进水的电离
难度: 中等查看答案及解析