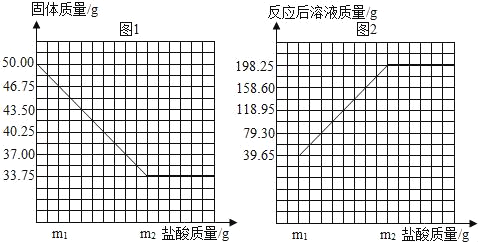
-
向氧化铜和铁粉的混合物中加入一定量稀硫酸,充分反应后过滤,向滤渣中再滴入稀硫 酸,有气泡产生,则下列判断正确的是
A. 滤渣中可能含 Cu B. 滤渣中只含 Fe
C. 滤液中不含 CuSO4 D. 滤液中不一定含 FeSO4
难度: 中等查看答案及解析
-
下列变化属于化学变化的是( )
A. 石蜡熔化 B. 潮湿的衣服被晒干了
C. 钢铁生锈 D. 水变成水蒸气
难度: 简单查看答案及解析
-
以下物质属于纯净物的是( )
A. 白酒 B. 牛奶 C. 冰水混合物 D. 可口可乐
难度: 简单查看答案及解析
-
下列物质可将氢氧化钠溶液与石灰水区分开的是( )
A. 氧气 B. 二氧化碳
C. 紫色石蕊试液 D. 酚酞
难度: 简单查看答案及解析
-
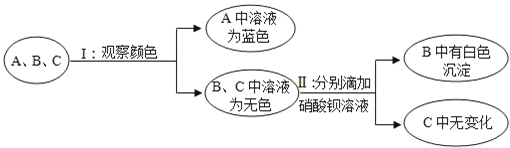
下列试剂中,能把稀硫酸、KOH溶液、CaCl2溶液一次性鉴别出来的是( )
A. KCl溶液 B. 稀盐酸 C. Na2CO3溶液 D. NaNO3溶液
难度: 中等查看答案及解析
-
下列物质NH4Cl、N2、N2O、X、N2O3、NO2、KNO3是按一定的规律排列的,则X应是( )
A. KNO2 B. (NH4)2SO4 C. NO D. N2O5
难度: 简单查看答案及解析
-
如图是不含结晶水的a、b、c 三种物质的溶解度曲线,下列说法正确的是 ( )
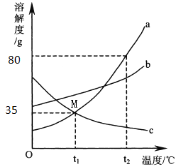
A.t2℃时,将50g a 物质加入到50g 水中充分搅拌,得到100g a的饱和溶液
B.用等质量的a、b、c 三种固体配制成t2℃时的饱和溶液,所得溶液质量的大小关系是:c溶液 > b溶液 > a溶液
C.将t1℃时三种物质的饱和溶液升温到t2℃时,所得溶液中溶质的质量分数的大小关系是: b > a = c
D.将t2℃时a、b 两种物质的饱和溶液降温到t1℃时,析出晶体的质量: a > b
难度: 中等查看答案及解析
-
如图所示装置(不可倒置)有多种用途,下列叙述正确的是( )
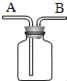
A. 若要除去H2中的CO2,可在此装置中装入NaOH溶液,气体从B端通入
B. 若用排空法往装置内收集H2时,气体应从A端通入
C. 若用水将此装置中的空气排出,水应从A端进入
D. 若用排水法往装置内收集CO时,气体应从A端通入
难度: 简单查看答案及解析
-
在一个密闭容器中有X、Y、Z、Q四种物质,一定条件下充分反应,测得反应前后各物质的质量如表所示:
X
Y
Z
Q
反应前的质量/g
8
10
1
21
反应后的质量/g
0
21
待测
9
已知X和Q两种物质的相对分子质量均为M,下列推理中正确的是( )
A. 反应后物质Z的质量为9g
B. 该反应是分解反应
C. 反应中物质Y与Q发生改变的质量之比为1:1
D. 该反应的化学方程式中,物质X与Q的化学计量数之比为2:3
难度: 简单查看答案及解析
-
下列物质能在pH=1的无色溶液中大量共存的是( )
A. NaNO3、NaCl、KNO3、(NH4)2SO4
B. H2SO4、HCl、AgNO3、Na2SO4
C. KMnO4、CuCl2、Fe2(SO4)3、NaNO3
D. K2SO4、NaCl、K2CO3、NaOH
难度: 中等查看答案及解析
-
常温下,有些盐如CaCl2、NaCl等物质的水溶液呈中性;有些盐如Na2CO3等物质的水溶液呈碱性;有些盐如NH4Cl等物质的水溶液呈酸性。现有HCl与CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH随滴入X的量的变化关系如图所示。则X是( )

A. 水 B. 澄清石灰水 C. 纯碱溶液 D. 稀盐酸
难度: 中等查看答案及解析