-
诗词是民族灿烂文化的瑰宝.下列著名诗句中只含有物理变化的是( )
A.野火烧不尽,春风吹又生 B.粉身碎骨浑不怕,要留清白在人间
C.夜来风雨声,花落知多少 D.春蚕到死丝方尽,蜡炬成灰泪始干
难度: 中等查看答案及解析
-
人在剧烈运动后,血液中会产生较多的乳酸(化学式为C3H6O3),使肌肉酸痛。放松一段时间后,由于乳酸与吸入的氧气反应生成二氧化碳和水,从而使肌肉的酸痛感消失。下列关于乳酸的表述不正确的是( )
A. 乳酸是由碳元素、氢元素、氧元素组成的 B. 乳酸的相对分子质量为90
C. 乳酸中碳元素与氢元素的质量比为1∶2 D. 乳酸中碳元素的质量分数为40%
难度: 中等查看答案及解析
-
下列关于空气的说法中,错误的是( )
A. 空气质量报告中所列的空气质量级别越小,空气质量越好
B. 空气中的稀有气体一般不跟其他物质反应,曾被称为“惰性气体”
C. 空气中的CO2含量逐渐增多的主要原因为化石燃料的大量燃烧
D. 按质量计算,空气中约含氮气78%,氧气21%,其他气体和杂质约占1%
难度: 简单查看答案及解析
-
海带、紫菜等海产品因富含碘元素而成为补碘的常用食物之一,关于碘元素的信息及碘原子的结构示意图如图所示。下列说法错误的是( )

A. 碘原子的相对原子质量为126.9
B. 加碘食盐中含有碘单质,也可为人体补充碘元素
C. 最外层电子数x =7
D. 碘离子核外有54个电子
难度: 简单查看答案及解析
-
下列实验操作,正确的是( )
A.
 取用药品 B.
取用药品 B.  验满氧气
验满氧气C.
 过滤 D.
过滤 D.  收集氢气
收集氢气难度: 简单查看答案及解析
-
银汞合金是目前广泛使用的一种补牙材料。银汞合金补牙的材料中除了银、汞外,还含有锌、锡、铜等金属。下列有关银汞合金的推测不合理的是( )
A. 银汞合金的熔点比汞低
B. 银汞合金是一种金属材料
C. 银汞合金的硬度比锡的大
D. 银汞合金的毒性一定远低于汞的毒性
难度: 简单查看答案及解析
-
逻辑推理是一种重要的化学思维方法,以下推理合理的是( )
A. 因为SO2和SO3的组成元素相同,所以它们的化学性质相似
B. 因为CO2可使紫色石蕊溶液变红,所以CO2属于酸
C. 因为金刚石与石墨的原子排列方式不同,所以它们的化学性质差异很大
D. 因为单质中只含有一种元素,所以含有多种元素的物质一定不是单质
难度: 简单查看答案及解析
-
环境就是民生,青山就是美丽,蓝天也是幸福,绿水青山就是金山银山。如图是某汽车尾气处理净化装置里的微观反应示意图。下列说法正确的是( )
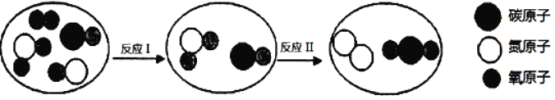
A. 反应Ⅱ前后,分子数目保持不变
B. 反应Ⅰ属于化合反应
C. 反应Ⅱ属于置换反应
D. 反应Ⅰ、Ⅱ历程中,共有两种元素的化合价改变
难度: 简单查看答案及解析
-
为除去下列物质中的少量杂质,所选用的试剂及方法均正确的是( )
选项
物质(括号内为杂质)
试剂及方法
A
CaCl2溶液(HCl)
加入足量的石灰石,过滤
B
CO2 (水蒸气)
缓慢通过盛有生石灰的干燥管
C
CO2(CO)
在氧气中点燃
D
锌粉(CuSO4粉末)
加入足量的水和铁粉后,过滤
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
下列实验事实不能作为相应观点证据的是( )
选项
实验事实
观点
A
过氧化氢分解可制得氧气
化学变化中,分子可分
B
少量KNO3加入水中,不久后“消失”
微粒是不断运动的
C
镁条在空气中燃烧后质量增大
化学反应前后质量守恒
D
5mL苯和5mL冰醋酸混合后体积大于10mL
微粒间存在间隔
A. A B. B C. C D. D
难度: 简单查看答案及解析