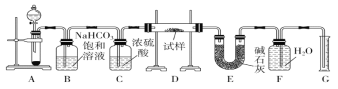
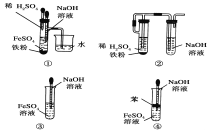
-
有两份质量相同的碳酸氢钠固体,向第一份中加入盐酸使其充分反应;将第二份加热使其完全分解,冷却至原温度再加入相同浓度的盐酸,充分反应,则它们所耗用的盐酸的体积比为( )
A. 2∶1 B. 1∶1 C. 1∶2 D. 4∶1
难度: 简单查看答案及解析
-
在天平的左右两个托盘上放有两个烧杯,两个烧杯中分别盛有盐酸和氢氧化钠溶液,天平处于平衡状态,当分别向两烧杯中加入等质量的铝(酸和碱都是足量的)充分反应后
A. 天平保持平衡 B. 左高右低 C. 左低右高 D. 无法确定
难度: 中等查看答案及解析
-
对于某些离子的检验及结论一定正确的是
A. 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32-
B. 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42-
C. 加稀硝酸酸化后,溶液中无明显变化,再加入AgNO3溶液,生成白色沉淀,能确定有Cl-存在
D. 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
难度: 中等查看答案及解析
-
有关实验的描述,符合事实的是
A. 金属钠暴露在空气里,表面变暗,生成白色的氧化钠固体
B. 用坩埚钳夹住打磨过的镁带,在酒精灯上点燃,发出耀眼的白光,放出大量的热,产生黄色粉末
C. 用坩埚钳夹住铝箔在酒精灯上点燃,发出耀眼的白光,放出大量的热
D. 用坩埚钳夹住一小块铝箔,在酒精灯上加热至熔化,轻轻晃动,有液态的铝滴落下来
难度: 中等查看答案及解析
-
下列关于铁与水蒸气反应的说法中不正确的是( )
A. 反应中有氢气产生 B. 此反应需在加热条件下才能发生
C. 生成的铁的化合物中铁全部呈+3价 D. 该反应中水作氧化剂
难度: 中等查看答案及解析
-
下列关于Na2O2的叙述中正确的是
A. Na2O2是淡黄色固体,久置于空气中变成Na2O
B. Na2O2与水的反应中,Na2O2只作氧化剂
C. Na2O2属于碱性氧化物
D. Na2O2与CO2或H2O反应,1 mol Na2O2参加反应,转移1 mol电子
难度: 中等查看答案及解析
-
把16 g甲烷(CH4)在64 g氧气中完全燃烧后的产物通入足量的过氧化钠后,过氧化钠增加的质量为
A. 48 g B. 16 g C. 80 g D. 32 g
难度: 中等查看答案及解析
-
在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如图所示,则原混合溶液中Al2(SO4)3与MgSO4的物质的量浓度之比为( )
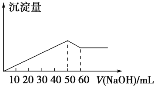
A. 6∶1 B. 3∶1 C. 2∶1 D. 1∶2
难度: 困难查看答案及解析
-
下列物质中既能与稀H2SO4反应, 又能与NaOH溶液反应的化合物是
①NaHCO3 ②Al2O3 ③Al(OH)3 ④Al ⑤(NH4)2 CO3
A.③④ B.①②③⑤ C.①③④ D.全部
难度: 中等查看答案及解析
-
下列各组离子,在某透明溶液中能大量共存的是( )
A. Fe3+ H+ SO32- Na+ B. AlO2— Na+ H+ SO42-
C. NO3— Cu2+ SO42- Cl- D. AlO2— Na+ SO42- HCO3-
难度: 中等查看答案及解析
-
有Fe2+﹑NO3-﹑NH4+﹑Fe3+、H+- H2O六种微粒,分别属于一个氧化还原反应中的反应物和生成物,下列叙述错误的是( )
A. 若有1mol NO3-参加还原反应,则转移8mole- B. 还原产物为NH4+
C. 氧化剂与还原剂的物质的量之比为8:1 D. 该反应中Fe2+被氧化
难度: 中等查看答案及解析
-
有以下物质 ① NaCl溶液 ② 熔融的MgCl2 ③ CuSO4·5H2O固体 ④ NaOH 固体 ⑤ 金属铜 ⑥ 蔗糖。有关它们的说法正确的是
A. 属于非电解质的有①⑤⑥ B. 属于电解质有①②③④
C. 不能导电的有③④⑥ D. 属于混合物的有①②③⑥
难度: 中等查看答案及解析
-
下列反应的离子方程式书写正确的是( )
A. CO2通入NaAlO2溶液中:AlO2—+CO2+H2O===Al(OH)3↓+CO32-
B. Al2O3与过量氨水:Al2O3+6NH3·H2O===2Al3++6NH4+
C. 向AlCl3溶液中加入过量NaOH溶液:Al3++3OH-===Al(OH)3↓
D. 向AlCl3溶液中滴入过量的氨水:Al3++3NH3·H2O===Al(OH)3↓+3NH4+
难度: 中等查看答案及解析
-
在FeCl3、CuCl2、FeCl2的混合溶液中,Fe3+、Cu2+、Fe2+的物质的量之比为3∶2∶1,现加入适量铁粉,使溶液中三种离子的物质的量之比变为1∶2∶4,则参加反应的铁粉与原溶液中Fe3+的物质的量之比为( )
A. 2∶1 B. 1∶2 C. 1∶3 D. 1∶4
难度: 困难查看答案及解析
-
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A. 1 mol氩气在标准状况下的体积约为11.2 L
B. 20 ℃、10 MPa状态下,32 g O2和O3的混合气体所含原子数为2.5NA
C. 标准状况下,11.2 L H2CO3含有的原子数为3NA
D. 常温常压下,44 g CO2含有的原子数为3NA
难度: 中等查看答案及解析
-
下列实验与对应示意图的关系正确的是( )
A
B
C
D
向NaAlO2溶液中逐滴滴加盐酸至过量
向AlCl3溶液中逐滴滴加氨水至过量
向明矾溶液中逐滴滴加
Ba(OH)2溶液至过量
向澄清石灰水中缓缓通入CO2至过量
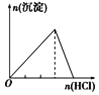
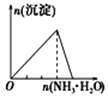
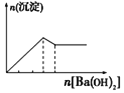
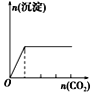
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
下列各组物质混合后,既有气体生成,最终又有沉淀生成的是
①金属钠投入到FeCl3溶液
②过量NaOH溶液和明矾溶液
③过量生石灰投入到少量饱和NH4HCO3溶液
④Na2O2投入FeCl2溶液
A. 只有① B. 只有③ C. 只有②③ D. 只有①③④
难度: 中等查看答案及解析
-
下列有关含铁物质的叙述正确的是( )
A. 向FeCl2溶液中加入NaOH溶液生成红褐色沉淀
B. Fe3+与KSCN溶液反应产生红色沉淀
C. 除去FeCl2溶液中的FeCl3杂质可以向溶液中加入过量铁粉,然后过滤
D. 除去FeCl3溶液中的FeCl2杂质可以向溶液中加入过量铁粉
难度: 中等查看答案及解析
-
下列关于碳酸钠和碳酸氢钠的说法中,正确的是( )
A. 二者在水中的溶解度不同,Na2CO3<NaHCO3
B. 相同浓度的水溶液的碱性不同,Na2CO3>NaHCO3
C. 向等浓度的二者的溶液中滴加相同浓度的盐酸,开始反应时放出气泡的速率不同,Na2CO3大于NaHCO3
D. 二者在一定的条件下不能相互转化
难度: 简单查看答案及解析
-
现有三组物质的分离:①含有水份的植物油中除去水份②回收碘的CCl4溶液中的CCl4③用食用酒精浸泡中草药提取其中的有效成分。分离以上各混合液的正确方法依次是( )
A. 萃取、分液、蒸馏 B. 分液、蒸馏、萃取
C. 萃取、蒸馏、分液 D. 蒸馏、萃取、分液
难度: 简单查看答案及解析
-
将适量的过氧化钠分别投入下列溶液中,有气体放出且溶液质量减轻的是( )
A. 稀硫酸溶液 B. 氯化铁溶液 C. 碳酸氢钠溶液 D. 氯化钠溶液
难度: 困难查看答案及解析
-
下列叙述错误的是( )
A. 丁达尔效应可以用来鉴别胶体和溶液
B. 在水溶液中NaHSO4的电离:NaHSO4=Na++HSO4-
C. 配置FeSO4溶液时,需加入少量铁粉防止Fe2+被氧化
D. 碳酸氢钠在医疗上可用于治疗胃酸过多
难度: 简单查看答案及解析
-
下列离子方程式正确的是( )
A. 过氧化钠加入水中:2O22-+2H2O== 4OH-+O2↑
B. 碳酸氢钠溶液加入盐酸:CO32-+2H+==CO2↑+H2O
C. 氢氧化铜中加入盐酸:OH-+H+==H2O
D. 四氧化三铁跟稀硫酸反应:Fe3O4+8H+==Fe2++2Fe3+ +4H2O
难度: 中等查看答案及解析
-
高铁酸钾(K2FeO4)是一种既能杀菌、消毒,又能絮凝净水的水处理剂。工业制备高铁酸钾的离子方程式为Fe(OH)3+ClO-+OH-
FeO42- +Cl-+H2O(未配平),下列有关说法不正确的是 ( )
A. 由上述反应可知,Fe(OH)3的氧化性强于FeO42-
B. 高铁酸钾中铁显+6价
C. 上述反应氧化剂和还原剂的物质的量之比为3∶2
D. K2FeO4处理水时,不仅能消毒、杀菌,而且生成的Fe3+水解形成Fe(OH)3胶体能吸附水中的悬浮杂质
难度: 困难查看答案及解析