-
R2O8n-在一定条件下可以把 Mn2+氧化为 MnO4-,若反应后 R2O8n-变成 RO42-,又知反应中氧化剂与还原剂的物质的量之比为 5:2,则 R2O8n-中 R 元素的化合价为( )
A. +7 B. +6 C. +3 D. +5
难度: 简单查看答案及解析
-
NA表示阿伏加德罗常数的值,下列判断正确的是
A. 在常温常压下,48g氧气和臭氧的混合气体含氧原子数是3NA
B. 标准状况下,22.4LSO3中含有的原子数目为3NA
C. 1molCl2参加反应转移电子数一定为2NA
D. lmolNa2O2与水充分反应转移的电子数为2NA
难度: 简单查看答案及解析
-
下列关于配制一定物质的量浓度溶液的说法正确的是
A. 容量瓶上标有刻度线、温度和浓度,使用前要事先检查是否漏水
B. 量筒内的残液必须冲洗下来,放入容量瓶中
C. 称量的固体(或量取的液体)可直接放入容量瓶中溶解(或稀释)
D. 定容摇匀后,若液面低于刻度线,不可再次加水补齐
难度: 简单查看答案及解析
-
、下列离子方程式书写正确的是( )
A. 向氢氧化钠溶液中通入足量二氧化碳:OH﹣+CO2===HCO3-
B. 氧化钠投入水中发生反应:O2﹣+H2O===2OH﹣
C. 硝酸银溶液中加入铜粉:Ag++Cu===Cu2++Ag
D. 金属铁溶于稀硫酸中:2Fe+6H+===2Fe3++3H2↑
难度: 中等查看答案及解析
-
下列说法中正确的是
A. 某无色溶液中可能含有下列离子:H+、Cl-、Na+、Fe2+
B. 能使石蕊变红的溶液中可能含有Cl-、K+、Na+、NO3-
C. 取少量某溶液,向其中加入盐酸酸化的BaCl2溶液,通过观察是否有白色沉淀生成,可证明该溶液中是否含有SO42-
D. H++OH-===H2O可描述所有酸碱中和反应的实质
难度: 中等查看答案及解析
-
胶体区别于其他分散系的本质特征是( )
A. 胶体的分散质能通过滤纸空隙,而浊液的分散质不能
B. 产生丁达尔现象
C. 分散质粒子直径在1nm~100nm之间
D. 胶体在一定条件下能稳定存在
难度: 简单查看答案及解析
-
实验中需2mol/L的Na2CO3溶液950ml,配制时应选用的容量瓶的规格和称取的Na2CO3的质量分别是 ( )
A. 1000mL,212g B. 950mL,201.4g C. 任意规格,572g D. 500mL,286g
难度: 中等查看答案及解析
-
某溶液含有NaCl、K2SO4、KCl三种溶质,已知c(Cl﹣)为0.4mol·L-1、c(K+)为0.7 mol·L-1、c(Na+)为0.1 mol·L-1。则该混合溶液中硫酸根离子浓度为
A. 0.1 mol·L-1 B. 0.2 mol·L-1
C. 0.3 mol·L-1 D. 0.4 mol·L-1
难度: 简单查看答案及解析
-
容量瓶上不会标示
A. 标线 B. 容量 C. 温度 D. 浓度
难度: 简单查看答案及解析
-
“靑蒿一握,以水二升渍,绞取汁”,以此获取靑蒿素用到的分离方法是
A. 过滤 B. 蒸馏 C. 蒸发 D. 分液
难度: 简单查看答案及解析
-
进行化学实验必须注意安全。下列做法不正确的是
A. 不慎将酒精灯打翻在桌上失火时,立即用湿抹布盖灭
B. 不慎将酸液溅到眼中,应立即用水冲洗,边洗边眨眼睛
C. 配制稀硫酸时,可先在量筒中加入一定体积水,再在搅拌下慢慢加入浓硫酸
D. 不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液
难度: 中等查看答案及解析
-
如下图所示的是某溶液稀释过程中,溶液的物质的浓度随溶液体积的变化曲线图,根据图中数据分析得出a值等于( )
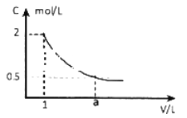
A. 2 B. 3 C. 4 D. 5
难度: 简单查看答案及解析
-
NA为阿伏加德罗常数,标准状况下,mg 氮气和氧气的混合气体含有b个分子,则ng该混合气体在相同状态下的体积为(单位为L) ( )
A.
B.
C.
D.
难度: 简单查看答案及解析
-
标准状况下,mg气体A与ng气体B的分子数目一样多,下列说法不正确的是( )
A. 在任意条件下,若两种分子保持原组成,则其相对分子质量之比为m:n
B. 相同状况下,同体积的气体A与B的质量之比为m:n
C. 同质量的A、B在非标准状况下,其分子数之比为n:m
D. 25℃、1.25×105Pa时,两气体的密度之比为n:m
难度: 简单查看答案及解析
-
有MgCl2和Al2(SO4)3的混合溶液,已知其中Al3+的物质的量浓度为0.4 mol·L-1,SO42-的物质的量浓度为0.7 mol·L-1,Cl-的物质的量浓度为0.2 mol·L-1 ,则Mg2+的物质的量浓度为
A. 0.05 mol·L-1 B. 0.1mol·L-1
C. 0.15 mol·L-1 D. 0.2mol·L-1
难度: 中等查看答案及解析
-
下列离子方程式中正确的是
A. 向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O
Fe(OH)3↓+3H+
B. 小苏打与氢氧化钠溶液混合:HCO3-+OH-=CO2↑+H2O
C. NaHSO4溶液与Ba(OH)2溶液混合后呈中性:H++SO42-+Ba2++OH-=BaSO4↓+H2O
D. 二氧化锰和浓盐酸共热:MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
难度: 简单查看答案及解析
-
分类法是一种行之有效、简单易行的科学方法。某同学用下表所示形式对所学知识进行分类,其中甲与乙、丙、丁是包含关系。下列各组中,正确的组合是( )
选项
甲
乙、丙、丁
A
纯净物
液氯、水玻璃、明矾
B
非电解质
冰醋酸、SO2、乙醇
C
弱电解质
CH3COOH 、氨水、H2O
D
碱性氧化物
CaO、Na2O、K2O
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
常温下,在溶液中可以发生反应X+2Y3+=2Y2++X2+,则下列叙述中①X被氧化;②X是氧化剂;③X具有还原性;④Y2+是氧化产物;⑤Y2+具有还原性;⑥Y3+的氧化性比X2+的氧化性强,正确的是
A. ②④⑥ B. ①③④ C. ①③⑤⑥ D. ②⑤
难度: 中等查看答案及解析
-
盐酸能发生下列反应: ①Zn+2HCl=ZnCl2+H2 ↑,②2HCl+CuO = CuCl2+H2O③MnO2+4HCl
MnCl2+Cl2 ↑+2H2O,因此盐酸应具有的性质是( )
A. 有酸性、氧化性和还原性 B. 只有氧化性
C. 只有还原性 D. 只有酸性
难度: 简单查看答案及解析
-
已知①反应2BrO3-+Cl2=Br2+2C103-;②5Cl2+I2+6H2O=2HIO3+10HCl;③ClO3-+5Cl-+6H+=3Cl2+3H2O,下列物质氧化能力强弱顺序正确的是
A. ClO3->BrO3->IO3->Cl2 B. BrO3->Cl2>ClO3->IO3-
C. BrO3->ClO3->Cl2>IO3- D. Cl2>BrO3-> ClO3->IO3-
难度: 简单查看答案及解析