-
下列过程中,涉及化学变化的是 ( )
A. 四氯化碳萃取碘水中的碘 B. 生石灰被用作干燥剂后失效
C. 过滤除去粗盐中的不溶性杂质 D. 蒸馏法将海水淡化为饮用水
难度: 简单查看答案及解析
-
下列实验操作或记录正确的是( )
A. 常温常压下测得1molN2的质量为28g
B. 用量筒测得排水法收集制得的氢气体积为50.28mL
C. 将洗净的锥形瓶和容量瓶放入烘箱中烘干
D. 用托盘天平称取2.50g胆矾,受热充分失水后,固体质量减轻0.90g
难度: 简单查看答案及解析
-
下列有关物质分类的说法正确的是( )
A. 二氧化硫、二氧化硅、一氧化碳均为酸性氧化物
B. 雾、稀豆浆、氯化钠溶液均为胶体
C. 分子中含三个氢原子的酸不一定是三元酸
D. 烧碱、醋酸、稀硫酸均属于电解质
难度: 简单查看答案及解析
-
现将AlCl3、MgCl2、MgSO4、Al2(SO4)3四种物质溶于水,形成的混合溶液中c(Al3+)=0.1 mol•L﹣1、c(Mg2+)=0.25 mol•L﹣1、c(Cl﹣)=0.2 mol•L﹣1,则该溶液中c(SO42-)为( )
A. 0.15 mol•L﹣1 B. 0.2 mol•L﹣1 C. 0.25 mol•L﹣1 D. 0.30 mol•L﹣1
难度: 中等查看答案及解析
-
运动会上发令枪所用“火药”的主要成分是氯酸钾和红磷,撞击时发生的化学反应为5KClO3+6P=3P2O5+5KCl。下列有关该反应的叙述不正确的是
A. KClO3是氧化剂
B. P2O5是氧化产物
C. 1molKClO3参加反应有6mole-转移
D. 每有6molP被还原,生成5molKCl
难度: 中等查看答案及解析
-
下列对实验过程的评价正确的是( )
A. 某固体中加入稀盐酸,产生了无色气体,证明该固体一定是CaCO3
B. 某溶液中滴加BaCl2溶液,生成不溶于稀硝酸的白色沉淀,该溶液中一定含SO42—
C. 某无色溶液滴入无色酚酞试液显红色,该溶液一定显碱性
D. 验证烧碱溶液中是否含有Cl-,先加稀盐酸除去OH-,再加硝酸银溶液,有白色沉淀出现,证明含Cl-
难度: 简单查看答案及解析
-
除去氯化钠中少量的氯化钙、硫酸钠杂质,下列选用的试剂及加入顺序正确的是
A. Na2CO3、BaCl2、HCl B. BaCl2、Na2CO3、H2SO4
C. BaCl2、Na2CO3、HCl D. Ba(NO3)2、Na2CO3、HCl
难度: 简单查看答案及解析
-
化学与科学、技术、社会、环境密切相关。下列有关说法中错误的是
A. KClO3属于盐,但不能作食用盐食用
B. 自来水一般是采用氯气消毒,为了检验Cl-的存在,可选用硝酸银溶液
C. 为防止月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰或硅胶
D. 把大豆磨碎后,用水溶解其中的可溶性成分,经过滤后,分成豆浆和豆渣
难度: 简单查看答案及解析
-
下列说法中正确的是
A. 不慎将酸或碱液溅入眼内,立即闭上眼睛,用手揉擦
B. 制取并用排水法收集氧气结束后,应立即停止加热
C. 蒸发结晶操作时,为了得到纯净的晶体应将溶液蒸干
D. 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出
难度: 简单查看答案及解析
-
一般检验SO42-的试剂是
A. BaCl2、稀硝酸 B. AgNO3、稀硝酸
C. 稀盐酸、BaCl2 D. AgNO3、稀盐酸
难度: 简单查看答案及解析
-
我们常用“往伤口上撒盐”来比喻某些人乘人之危的行为,其实从化学的角度来说,“往伤口上撒盐”的做法并无不妥,甚至可以说并不是害人而是救人。那么,这种做法的化学原理是
A. 胶体的丁达尔效应
B. 血液的氧化还原反应
C. 血液中发生复分解反应
D. 胶体的聚沉
难度: 简单查看答案及解析
-
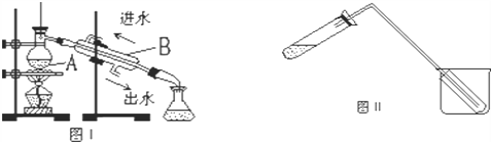
①漏斗 ②试管 ③蒸馏烧瓶 ④天平 ⑤分液漏斗 ⑥研钵
A. ①③⑤ B. ①③④ C. ①②⑥ D. ①③⑥
难度: 中等查看答案及解析
-
在某无色酸性溶液中能大量共存的一组离子是
A.Na+、K+、HCO3、NO3 B.NH4+、SO42、Al3+、NO3
C.Na+、Ca2+、NO3、CO32 D.K+、MnO4、NH4+、NO3
难度: 困难查看答案及解析
-
下列变化过程中,画横线的元素被氧化的是( )
A. CO2→CO B. FeCl3→FeCl2
C. HCl→AgCl D. KI→I2
难度: 简单查看答案及解析
-
需要分离下列两种混合物,选用最合适的实验装置是
a.汽油中不小心混入了大量的水;
b.水与丙酮的混合物,已知:丙酮是一种可与水混溶的无色液体,密度小于水,沸点约为56℃。
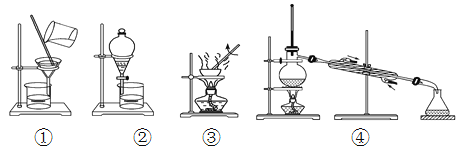
A. ④③ B. ②④ C. ②① D. ④③
难度: 中等查看答案及解析
-
下列说法正确的是
A. NaCl晶体中含有Na+、Cl-,所以NaCl晶体能导电
B. CO2溶于水能导电,所以CO2是电解质
C. BaSO4难溶于水,BaSO4是非电解质
D. Cl2的水溶液能够导电,但Cl2不是电解质
难度: 简单查看答案及解析
-
NA代表阿伏加德罗常数的值,下列说法正确的是
A. 在常温常压下,28 g N2与CO混合物气体中所含的分子数目一定为NA
B. 标准状况下,17 g氨气所含原子数目为NA
C. 在常温常压下,11. 2 L氮气所含的原子数目为NA
D. 10 mL 2 mol/LH2SO4溶液中取出的5 mL溶液,其浓度为1 mol/L
难度: 简单查看答案及解析
-
下列离子方程式正确的是
A. 稀硝酸与氢氧化钾溶液反应:H++OH﹣=H2O
B. 铁与稀盐酸反应:Fe+2H+=Fe3++H2↑
C. 三氯化铁溶液与氢氧化钠溶液反应:FeCl3+3OH﹣=Fe(OH)3↓+3Cl﹣
D. 足量二氧化碳与澄清石灰水反应:CO2+2OH﹣=CO32-+H2O
难度: 简单查看答案及解析
-
常温常压下,将等质量的氢气、甲烷、氧气、二氧化碳四种气体分别吹入四个气球,气球中气体为甲烷的是
A.
B.
C.
D.
难度: 简单查看答案及解析
-
已知下列分子或离子在酸性条件下都能氧化KI,自身发生如下变化:H2O2→H2O,IO3﹣→I2,MnO4-→Mn2+,HNO2→NO,如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是
A. H2O2 B. IO3-
C. MnO4- D. HNO2
难度: 简单查看答案及解析