-
下列溶液与20mL 1 mol·L—1 NaNO3溶液中NO3—物质的量浓度相等的是( )
A. 10 mL 1 mol·L—1 Mg(NO3)2溶液 B. 5 mL 0.8 mol·L—1 Al(NO3)3溶液
C. 10 mL 2 mol·L—1 AgNO3溶液 D. 10 mL 0.5 mol·L—1 Cu(NO3)2溶液
难度: 中等查看答案及解析
-
下列化学方程式中,不能用离子方程式Ba2+ + SO42- = BaSO4↓表示的是
A. Ba(NO3)2 +H2SO4= BaSO4↓+2HNO3 B. BaCl2+ Na2SO4= BaSO4↓+2 NaCl
C. BaCO3 + H2SO4= BaSO4↓+ H2O+CO2↑ D. BaCl2+ H2SO4= BaSO4↓+2HCl
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数,下列对于0.3mol/L的硫酸钾溶液的说法中不正确的是
A. 1L溶液中含有0.6NA个钾离子
B. 1L溶液中含有钾离子和硫酸根离子总数为0.9NA
C. 2L溶液中钾离子浓度为1.2mol/L
D. 2L溶液中含有硫酸根离子0.6NA个
难度: 中等查看答案及解析
-
下列实验操作正确的是
A. 当某实验没有准确的药品用量说明时,为看到明显现象,取用药品越多越好
B. 取用细口瓶里的试液时,先拿下瓶塞,倒放在桌上,然后标签朝外拿起瓶子,瓶口要紧挨着试管口,将液体缓缓地倒入试管
C. 胶头滴管取完一种试液后,可直接取另一种不与其反应的试液
D. 取用粉末状固体或固体小颗粒时,应用药匙或纸槽,取用块状固体时,应用镊子夹取
难度: 简单查看答案及解析
-
在同温同压下,相同体积的甲、乙两种气体的质量比是17∶14。若乙气体是CO,则甲气体可能是( )
A. H2S B. HCl C. NH3 D. Cl2
难度: 中等查看答案及解析
-
下列溶液中溶质的物质的量浓度为1mol/L的是( )
A. 将40gNaOH溶解在1L水中
B. 将1L10mol/L的浓盐酸加入9L水中
C. 将22.4LHCl气体溶于水配成1L溶液
D. 将10gNaOH溶解在少量水中,再加蒸馏水直到溶液体积为250mL
难度: 中等查看答案及解析
-
用10 mL的0.1 mol·L-1 BaCl2溶液恰好可使相同体积的硫酸铁、硫酸锌和硫酸钾三种溶液中的硫酸根离子完全转化为硫酸钡沉淀,则三种硫酸盐溶液的物质的量浓度之比是
A. 3∶2∶2 B. 1∶2∶3 C. 1∶3∶3 D. 3∶1∶1
难度: 中等查看答案及解析
-
设NA表示阿伏加德罗常数,下列说法正确的是 ( )
A. 1 mol氦气中有2NA个氦原子
B. 14 g氮气中含NA个氮原子
C. 2 L 0.3 mol·L-1Na2SO4溶液中含0.6 NA个Na+
D. 18 g水中所含的电子数为8NA
难度: 中等查看答案及解析
-
将30 mL 0.5 mol·L-1NaOH溶液加水稀释到500mL,稀释后溶液中NaOH的物质的量浓度为
A. 0.3 mol·L-1 B. 0.03 mol·L-1 C. 0.05 mol·L-1 D. 0.04 mol·L-1
难度: 简单查看答案及解析
-
下列物质属于电解质的是( )
A. 铜 B. 食盐水 C. 烧碱 D. 蔗糖
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.能电离出H+ 的化合物叫做酸
B.实验测得1mol某气体体积为22.4 L,测定条件一定是标准状况
C.摩尔是七个基本物理量之一
D.化合物分为酸、碱、盐和氧化物是用树状分类法分类的
难度: 简单查看答案及解析
-
配制100mL1.0mol·L-1的NaOH溶液,下列情况不会影响溶液浓度的是
A. 容量瓶使用前有蒸馏水
B. 配制过程中,未用蒸馏水洗涤烧杯和玻璃棒
C. 俯视确定凹液面与刻度线相切
D. 称量NaOH固体时使用了称量纸
难度: 简单查看答案及解析
-
下列实验方法或操作正确的是( )
A.
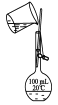 B.
B. 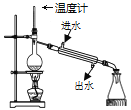 C.
C. 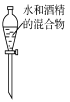 D.
D. 
难度: 中等查看答案及解析
-
1g N2中含有x个原子,则阿伏加德罗常数是( )
A.
mol—1 B.
mol—1 C. 14x mol—1 D. 28x mol—1
难度: 简单查看答案及解析
-
下列各组中的离子,能在水溶液中大量共存的是
A. K+、H+、SO42—、OH— B. Na+、Ca2+、CO32—、NO3—
C. Na+、H+、Cl—、CO32— D. Na+、Cu2+、SO42—、Cl—
难度: 简单查看答案及解析
-
下列离子方程式中,正确的是( )
A. 稀硫酸滴在铜片上:Cu + 2H+= Cu2++ H2↑
B. 氧化镁与稀盐酸混合:MgO + 2H+= Mg2++ H2O
C. 铜片插入硝酸银溶液中:Cu + Ag+= Cu2++ Ag
D. 铁与稀硫酸反应 2 Fe + 6H+= 2Fe3++ 3H2↑
难度: 简单查看答案及解析
-
200 ml Fe2(SO4)3溶液中含Fe3+ 56g,溶液中SO42—的物质的量浓度是( )
A. 5mol/L B. 7.5 mol/L C. 10 mol/L D. 2.5 mol/L
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数,下列说法正确的是( )
①标准状况下,11.2 L以任意比例混合的氮气和氧气所含的原子数为NA
②同温同压下,体积相同的氢气和氩气所含的分子数相等
③1 L 2 mol·L-1的氯化镁溶液中含氯离子为4NA
④标准状况下22.4 L H2O中分子数为NA
⑤32 g O2和O3混合气体中含有原子数为2NA
A. ①②③④ B. ③④
C. ①③④ D. ①②③⑤
难度: 困难查看答案及解析
-
下列有关化学实验安全问题的叙述中,不正确的是( )
A. 少量的浓硫酸沾到皮肤上时,迅速用干布擦拭,再用大量水冲洗
B. 取用化学药品时,应特别注意观察药品包装容器上的安全警示标志
C. 凡是给玻璃仪器加热,都要加垫石棉网,以防止仪器炸裂
D. 闻任何化学药品的气味都不能使鼻子凑近药品
难度: 简单查看答案及解析
-
下列有关使用托盘天平的叙述,不正确的是( )
①称量前先调节托盘天平的零点 ;②称量时左盘放被称量物,右盘放砝码;③潮湿的或有腐蚀性的药品,必须放在玻璃器皿里称量,其他固体药品可直接放在天平托盘上称量; ④用托盘天平可以准确称量5.85g的固体食盐;⑤称完,应把砝码放回砝码盒中。
A. ②③ B. ②④ C. ③④ D. ③
难度: 中等查看答案及解析
-
下列说法中不正确的是( )
A. 1 mol 氧气中含有1.204×1024个氧原子,占有体积22.4 L
B. 1 mol臭氧和1.5 mol氧气含有相同的氧原子数
C. 等体积、浓度均为1 mol/L的硫酸和盐酸,电离出的氢离子数之比为2∶1
D. 等物质的量的干冰和葡萄糖(C6H12O6)中所含碳原子数之比为1∶6,氧原子数之比为1∶3
难度: 中等查看答案及解析
-
已知1.505×1023个X气体分子的质量为8 g,则X气体的摩尔质量是( )
A. 16 g B. 32 g C. 64 g/mol D. 32 g/mol
难度: 简单查看答案及解析
-
有NaCl、FeCl3、CuCl2、Na2SO4四种溶液,只用一种试剂能够鉴别它们,该试剂是( )
A. 盐酸 B. 烧碱溶液
C. 氢氧化钡溶液 D. 氯化钡溶液
难度: 中等查看答案及解析
-
对于某些离子的检验及结论中一定正确的是( )
A. 加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中,溶液变浑浊,则一定有CO32-
B. 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,则一定有SO42-
C. 分别含有Mg2+、Cu2+和Na+的三种盐酸盐溶液,用NaOH溶液就能一次鉴别开
D. 加入碳酸钠溶液产生白色沉淀,再加盐酸,白色沉淀消失,一定有Ba2+
难度: 中等查看答案及解析