-
配制一定物质的量浓度的NaCl溶液时,下列因素对结果没有影响的是
A. 溶解过程中有少量液体溅出 B. 容量瓶使用前未干燥
C. 洗涤液未全部转移到容量瓶中 D. 定容时液面未到刻度线
难度: 简单查看答案及解析
-
宋代《开宝本草》中记载了KNO3的提纯方法 “…所在山泽,冬月地上有霜,扫取以水淋汁后,乃煎炼而成”,这里不涉及到的操作方法是 ( )
A. 蒸馏 B. 蒸发 C. 结晶 D. 溶解
难度: 简单查看答案及解析
-
已知反应①2BrO3-+Cl2==Br2+2ClO3- ②5C12+I2+6H2O==2HIO3+10HCl
③ClO3-+5C1-+6H+==3Cl2+3H2O,下列物质氧化能力强弱顺序正确的是( )
A. ClO3-﹥BrO3-﹥IO3-﹥C12 B. BrO3-﹥C12﹥ClO3-﹥IO3-
C. BrO3-﹥ClO3-﹥C12﹥IO3- D. C12﹥BrO3-﹥ClO3-﹥IO3-
难度: 中等查看答案及解析
-
已知: 2KMnO4+16HCl(浓) = 2KCl+5Cl2↑+2MnCl2+8H2O,下列说法正确的是
A. HCl发生了还原反应
B. 氧化性: Cl2>KMnO4
C. 氧化剂与还原剂的物质的量比为1 : 8
D. 当标准状况下产生22.4L氯气,转移电子数为2NA
难度: 中等查看答案及解析
-
下列溶液中含Cl-浓度最大的是
A. 10mL 0.1mol/L的FeCl3溶液 B. 20mL 0.1mol/LCaCl2溶液
C. 30mL 0.2mol/L的KCl溶液 D. 100mL 0.25mol/L的NaCl溶液
难度: 中等查看答案及解析
-
下列物质中,摩尔质量最大的是
A. 10 mL H2O B. 0.8 mol H2SO4 C. 54 g Al D. 1 g CaCO3
难度: 简单查看答案及解析
-
在容量瓶上,没有标记符号的是
A. 标线 B. 温度
C. 物质的量浓度 D. 容量
难度: 简单查看答案及解析
-
很多人喜欢逛超市,走进超市可以看到饮料区的货架上放有碳酸饮料,顾名思义,碳酸饮料就是饮料中溶解了碳酸;人身体有汗时容易发生触电事故;把一个橘子,插入电极接入电路,也能导电。则下列有关说法不正确的是( )
A. 碳酸是电解质,而碳酸饮料是电解质溶液
B. 身体有汗容易发生触电事故,是因为人的汗液中含有自由移动的无机盐离子
C. 二氧化碳溶于水形成碳酸能导电,所以二氧化碳是电解质
D. 橘子能导电,是因为在橘子汁中存在自由移动的离子
难度: 简单查看答案及解析
-
在盛放浓硫酸的试剂瓶的标签上应印有下列警示标志中的( )
A.
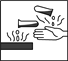 B.
B.  C.
C. D.
难度: 简单查看答案及解析
-
某血液化验单中“总胆固醇”一项的结果为4.27×10−3 mol/L。这里的“4.27×10−3 mol/L”表示总胆固醇的
A. 质量分数 B. 摩尔质量
C. 物质的量 D. 物质的量浓度
难度: 简单查看答案及解析
-
工业上冶炼钛有如右反应:TiCl4+2Mg
Ti+2MgCl2该反应属于
A. 化合反应 B. 分解反应 C. 置换反应 D. 复分解反应
难度: 简单查看答案及解析
-
下列物质属于非电解质的是
A. 烧碱 B. 干冰 C. 金刚石 D. 硫酸
难度: 简单查看答案及解析
-
下列仪器名称为“分液漏斗”的是
A.
 B.
B.  C.
C. 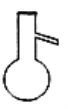 D.
D. 
难度: 简单查看答案及解析
-
下列分散质粒子直径在1~100 nm之间的分散系是
A. 鸡蛋清溶液 B. 盐酸
C. Cu(OH)2悬浊液 D. CuSO4溶液
难度: 中等查看答案及解析
-
下列物质溶于水,电离方程式错误的是
A. Na2CO3 = Na+ + CO32-
B. H2SO4 = 2H++ SO42-
C. MgCl2 = Mg2++2Cl-
D. NaHSO4 = Na++H++ SO42-
难度: 中等查看答案及解析
-
从溴水中分离溴,下列物质不能作为萃取剂的是
A. 汽油 B. 苯 C. 乙醇 D. 四氯化碳
难度: 简单查看答案及解析
-
下列各组物质,按酸、混合物、碱顺序排列的是
A. 空气、硫酸铜、硫酸 B. 乙酸、空气、纯碱
C. 氧化铁、胆矾、熟石灰 D. 硝酸、蔗糖水、氢氧化铁
难度: 简单查看答案及解析
-
下列反应既属于化合反应,又属于氧化还原反应的是( )
A. Fe +2 HCl = H2 ↑+ FeCl2 B. 2FeCl2 + Cl2 = 2FeCl3
C. CaO + H2O = Ca(OH)2 D. 2Fe(OH)3 = Fe2O3 + 3H2O
难度: 中等查看答案及解析
-
己知在碱性溶液中可发生如下反应:
2R(OH)3+ 3C1O-+ 4OH-= 2RO4n-+3Cl-+5H2O。则RO4n-中R的化合价是( )
A. +3 B. +4 C. +5 D. +6
难度: 中等查看答案及解析
-
下列各组中的离子,能在溶液中大量共存的是
A. K+、H+、SO42-、OH- B. Ca2+、Na+、NO3-、CO32-
C. Mg2+、Na+、Cl-、SO42- D. H+、Na+、HCO3-、Cl-
难度: 中等查看答案及解析
-
下列说法正确的是
A. H2的摩尔质量是2g B. 1mol OH-的质量是17g
C. 摩尔是物质的质量单位 D. 1mol气体所占的体积约为22.4L
难度: 简单查看答案及解析
-
操作规范是化学实验的基本要求。下列实验操作正确的是
A. 检查容量瓶是否漏水
 B. 给液体加热
B. 给液体加热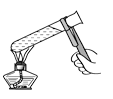
C. 滴加试液
D. 过滤
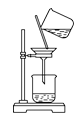
难度: 中等查看答案及解析
-
下列物质溶液间中的反应可用离子方程式OH-+ H+= H2O表达的是
A. H2SO4和Ba(OH)2 B. NH3·H2O和HCl
C. NaHSO4和KOH D. NaHCO3和NaOH
难度: 中等查看答案及解析
