-
下列物质分类的正确组合是( )
选项
混合物
纯净物
单质
电解质
A
盐酸
NaOH
石墨
K2SO4溶液
B
空气
Fe(OH)3胶体
铁
Na2CO3
C
CuSO4·5H2O
CaCl2
水银
铜
D
氯水
KNO3晶体
O3
NaCl
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
某化合物由两种单质直接反应生成,将其加入Ba(HCO3)2溶液中同时有气体和沉淀产生。下列化合物中符合上述条件的是
A. AlCl3 B. Na2O
C. FeCl2 D. SiO2
难度: 困难查看答案及解析
-
下列对古文献记载内容理解错误的是
A. 《天工开物》记载:“凡埏泥造瓦,掘地二尺余,择取无沙黏土而为之”。“瓦”,传统无机非金属材料,主要成分为硅酸盐。
B. 《本草纲目》“烧酒”条目下写道:“自元时始创其法,用浓酒和糟入甑,蒸令气上……其清如水,味极浓烈,盖酒露也”。这里所用的“法”是指蒸馏。
C. 《抱朴子·金丹篇》中记载:“丹砂烧之成水银,积变又还成丹砂”。该过程未发生氧化还原反应。
D. 《本草经集注》中关于鉴别硝石(KNO3)和朴硝(Na2SO4)的记载:“以火烧之,紫青烟起,乃真硝石也”,该方法应用了焰色反应。
难度: 中等查看答案及解析
-
化学与人类社会生产、生活密切相关。下列说法中正确的是
A. 误食重金属盐引起人体中毒,可喝大量的食盐水解毒
B. 燃料的脱硫脱氮、SO2的回收利用和NOx的催化转化都是减少酸雨产生的措施
C. 碳酸钡可用于胃肠X 射线造影检查
D. 生石灰可用作食品抗氧化剂
难度: 中等查看答案及解析
-
根据所给的信息和标志,判断下列说法错误的是( )
A
B
C
D
《神农本草经》记载,麻黄能“止咳逆上气”
碳酸氢钠药片


古代中国人已用麻黄治疗咳嗽
该药是抗酸药,服用时喝些醋能提高药效
看到有该标志的丢弃物,应远离并报警
贴有该标志的物品是可回收物
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
设nA为阿伏伽德罗常数的数值,下列说法正确的是
A. 23g Na 与足量H2O反应完全后可生成nA个H2分子
B. 1 molCu和足量热浓硫酸反应可生成nA个SO3分子
C. 标准状况下,22.4L N2和H2混合气中含nA个原子
D. 3mol单质Fe完全转变为Fe3O4,失去8nA个电子
难度: 中等查看答案及解析
-
25℃时,下列各组离子在指定溶液中一定能大量共存的是
A. 由水电离产生的c(H+)=1×10-13mol/L的溶液中:Na+、Ba2+、NO3-、Cl-
B. 0.1 mol/L的Fe(NO3)3溶液中:Na+、H+、Cl-、I-
C. 0.1 mol/L的NaAlO2溶液中:K+、H+、NO3-、SO42-
D. 滴入石蕊试液显蓝色的溶液中:K+、Na+、HSO3-、ClO-
难度: 中等查看答案及解析
-
下列有关离子方程式正确的是
A. 稀硝酸和过量的铁屑反应:Fe+4H++NO3-===Fe3++NO↑+2H2O
B. 向硫酸氢钠溶液中加入氢氧化钡溶液至中性,则离子方程式为:2H++SO42-+2OH-+Ba2+===BaSO4↓+2H2O
C. 氯气溶于水:Cl2+H2O⇌2H++Cl-+ClO-
D. 向NaAlO2溶液中通入过量的CO2:2AlO2-+CO2+3H2O===2Al(OH)3↓+CO32-
难度: 中等查看答案及解析
-
下列关于分散系的说法不正确的是
A. 直径为1.3×10-9 m的“钴钛菁”分子在水中形成的分散系属于胶体
B. 向沸水中滴加适量饱和FeCl3溶液,能形成带电的胶体
C. 向氢氧化铁胶体中滴加稀硫酸,先产生沉淀,后沉淀溶解
D. 利用丁达尔效应可区分溶液与胶体
难度: 中等查看答案及解析
-
某实验室需要 1.0 mol/L 的碳酸钠溶液 450 mL,利用碳酸钠晶体(Na2CO3·10H2O)来配制。下列说法正确的是
A. 应称取该碳酸钠晶体128.7 g
B. 取 100 mL 该溶液,向其中加入100 mL 水,所得溶液浓度为0.5 mol/L
C. 定容时俯视刻度线会引起配制溶液的浓度偏高
D. 定容、摇匀、静置后发现液面低于刻度线,应再补加少量水至刻度线
难度: 中等查看答案及解析
-
关于反应2KI+O3+H2O ==2KOH+I2+O2,下列说法正确的是
A.当有2 molKI被氧化时,2 mol氧原子被还原
B.O2是还原产物
C.若消耗2.24 L O3,则转移0.2 mol电子
D.氧化剂与还原产物的物质的量之比为1:1
难度: 中等查看答案及解析
-
下列实验所述的变化过程与氧化还原反应无关的是
A
B
C
D
实验
NaOH 溶液滴入FeSO4 溶液中
石蕊溶液滴入氯水中
向 K2Cr2O7 溶液
中滴加浓硫酸
CO2 通入 Na2O2
现象
产生白色沉淀,最
终变为红褐色
溶液变红,随后迅速褪色
溶液黄色变浅,
橙色加深
固体逐渐变白
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
高纯度单晶硅是典型的无机非金属材料,又称“半导体”材料,它的发现和使用曾引起计算机的一场“革命”。这种材料可以按下列方法制备,下列说法正确的是
SiO2
Si(粗)
SiHCl3
Si(纯)
A. 步骤①的化学方程式为SiO2+C
Si+CO2↑
B. 步骤①、②、③中每生成或反应1 mol Si,转移2 mol电子
C. 二氧化硅能与氢氟酸反应,而硅不能与氢氟酸反应
D. SiHCl3(沸点33.0 ℃)中含有少量的SiCl4(沸点67.6 ℃),通过蒸馏可提纯SiHCl3
难度: 中等查看答案及解析
-
A、B、C、X均为中学化学常见物质,一定条件下它们有如图所示转化关系(部分产物已略去)。下列说法正确的是

A. 若X为O2,则A可为有机物乙醇,也可为非金属单质硫
B. 若X为KOH溶液,则A可能为Al
C. 若A、B、C均为焰色反应呈黄色的化合物,则X一定为CO2
D. 若X为Fe,则C可能为Fe(NO3)2溶液
难度: 中等查看答案及解析
-
现有两瓶无标签的无色溶液,分别装有Na2CO3和NaHCO3,用下列试剂或方法能将两者区分的是
①Ca(OH)2 ②盐酸 ③CaCl2 ④NaOH ⑤加热
A. ①③ B. ①④ C. ②③ D. ②⑤
难度: 中等查看答案及解析
-
下列除去杂质的方法不正确的是( )
A. 镁粉中混有少量铝粉:加入过量烧碱溶液充分反应,过滤、洗涤、干燥
B. 用过量氨水除去Fe3+溶液中的少量Al3+
C. Al(OH)3中混有少量Mg(OH)2:加入足量烧碱溶液,充分反应,过滤,向滤液中通入过量CO2后过滤
D. MgO中混有少量Al2O3:加入足量烧碱溶液,充分反应,过滤、洗涤、干燥得到MgO
难度: 中等查看答案及解析
-
下列说法正确的是
A. 由反应SiO2+4HF===SiF4↑+2H2O,可知SiO2是碱性氧化物
B. 浓硝酸在光照下颜色变黄,说明浓硝酸见光易分解
C. SO2、漂白粉、活性炭、Na2O2都能使红墨水褪色,其原理相同
D. SO2和Cl2等物质的量混合后通入装有湿润的有色布条的集气瓶中,漂白效果更好
难度: 中等查看答案及解析
-
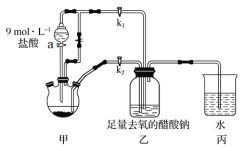
某同学用下列装置制备并检验Cl2的性质,下列说法正确的是
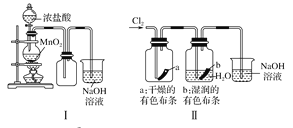
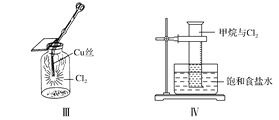
A. Ⅰ图中:如果MnO2过量,浓盐酸就可全部消耗
B. Ⅱ图中:湿润的有色布条能褪色,烧杯NaOH溶液的作用是吸收尾气
C. Ⅲ图中:生成蓝色的烟
D. Ⅳ图中:量筒中发生了加成反应,量筒内液面上升,量筒壁上有无色液滴出现
难度: 中等查看答案及解析
-
下列有关实验操作、现象、解释或结论都正确的是
选项
实验操作
现象
解释或结论
A
充分吸收了Na2SiO3 饱和溶液的小木条,沥干后放在酒精灯外焰加热
小木条不燃烧
Na2SiO3 可作防火剂
B
将H2 在充满Cl2 的集气瓶中燃烧
集气瓶口上方有白烟生成
H2、Cl2 化合生成HCl
C
将SO2 通入酸性高锰酸钾溶液中
溶液褪色
SO2 具有漂白性
D
用分别蘸有浓盐酸和浓氨水的玻璃棒相互靠近
冒白烟
NH3 具有还原性
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
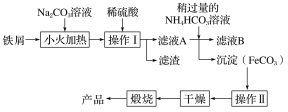
从某含有FeCl2、FeCl3、CuCl2的工业废液中回收铜并制备氯化铁晶体的流程如下:则下列说法正确的是
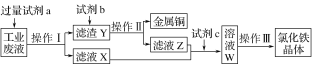
A. 试剂a是铁、试剂b是稀硫酸
B. 操作Ⅰ、操作Ⅱ、操作Ⅲ所用仪器相同
C. 试剂c是氯气,相应的反应为: 2Fe2++Cl2===2Cl-+2Fe3+
D. 用酸性KMnO4溶液可检验溶液W中是否还有Fe2+
难度: 中等查看答案及解析
-
将3.48g四氧化三铁完全溶解在100mL 1mol·L-1 的硫酸中,然后加入K2Cr2O7溶液25mL,恰好使溶液中的Fe2+全部转化为Fe3+,Cr2O72-全部转化为Cr3+,则K2Cr2O7溶液的物质的量浓度是
A.0.05mol·L—1 B.0.1mol·L—1
C.0.2mol·L—1 D.0.3mol·L—1
难度: 中等查看答案及解析