-
2014年世界环境日的主题是“思前、食后、厉行节约”。下列做法正确的是
A.霉变大米,洗净再吃 B.燃气泄漏,点火检验
C.鱼虾保鲜,甲醛浸泡 D.治理雾霾,节能减排
难度: 简单查看答案及解析
-
收藏家收藏的清末铝制品至今保存十分完好,该艺术品不易锈蚀的原因( )
A. 铝的氧化物容易发生还原反应
B. 铝不易氧化
C. 铝易氧化,但铝表面的氧化铝具有保护内部铝的作用
D. 铝不易发生化学反应
难度: 简单查看答案及解析
-
化学是材料科学、生命科学、环境科学和能源科学的重要基础.下列说法正确的是
A.合金、合成纤维、合成橡胶都是有机合成材料
B.酒精、吗啡、海洛因都是毒品
C.二氧化硫、二氧化氮、粉尘都是大气污染物
D.石油、煤、氢气都是不可再生的化石燃料
难度: 中等查看答案及解析
-
如果把厨房中的①食盐、②料酒、③豆油、④白糖、⑤面粉、⑥面酱分别放入水中充分搅拌,能够得到溶液的是( )
A. ①②④
B. ①②⑥
C. ④⑤⑥
D. ③⑤⑥
难度: 简单查看答案及解析
-
下列有关金属的说法中,正确的是( )
A. 纯铁,可用来制造机械
B. 地壳中含量最多的金属元素是铁
C. 铁、铝的表面都有一层致密的氧化物薄膜
D. 铜的导电性在金属中仅次于银,常用作导线
难度: 简单查看答案及解析
-
日常生活中的下列物质中加入紫色石蕊溶液无明显变化的是( )
A. 柠檬汁
B. 苹果汁
C. 纯净水
D. 石灰水
难度: 中等查看答案及解析
-
CuO、稀硫酸、Ba(OH)2溶液、Na2CO3溶液四种物质,在常温下两两混合能发生的化学反应有( )
A. 3个
B. 4个
C. 5个
D. 6个
难度: 中等查看答案及解析
-
下列物质中,不属于糖类的是
A.葡萄糖 B.淀粉 C.蛋白质 D.纤维素
难度: 简单查看答案及解析
-
在一定条件下,反应的浓度越大,则化学反应速率越快,现有50 g溶质质量分数为30%的硫酸溶液与过量的锌粉反应,为了减缓反应速率,而又不影响生成H2的总质量,可向该硫酸中加入适量的( )
A. 碳酸钾溶液
B. 稀盐酸
C. 氧化铁
D. 水
难度: 中等查看答案及解析
-
蛋白质是构成人体的基本物质,下列食物中富含蛋白质的是( )
A.植物油 B.西红柿 C.马铃薯 D.红烧鱼
难度: 简单查看答案及解析
-
下列物品所使用的主要材料属于有机合成材料的是( )
A. 陶瓷茶杯
B. 塑料凉鞋
C. 纯棉T恤
D. 不锈钢饭盒
难度: 简单查看答案及解析
-
地壳中含量最多的金属元素与非金属元素组成的化合物的化学式为( )
A. SiO2
B. FeO
C. Fe3O4
D. Al2O3
难度: 简单查看答案及解析
-
下列事实不能说明Zn比Ag活泼的是( )
A. Zn能与AgNO3溶液反应置换出Ag
B. Zn能与稀硫酸反应,Ag则不能
C. 自然界没有以单质形式存在的Zn,而有以单质形式存在的Ag
D. Zn的熔点为420 ℃,Ag的熔点为962 ℃
难度: 中等查看答案及解析
-
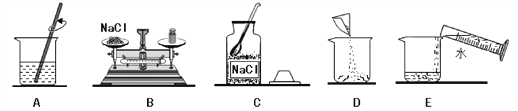
以下用品中,主要利用金属导热性的是( )
A.

B.

C.
D.

难度: 简单查看答案及解析
-
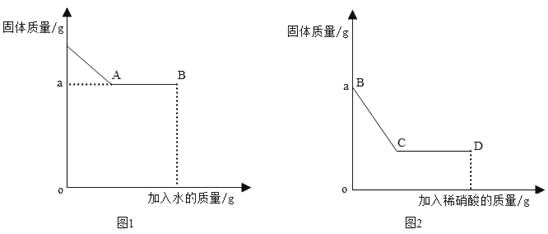
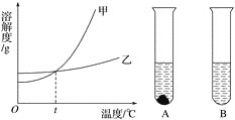
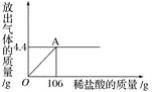
下列曲线正确的是( )
A. 向等体积、等浓度的稀盐酸中加金属
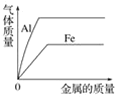
B. 向稀硝酸中加水
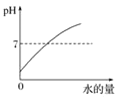
C. 双氧水分解
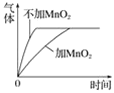
D. 向等体积、等浓度的稀盐酸中加金属
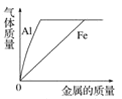
难度: 简单查看答案及解析
-
判断下列化学方程式中,属于分解反应的是( )
A.H2SO4+2NaOH═Na2SO4+2H2O
B.2H2O
2H2↑+O2↑
C.2CO+O2
2CO2
D.Fe+CuSO4═FeSO4+Cu
难度: 简单查看答案及解析
-
下列各组物质混合后不能发生反应的是
A.银和稀盐酸
B.。..氢氧化钡溶液和硝酸
C.铝和稀硫酸
D.氯化钡溶液和硫酸钠溶液
难度: 困难查看答案及解析
-
下列措施或方法不能达到目的是( )
A. 铵态氮肥与熟石灰混合使用,增强肥效
B. 用10 mL的量筒量取9.5 mL的水
C. 用pH试纸测得某溶液的pH为7
D. 油锅着火,用锅盖盖灭
难度: 简单查看答案及解析
-
下列实验现象描述正确的是( )
A. 将干燥的紫色小花(石蕊浸泡)放到二氧化碳气体中,小花由紫色变成红色
B. 铁锈与稀盐酸反应后,溶液由无色变成了浅绿色
C. 硫酸铵和熟石灰混合研磨,能闻到刺激性气味
D. 打开盛有浓盐酸的瓶盖,瓶口出现白烟
难度: 简单查看答案及解析
-
在配制100 g质量分数为10%的氢氧化钠溶液的过程中,下列操作正确的是( )
A. 用量筒量取90 mL水时俯视读数
B. 氢氧化钠易潮解,应放在玻璃器皿中称量
C. 用蒸馏水洗涤烧杯后,立即溶解氢氧化钠
D. 实验过程中,用到的玻璃仪器只有烧杯和量筒
难度: 简单查看答案及解析