-
下列谚语或俗语中包含化学变化的是
A. 只要功夫深,铁杵磨成针 B. 冰冻三尺非一日之寒
C. 墙内开花墙外香 D. 生米已成熟饭
难度: 简单查看答案及解析
-
对物质进行分类,有利于我们的学习。下列物质的分类正确的是
选项
酸
碱
盐
非电解质
A
H2SO4
NaOH
NaHCO3
BaSO4
B
HCl
C2H5OH
NaCl
CO2
C
HNO3
Ba(OH)2
BaCO3
CH4
D
CH3COOH
KOH
Na2S
Cl2
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
下列反应中,既不属于四种基本反应类型,也不属于氧化还原反应的是
A. C(石墨) ═ C(金刚石) B. CuSO4 + 2NaOH ═ Cu(OH)2↓ + Na2SO4
C. Cl2 + 2KBr ═ Br2 + 2KCl D. 3CO + Fe2O3
2 Fe + 3CO2
难度: 简单查看答案及解析
-
有关化学史的,下列说法中不正确的是
A. 道尔顿——提出原子学说 B. 爱迪生——发现电子
C. 卢瑟福——提出带核的结构模型 D. 玻尔——提出了电子在核外的量子化轨道
难度: 简单查看答案及解析
-
李时珍在《本草纲目》中写到:“烧酒非古法也,自元时始创其法。用浓酒和糟入甑,蒸令气上,用器承取滴露。” “凡酸坏之酒,皆可蒸烧”,“以烧酒复烧二次,……,价值数倍也”,这里用到的方法可用于分离
A. 硝酸钾和氯化钾 B. 四氯化碳和水
C. 甲醇(沸点64.7℃)和丁醇(沸点117.6℃) D. 碘化钾和碘
难度: 简单查看答案及解析
-
中国科学技术大学的钱逸泰教授等以四氯化碳和金属钠为原料,在700 ℃时制造出纳米级金刚石粉末。该成果发表在世界权威的《科学》杂志上,立刻被科学家们高度评价为“稻草变黄金”。同学们对此有下列一些理解,其中正确的是
A. 该反应是氧化还原反应
B. 制造过程中原子的种类和数目发生了改变
C. 生成的纳米级金刚石是一种新型的化合物
D. 生成的纳米级金刚石粉末能产生丁达尔效应
难度: 简单查看答案及解析
-
实验室需配置离子浓度均为0.1mol/L的某混合溶液,下列选项中能达到实验目的的是
A. K+、Na+、NO3-、Cl- B. K+、Ba2+、Cl-、OH-
C. Ag+、K+、Cl-、NO3- D. Na+、NH4+、SO42-、NO3-
难度: 简单查看答案及解析
-
下列各组物质的转化,一定要加入氧化剂才能完成的是
A. Cl2 → NaCl B. H2O2 → O2
C. Fe → FeCl3 D. K2CO3 → KOH
难度: 简单查看答案及解析
-
稀有金属铟由于其良好的性能常用于生产液晶显示器和平板屏幕,下图是铟元素的相关信息,下列有关铟的说法错误的是

A. 115In原子核内有66个中子
B. 115In原子核外有49个电子
C. 115In、113In互为同位素
D. 115In、113In的化学性质有较大的不同
难度: 简单查看答案及解析
-
NA为阿伏加德罗常数的值,下列说法正确的是
A. 标准状况下,3.6 g D2O含有的电子数为2NA
B. 常温常压下,3.2gO2和O3 的气体混合物中含氧原子数目为0.2NA
C. 2L 0.5mol/L的KClO3溶液中含有Cl-的物质的量为NA
D. 标准状况下,11.2L四氯化碳所含的分子数为0.5NA
难度: 简单查看答案及解析
-
下列生活中常见的物质中,不能产生丁达尔效应的是
A. 牛奶 B. 白糖水 C. 豆浆 D. 鸡蛋清溶液
难度: 简单查看答案及解析
-
下列物质在水溶液中的电离方程式,书写正确的是
A. BaSO4
Ba2+ + SO42 - B. NaHCO3 == Na++ H+ + CO32 -
C. NaHSO4 == Na++ HSO4- D. KNO3 =K+ + NO3-
难度: 简单查看答案及解析
-
等温等压下,等质量的C2H4和C3H6气体,下列叙述正确的是
A. 密度相等 B. 体积相等 C. 原子数相等 D. 分子数相等
难度: 简单查看答案及解析
-
下列实验操作正确的是

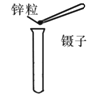

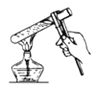
A.蒸馏
B.块状固体得取用
C.过滤
D.用试管给液体加热
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
下列是对某溶液进行离子检测的方法和结论,其中正确的是
A. 用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定不含钾离子
B. 加入足量的BaCl2溶液,产生白色沉淀,再加入足量的稀盐酸,沉淀不溶解,则溶液中一定含有大量的SO42 -
C. 加入盐酸,能产生使澄清石灰水变浑浊的无色无味气体,则溶液中一定含有CO32 -
D. 加入NaOH溶液后加热产生能使湿润的红色石蕊试纸变蓝的气体,则溶液中一定含有NH4+
难度: 简单查看答案及解析
-
实验室要配制450mL浓度为1mol/L 的Na2CO3溶液,下列操作正确的是
A. 称取47.7g的Na2CO3固体溶于水,配成500mL溶液
B. 称取143.0g的Na2CO3﹒10H2O固体溶于水,配成500mL溶液
C. 称取53.0g的Na2CO3固体溶于500mL水中
D. 称取53.0g的Na2CO3固体置于500mL容量瓶,加水至刻度线
难度: 简单查看答案及解析
-
元素R的质量数为A,Rn-的核外电子数为x,则w g Rn-所含中子的物质的量为
A. (A-x+n)mol B. (A-x-n)mol C. (A-x+n)w/Amol D. (A-x-n)w/Amol
难度: 困难查看答案及解析
-
下列溶液中NO3 - 物质的量与50mL 1mol/L Al(NO3)3溶液的NO3 - 物质的量不相等的是
A. 100mL 2.0mol·L-1 AgNO3溶液 B. 75 mL 1.0 mol·L-1 Mg(NO3)2溶液
C. 100 mL 0.5 mol·L-1 Fe(NO3)3溶液 D. 75 mL 2.0 mol·L-1 Na NO3溶液
难度: 简单查看答案及解析
-
把V L含有MgCl2和KCl的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含有b molAgNO3的溶液,恰好使氯离子完全沉淀。则原混合溶液中钾离子浓度为
A. 2(b-a)/Vmol·L-1 B. (2b-a)/Vmol·L-1
C. (b-a)/Vmol·L-1 D. 2(2b-a)/Vmol·L-1
难度: 中等查看答案及解析
-
X、Y、Z、W均为原子序数小于18的四种元素的原子,已知X核外电子总数等于电子层数,Y最外层电子数是次外层电子数的两倍,Z2是空气的主要成分之一,是最常见的助燃剂,W+与氖原子核外电子排布相同,下列说法不正确的是
A. Z2-与W+具有相同的核外电子排布
B. YZ2的水溶液能导电,所以化合物YZ2属于电解质
C. 化合物WZX的水溶液能使湿润的红色石蕊试纸变蓝
D. 元素X、Z之间可以形成X2Z和X2Z2两种化合物
难度: 中等查看答案及解析
-
室温下,在两个体积相同密闭容器中,分别充等质量的甲、乙两种气体,若测得含甲气体的容器中气体压强大于含乙气体的容器中气体压强,则下列说法正确的是
A. 在上述情况中甲气体密度比乙气体密度大
B. 甲的摩尔质量比乙的摩尔质量小
C. 甲的物质的量比乙的物质的量少
D. 甲所含原子数比乙所含原子数少
难度: 简单查看答案及解析
-
某溶液中含有较大量的Cl-、CO32-、OH- 3种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来,下列实验操作顺序中,正确的是
①滴加Ba(NO3)2溶液; ②过滤; ③滴加Mg(NO3)2溶液; ④滴加AgNO3溶液
A. ①②④②③ B. ④②①②③
C. ①②③②④ D. ④②③②①
难度: 中等查看答案及解析