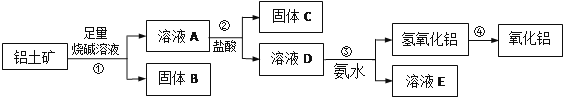
-
下列现象或应用不能用胶体的知识解释的是( )
A. 清晨,人们经常看到阳光穿过茂密的树木枝叶所产生的美丽景象
B. 土壤表面积巨大且一般带负电,能吸收NH4+等营养离子,使土壤具有保肥能力
C. 向FeCl3溶液中加入NaOH溶液,会出现红褐色沉淀
D. 水泥、冶金工厂常用高压电除去工厂烟尘,减少对空气的污染
难度: 中等查看答案及解析
-
下列实验操作中错误的是( )
A. 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出
B. 称量NaOH时,称量物放在称量纸上,置于托盘天平的左盘中
C. 过滤时,漏斗下端紧贴烧杯内壁
D. 蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口处
难度: 简单查看答案及解析
-
下列叙述错误的是( )
A. 节假日燃放的五彩缤纷的烟花是和一些金属元素的焰色反应有关
B. 硅胶常作实验室和袋装食品等的干燥剂
C. 84消毒液的有效成分为次氯酸钠
D. SiO2是光导纤维的原料,是一种酸性氧化物,不能与任何酸反应
难度: 简单查看答案及解析
-
下列说法正确的是( )
A. 向饱和FeCl3溶液中逐滴滴加NaOH溶液即可以制备Fe(OH)3胶体
B. 明矾溶于水可产生具有吸附性的胶体粒子,常用于饮用水的杀菌消毒
C. 多数合金比成分金属熔点低、硬度大
D. 非金属氧化物一定属于酸性氧化物
难度: 简单查看答案及解析
-
下列物质的分类合理的是( )
A. 酸性氧化物:CO2、SiO2、SO2、CO
B. 碱:烧碱、纯碱、苛性钾、氢氧化钡
C. 混合物:盐酸、漂白粉、水煤气、氢氧化铁胶体
D. 碱性氧化物:Na2O、CaO、MgO、Na2O2
难度: 简单查看答案及解析
-
下列物质中既能跟盐酸反应,又能跟氢氧化钠溶液反应的化合物是( )
①Al ②Al2O3 ③Al(OH)3 ④AlCl3 ⑤NaHCO3.
A. ① ③④ B. ②③⑤ C. ②③④ D. 全部
难度: 简单查看答案及解析
-
下列有关实验操作不能达到相应目的的是( )
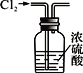
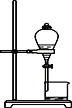
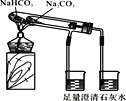
A.干燥Cl2
B.分离汽油与食盐溶液
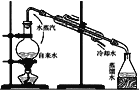
C.实验室制取少量蒸馏水
D.比较Na2CO3与NaHCO3的稳定性
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
A. 在25℃、101kPa下,11.2 L CO2气体中含有的碳原子数目为0.5NA
B. 1mol氯气与足量Fe粉完全反应,失去的电子数为3NA
C. 常温常压下,78g Na2O2与足量水反应生成O2分子数为0.5NA
D. 2 mol·L-1H2SO4溶液中含有的H+数目为4NA
难度: 简单查看答案及解析
-
下列溶液中,溶质的物质的量浓度为1mol·L-1的是( )
A. 将40gNaOH溶解于1L水中配成的NaOH溶液
B. 将80gSO3溶于水并配成1L的溶液
C. 将0.5 mol·L-1的NaNO3溶液100mL加热蒸发掉50g水后的溶液
D. 1L含K+为1mol的K2SO4溶液
难度: 简单查看答案及解析
-
下列反应的离子方程式不正确的是( )
A. FeCl3溶液与Cu的反应:Cu+Fe3+=Cu2++Fe2+
B. 碳酸钠与足量的盐酸反应:CO32-+2H+=H2O+CO2↑
C. 少量金属钠加到冷水中:2Na+2H2O=2Na++2OH-+H2↑
D. 氢氧化铜加到盐酸中:Cu(OH)2+2H+=Cu2++2H2O
难度: 简单查看答案及解析
-
下列反应既是离子反应,又是氧化还原反应的是( )
A. BaCl2溶液中滴加稀硫酸 B. 盐酸和氧化铁反应
C. 铁片放入CuSO4溶液中 D. 氢气还原CuO
难度: 简单查看答案及解析
-
通入足量氯水后能大量共存的一组离子是( )
A. Na+、SO42-、Al3+、NO3- B. Na+、K+、HCO3-、OH-
C. Na+、Ca2+、NO3-、CO32- D. K+、Fe2+、NO3-、Cl-
难度: 简单查看答案及解析
-
已知5KCl+ KClO3 + 3H2SO4 = 3Cl2↑+ 3K2SO4 + 3H2O,下列说法不正确的是 ( )
A. KClO3是氧化剂
B. 标准状况下产生33.6L Cl2时有3mol电子转移
C. H2SO4既不是氧化剂也不是还原剂
D. 被氧化与被还原的氯元素的质量比为5︰1
难度: 简单查看答案及解析
-
下列有关钠及钠的化合物的叙述中,正确的是( )
A. Na2O2可用于呼吸面具中氧气的来源
B. 钠在空气中燃烧发出黄色的火焰,生成Na2O
C. 钠与CuSO4溶液反应置换出Cu
D. 用铂丝蘸取硫酸钠溶液在酒精灯上灼烧时火焰呈紫色
难度: 简单查看答案及解析
-
下列各项操作中,不发生“先产生沉淀,然后沉淀又溶解”现象的是( )
①向饱和碳酸钠溶液中通入过量的CO2;②向NaAlO2溶液中逐滴加入过量的稀盐酸;③向Fe(OH)3胶体中逐滴加入稀硫酸至过量;④向AlCl3溶液中通入NH3气体至过量
A. ①② B. ①③ C. ①④ D. ②③
难度: 简单查看答案及解析
-
图用分类法表示了一些物质或概念之间的从属或包含关系,不正确的是( )

X
Y
Z
A
NaAlO2
盐
纯净物
B
胶体
分散系
混合物
C
Al2O3
两性氧化物
氧化物
D
单质参与反应
置换反应
氧化还原反应
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
烧杯中盛有含 Cu2+、Al3+、Fe3+、SO42-、Fe2+、Cl-六种离子的溶液,若向其中加入足量的 Na2O2 搅拌,充分反应后再向该烧杯中滴加足量的稀盐酸,此时上述离子物质的量保持不变的有( )
A. 1 种 B. 2 种 C. 3种 D. 4 种
难度: 简单查看答案及解析
-
下列除杂(括号内为杂质)所选用的试剂及操作方法均正确的一组是( )
待提纯的物质
选用的试剂
操作方法
A
NaOH (Na2CO3)
盐酸
——
B
CO2 (HCl)
Na2CO3溶液
洗气
C
FeCl3 (FeCl2)
铁粉
过滤
D
Mg (Al)
NaOH溶液
过滤
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
下列说法不正确的是( )
A. 无论新制还是久置的氯水,滴加AgNO3溶液均生成白色沉淀
B. 氯水呈黄绿色,说明氯水中含有 Cl2
C. 向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有H+
D. 向新制氯水中滴加少量紫色石蕊试液,充分振荡后溶液呈红色
难度: 简单查看答案及解析
-
下列相关实验的叙述中,正确的是( )

A. HClO、活性炭均能使某些有色物质褪色,说明二者均有氧化性
B. 加热分别盛有NaHCO3和碘的两支试管,试管底部固体均减少,说明二者均发生升华
C. 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热,熔化后的液态铝滴落下来
D. 用上图装置观察 Fe(OH)2 的生成
难度: 简单查看答案及解析
-
只用一种试剂,就能将氯化钠、氯化铝、氯化亚铁、氯化铁、氯化镁五种溶液通过一步实验加以区别,这种试剂是( )
A. KSCN B. BaCl2 C. NaOH D. HCl
难度: 简单查看答案及解析
-
下列物质:①Na,②Cl2,③Na2O2分别与水反应,氧化剂与还原剂的物质的量之比为1:1的是
A. ①③ B. ②③ C. ①② D. ①②③
难度: 简单查看答案及解析
-
下列物质之间的转化都一步能实现的是( )
A. Si→SiO2→H2SiO3→Na2SiO3
B. Al→Al2O3→Al(OH)3→NaAlO2
C. Na→Na2O→Na2O2→NaOH→Na2CO3→NaHCO3
D. Fe→Fe2O3→Fe(OH)3→FeCl3
难度: 简单查看答案及解析
-
关于下列实验装置或操作的说法中,正确的是( )
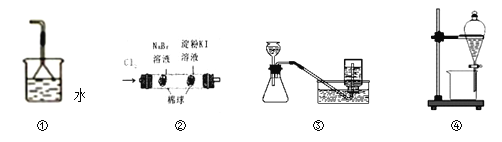
A. ③选择合适的试剂,可分别制取并收集少量H2和Cl2
B. ②实验中若左边棉花变橙红色,右边棉花变蓝色,则能证明氧化性:Cl2>Br2>I2
C. ①实验用来吸收氯化氢气体并防止倒吸
D. 用图④操作可用乙醇提取碘水中的碘
难度: 简单查看答案及解析
-
下列关于Na2CO3和NaHCO3的叙述中正确的是( )
A. 常温下,Na2CO3比NaHCO3的溶解度小
B. 质量相同的Na2CO3和NaHCO3与足量盐酸反应可生成等量的CO2
C. 石灰水可鉴别Na2CO3和NaHCO3溶液
D. 相同条件下Na2CO3和NaHCO3分别与盐酸反应,后者放出气体快
难度: 简单查看答案及解析
-
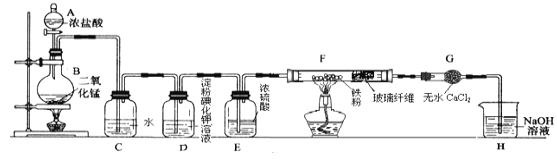
某化学兴趣小组利用KMnO4和浓HCl及如图装置制备Cl2。下列分析中不正确的是( )

A. A中可用分液漏斗代替长颈漏斗
B. B中盛放的NaOH溶液可以净化Cl2
C. C为向上空气法收集氯气
D. D中盛放的NaOH溶液可以吸收尾气
难度: 简单查看答案及解析
-
某溶液中含有Cl-、SO42—、Fe3+、K+、M,且离子的物质的量之比为2:3:1:3:1,则微粒M为( )
A. Na+ B. S2- C. Mg2+ D. Al3+
难度: 简单查看答案及解析
-
已知还原性:SO2>I->Fe2+,下列离子反应不能发生的是( )
A. SO2 + 2Fe3+ + 2H2O = 2Fe2+ + SO42- + 4H+
B. I2 + 2Fe2+ = 2I- + 2Fe3+
C. SO2 + Cl2 + 2H2O= 2Cl- + SO42- + 4H+
D. 少量Cl2通入FeI2溶液中:Cl2 + 2I- =I2+2Cl—
难度: 简单查看答案及解析
-
下列实验与对应示意图的关系正确的是( )
A
B
C
D
向NaAlO2溶液中逐滴滴加盐酸至过量
向AlCl3溶液中逐滴滴加氨水至过量
向明矾溶液中逐滴滴加
Ba(OH)2溶液至过量
向澄清石灰水中缓缓通入CO2至过量




A. A B. B C. C D. D
难度: 中等查看答案及解析
-
硫代硫酸钠(Na2S2O3)可作为还原剂,已知25.0mL0.01mol/LNa2S2O3溶液恰好把22.4mL(标准状况下)Cl2完全转化为Cl-离子,则S2O32-将转化成( )
A. S2- B. S C. SO42- D. SO32-
难度: 简单查看答案及解析