-
下列化工生产过程中,未涉及氧化还原反应的是( )
A. 海带提碘 B. 氯碱工业
C. 氨碱法制碱 D. 海水提溴
难度: 中等查看答案及解析
-
、下列离子方程式书写正确的是( )
A. 向氢氧化钠溶液中通入足量二氧化碳:OH﹣+CO2===HCO3-
B. 氧化钠投入水中发生反应:O2﹣+H2O===2OH﹣
C. 硝酸银溶液中加入铜粉:Ag++Cu===Cu2++Ag
D. 金属铁溶于稀硫酸中:2Fe+6H+===2Fe3++3H2↑
难度: 中等查看答案及解析
-
下列关于物质分类的正确组合是
碱
酸
盐
碱性氧化物
酸性氧化物
A
氨气
硫酸
小苏打
氧化钙
干冰
B
烧碱
盐酸
食盐
氧化钠
一氧化碳
C
石灰水
冰醋酸(CH3COOH)
胆矾CuSO4·5H2O
过氧化钠
二氧化硫
D
NH3·H2O
HNO3
碳酸钙
氧化铁
SO3
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
用NA表示阿伏加德罗常数的值,下列关于0.2mol/LK2SO4溶液说法正确的是
A. 1L溶液中K+浓度是0.4mol/L B. 500mL溶液中含有0.1NA个K+
C. 1L溶液中所含K+、SO42-总数为0.3NA D. 2L溶液中SO42-浓度是0.4mol/L
难度: 中等查看答案及解析
-
有五瓶失去标签的溶液,它们分别为:
①Ba(NO3)2 ②KCl ③NaOH ④CuSO4 ⑤Na2SO4如果不用其他任何试剂(包括试纸),用最简便的方法将它们一一鉴别开来,则在下列的鉴别顺序中,最合理的是( )
A. ④③①⑤② B. ④②①③⑤ C. ①⑤③④② D. ③④①⑤②
难度: 中等查看答案及解析
-
下列叙述正确的是( )
A. 1 mol H2O的质量为18g/mol
B. CH4的摩尔质量为16g
C. 3.01×1023个SO2分子的质量为32g
D. 标准状况下,1 mol任何物质体积均为22.4L
难度: 中等查看答案及解析
-
实验测得某溶液中仅含有K+、Cu2+、SO42-、Cl-四种离子,其中K+、Cu2+、Cl-三种离子的个数比为4:5:8,则K+与SO42-的物质的量比为( )
A. 4:3 B. 4:1 C. 2:3 D. 2:1
难度: 中等查看答案及解析
-
配制250mL 0.10mol/L的盐酸溶液时,下列实验操作会使配制的溶液浓度偏高的是
A. 容量瓶内有水,未经过干燥处理
B. 定容时,仰视刻度线
C. 用量筒量取浓盐酸时,用水洗涤量筒2~3次,洗涤液倒入烧杯中
D. 定容后倒转容量瓶几次, 发现液体最低点低于刻度线,再补加几滴水到刻度线
难度: 中等查看答案及解析
-
Rn+离子有m个电子,它的质量数为A,则原子核内的中子数为
A. m+n B. A-m+n C. A-m-n D. A+m-n
难度: 简单查看答案及解析
-
等温等压下,关于等质量H2、D2、T2三种气体的下列叙述中不正确的是 ( )
A. 密度之比1:2:3 B. 质子数之比6:3:2 C. 中子数之比0:3:4 D. 体积之比1:2:3
难度: 简单查看答案及解析
-
下列有关物质分离的叙述,不正确的是
A. 用过滤的方法分离溶液和胶体 B. 用蒸馏的方法将自来水制成蒸馏水
C. 用四氯化碳萃取碘水中的碘 D. 用加热的方法分离氯化钠和碘单质
难度: 简单查看答案及解析
-
下列对于某些离子的检验及结论一定正确的是( )
A. 加入稀盐酸产生无色气体,原物质一定有CO32-
B. 加入氯化钡溶液有白色沉淀产生,一定有SO42-
C. 加入硝酸银溶液产生白色沉淀,则原溶液一定有Cl-
D. 加入碳酸钠溶液产生白色沉淀,再加盐酸,白色沉淀消失,不一定有Ba2+
难度: 中等查看答案及解析
-
ClO2是一种消毒杀菌效率高、二次污染小的水处理剂.实验室可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4
2ClO2↑+K2SO4+2CO2↑+2H2O.下列说法中正确的是( )
A. KClO3在反应中是还原剂
B. 1 mol KClO3参加反应,在标准状况下能得到22.4 L气体
C. 在反应中H2C2O4既不是氧化剂也不是还原剂
D. 1 mol KClO3参加反应有1 mol电子转移
难度: 中等查看答案及解析
-
既能跟盐酸反应,又能跟氢氧化钠溶液反应的盐是
A.Na2CO3 B. NaHCO3 C.MgO D.Al(OH)3
难度: 简单查看答案及解析
-
下列各组离子中,能在溶液中大量共存的是( )。
A. Na+、Cl-、Al3+、SO42- B. Cu2+、NO3-、Cl- OH-
C. K+、Ca2+、NO3-、CO32- D. H+、SO42- 、NO3-、OH-
难度: 简单查看答案及解析
-
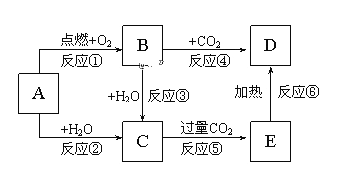
已知A是一种金属单质,B显淡黄色,其转化关系如下图所示,则关于C的以下性质叙述错误的是
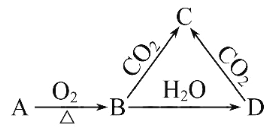
A. 溶液呈碱性
B. 与澄清石灰水反应产生白色沉淀
C. 与足量盐酸反应放出气体
D. 受热易分解
难度: 简单查看答案及解析
-
下列书写电离方程式,正确的是( )
A. Na2SO4====Na2++SO42- B. NaOH
Na++OH-
C. NaHCO3=Na++H++CO32- D. NH3·H2O
NH4++OH-
难度: 简单查看答案及解析
-
等物质的量的Na2O2与NaHCO3混合后,在密闭容器中充分加热,排出气体物质后冷却,残留的固体物质是
A. Na2O2、Na2CO3 B. Na2CO3 C. NaOH、Na2CO3 D. Na2O2、NaOH、Na2CO3
难度: 中等查看答案及解析
-
下列说法错误的是
A. 胶体具有丁达尔现象
B. 热稳定性:Na2CO3>NaHCO3
C. 表示Na2CO3和NaHCO3分别与Ba(OH)2溶液反应的离子方程式相同
D. 等质量的Na2CO3和NaHCO3分别与等浓度的HCl溶液完全反应,后者消耗的盐酸少
难度: 简单查看答案及解析
-
下列气体不能用碱石灰(氢氧化钠固体和生石灰的混合物)干燥的是( )
A. H2 B. Cl2 C. NH3 D. CO
难度: 简单查看答案及解析
-
已知2A-+B2===A2+2B-,2A-+C2===A2+2C-,2B-+C2===B2+2C-,2C-+D2=== C2+2D-。则各种单质氧化性由强到弱的顺序是( )
A. A2>C2>B2>D2 B. B2>C2>A2>D2
C. D2>C2>B2>A2 D. C2>B2>A2>D2
难度: 中等查看答案及解析
-
一定条件下,PbO2与Cr3+反应,产物是Cr2O72-和Pb2+,则与1 mol Cr3+反应所需PbO2的物质的量为
A. 3.0 mol B. 1.5 mol C. 1.0 mol D. 0.75 mol
难度: 中等查看答案及解析