-
下列反应与Na2O2+SO2→Na2SO4相比较,Na2O2的作用相同的是
A. 2Na2O2+2CO2→2Na2CO3+O2 B. 2Na2O2+2SO3→2Na2SO4+O2
C. 2Na2O2+H2SO4→Na2SO4+H2O2 D. 3Na2O2+Cr2O3→2Na2CrO4+Na2O
难度: 简单查看答案及解析
-
在常温下发生下列反应: (1)16H+ +10Z-+ 2XO-4 ===2X2++ 5Z2+ 8H2O (2) 2A2十+B2==2A3++ 2B- (3) 2B- +Z2==B2+2Z- 根据上述反应,判断下列结论中错误的是( )
A. 溶液中可能发生:Z2+2A2+==2A3++2Z- B. Z2在①、③反应中均为氧化剂
C. 氧化性强弱顺序为:XO-4>Z2>B2>A3+ D. X2+是XO-4的还原产物
难度: 中等查看答案及解析
-
把V L含有MgS04和K2S04的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为
A.mol·L-1 B. mol·L-1
C. mol·L-1 D. mol·L-1
难度: 简单查看答案及解析
-
完全沉淀等物质的量浓度的NaCl、MgCl2、AlCl3溶液中的Cl﹣,消耗等物质的量浓度的AgNO3溶液的体积比为1∶1∶1,则上述溶液的体积比为
A. 1∶1∶1 B. 6∶3∶2 C. 3∶2∶1 D. 9∶3∶1
难度: 简单查看答案及解析
-
2.3 g纯净的金属钠在干燥的空气中,被氧化后得到3.5 g固体,由此可判断出产物是
A. 氧化钠 B. 过氧化钠
C. 氧化钠和过氧化钠的混合物 D. 无法确定
难度: 中等查看答案及解析
-
下列实验操作中,不是从人身安全因素考虑的是( )
A. 酒精灯不使用时,必须盖上灯帽
B. 给试管里的固体加热时,试管口应略向下倾斜,外壁干燥后再加热
C. 给试管里的液体加热时,试管口略向上倾斜(约45°),外壁干燥后再加热
D. 用H2还原CuO时,应先通一会儿H2,再加热CuO
难度: 简单查看答案及解析
-
某氯化镁溶液的密度为1.18g/cm3,其中镁离子的质量分数为5.1%,300mL该溶液中Cl-离子的物质的量约等于( )
A. 0.37mol B. 0.63mol C. 0.74mol D. 1.5mol
难度: 中等查看答案及解析
-
下列选项中,与物质体积大小无关的因素是
A. 粒子数目 B. 粒子大小
C. 粒子之间的距离 D. 粒子的化学性质
难度: 中等查看答案及解析
-
某混合物的水溶液,只可能含有以下离子中的若干:NH4+、Cl﹣、Mg2+、Ba2+、K+、CO32-、SO42-,现取三份100mL溶液进行如下实验:
①第一份加入AgNO3溶液有沉淀产生;
②第二份加足量NaOH溶液加热后,收集到气体0.04mol;
③第三份加足量BaCl2溶液后,得干燥沉淀6.27 g,经足量盐酸洗涤、干燥,沉淀质量2.33g。
根据上述实验,以下推测正确的是( )
A. K+一定不存在 B. 该溶液中含CO32-的浓度为0.1 mol·L-1
C. Cl﹣可能存在 D. Ba2+一定不存在,Mg2+可能存在
难度: 中等查看答案及解析
-
氢氧化铁胶体稳定存在的主要原因是
A. 胶粒直径小于1 nm B. 胶粒不停地作无规则运动
C. 胶粒带正电荷 D. 胶粒不能通过半透膜
难度: 简单查看答案及解析
-
金属及其化合物转化关系是化学学习的重要内容之一。下列各组物质的转化关系中不全部是通过一步反应完成的是( )
A. Na→NaOH→Na2CO3→NaCl B. Al→Al2O3→Al(OH)3→AlCl3
C. Mg→MgCl2→Mg(OH)2→MgSO4 D. Fe→FeCl2→Fe(OH)2→Fe(OH)3
难度: 中等查看答案及解析
-
物质在反应中可表现氧化性、还原性、酸性、碱性等,下面方程式中划线的物质,能在同一反应中同时表现上述两种或两种以上性质的有( )
①Cu+2H2SO4(浓)===CuSO4+SO2↑+2H2O
②C+2 H2SO4(浓)===CO2↑+2SO2↑+2H2O
③8NH3+3Cl2===6NH4Cl+N2
④3NO2+H2O===2HNO3+NO
A. ①② B. ①④ C. ③④ D. 全部
难度: 中等查看答案及解析
-
下列物质中可以随身携带乘车、船或飞机的是
A. 硫黄 B. 氯酸钾 C. 硝酸钾 D. 碘盐
难度: 简单查看答案及解析
-
已知:2Fe2++Cl2=2Cl﹣+2Fe3+,2Br﹣+Cl2=Br2+2Cl﹣,2Fe2++Br2=2Br﹣+2Fe3+。在bL FeBr2溶液中通入amol Cl2时,使溶液中50% 的Br﹣氧化为Br2,则原FeBr2的物质的量浓度为
A. a/bmol•L﹣1 B. 2a/bmol•L﹣1 C. 3a/bmol•L﹣1 D. 5a/bmol•L﹣1
难度: 中等查看答案及解析
-
下列叙述中不正确的是
A. 加热蒸发饱和食盐水有氯化钠析出
B. 硫酸溶液加热蒸发时,硫酸的浓度增大
C. 加热蒸发硫酸钠溶液不一定有晶体析出
D. 加热蒸发饱和硫酸铜溶液析出无水硫酸铜
难度: 简单查看答案及解析
-
120 mL浓度为1 mol·L-1的Na2SO3溶液,恰好与100 mL浓度为0.4 mol·L-1的K2Cr2O7溶液完全反应,在还原产物中Cr元素的化合价
A. +3 B. +1 C. +4 D. +2
难度: 中等查看答案及解析
-
下列说法正确的是
A. 阳离子只有氧化性,阴离子只有还原性
B. 失电子难的原子获得电子的能力一定强
C. 得到电子越多的氧化剂,其氧化性就越强
D. 要实现Fe2+→Fe3+的转化,必须加入氧化剂
难度: 简单查看答案及解析
-
下列物质中导电性能最差的是
A. 石墨棒 B. 固体氧化钾
C. 盐酸 D. 熔融氢氧化钠
难度: 中等查看答案及解析
-
下列化学反应的离子方程式正确的是
A. 钠和冷水反应:Na+2H2O=Na++2OH﹣+H2↑
B. 用小苏打治疗胃酸过多:
+H+=CO2↑+H2O
C. 氯化铝溶液中加入过量氨水:Al3++3OH﹣=Al(OH)3↓
D. 三氯化铁溶液中加入铁粉:Fe3++Fe=2Fe2+
难度: 简单查看答案及解析
-
下列有关胶体的说法正确的是
A. 胶体是纯净物
B. 胶体与溶液的本质区别是有丁达尔效应
C. 将饱和氯化铁溶液滴入稀氢氧化钠溶液中加热,可得氢氧化铁胶体
D. 胶体属于介稳体系
难度: 简单查看答案及解析
-
下列溶液中,氯离子浓度最大的是
A. 100 mL 1 mol·L-1的NaCl溶液
B. 150 mL 1 mol·L-1的MgCl2溶液
C. 200 mL 1 mol·L-1的HCl溶液
D. 10 mL 1 mol·L-1的AlCl3溶液
难度: 简单查看答案及解析
-
下列叙述中不正确的是
A. 质量是国际单位制(SI)的七个基本单位之一
B. 电流是国际单位制中安培(A)衡量的物理量
C. 物质的量是含有一定数目粒子集合体的物理量
D. 物质的量常用符号n表示,其单位是摩尔(mol)
难度: 简单查看答案及解析
-
常温常压下,用等质量的CH4、CO2、O2、SO2四种气体分别吹出四个气球,其中气体为CH4的是( )。
A.
B.
C.
D.
难度: 简单查看答案及解析
-
四种金属在稀盐酸中的反应现象分别如下图所示,其中为金属铜的是
A.
 B.
B.  C.
C.  D.
D. 
难度: 简单查看答案及解析
-
下列离子方程式正确的是
A. 澄清石灰水与过量碳酸氢钠溶液反应:
+Ca2++OH﹣=CaCO3↓+H2O
B. 硫酸氢钠溶液中加入氢氧化钡溶液至中性:H++
+Ba2++OH﹣=BaSO4↓+2H2O
C. 向氢氧化钠溶液中通入足量CO2:2OH﹣+CO2=
+H2O
D. 向氢氧化钡溶液中加入过量硫酸:2H++
+Ba2++2OH﹣=BaSO4↓+2H2O
难度: 中等查看答案及解析
-
分离下列混合物,按溶解、过滤、蒸发顺序进行的是
A. 碳酸钙、木炭 B. 氧化铜、硝酸钾
C. 乙醇、碘 D. 硝酸钾、氯化钠
难度: 简单查看答案及解析
-
镁、铝能够在空气中稳定存在的原因是
A. 性质不活泼,不与空气中的成分反应
B. 镁、铝与氧气的反应速率极慢
C. 经过了特殊工艺处理
D. 与氧气反应形成了氧化物保护膜
难度: 简单查看答案及解析
-
用足量的一氧化碳还原4.64 g某金属氧化物,把生成的二氧化碳全部通入到过量的澄清石灰水中,得到的沉淀干燥后质量为8.0 g,则此金属氧化物是下列中的( )
A. 氧化铜 B. 氧化铁 C. 四氧化三铁 D. 二氧化锰
难度: 中等查看答案及解析
-
下列各组溶液,当后一种溶液逐滴加入到一定量的前一种溶液中并稍过量,其溶液的导电性(I表示导电能力)与后一种溶液的质量(m)的函数关系符合下图的是
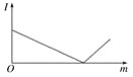
A. 澄清石灰水、碳酸钠溶液
B. 硝酸银溶液、氯化钠溶液
C. 盐酸、氢氧化钠溶液
D. 稀硫酸、氢氧化钡溶液
难度: 简单查看答案及解析