-
关于原子结构的叙述正确的是( )
A. 所有的原子核都是由质子和中子组成的 B. 原子的最外层电子数不超过8个
C. 稀有气体原子的最外层电子数均为8 D. 原子的次外层电子数都是8
难度: 中等查看答案及解析
-
下列说法中不正确的是( )
A. 氟化银可用于人工降雨 B. 从海水中获取食盐不需要化学变化
C. FeCl3溶液可用于制作印刷电路板 D. 绿矾可用来生产铁系列净水剂
难度: 中等查看答案及解析
-
下列说法不正确的是( )
A. 氯气可用于合成药物 B. 碳酸钠可用于治疗胃酸过多
C. 高压钠灯常用来广场照明 D. 镁合金密度小强度大可用于制飞机零部件
难度: 简单查看答案及解析
-
下列物质属于盐的是( )
A. Cu2(OH)2CO3 B. Na2O C. Mg(OH)2 D. CH3CH2OH
难度: 简单查看答案及解析
-
下列属于碱性氧化物的是( )
A. HCl B. CO2 C. CaO D. KOH
难度: 简单查看答案及解析
-
下图所示是分离混合物时常用的仪器,从左至右,可以进行的混合物分离操作分别是
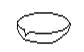
A. 蒸馏、蒸发、分液、过滤 B. 蒸馏、过滤、分液、蒸发
C. 分液、过滤、蒸馏、蒸发 D. 过滤、蒸发、分液、蒸馏
难度: 中等查看答案及解析
-
用NA表示阿伏德罗常数,下列叙述正确的是
A. 标准状况下,22.4LH2O含有的分子数为1 NA
B. 常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA
C. 通常状况下,1 NA 个CO2分子占有的体积为22.4L
D. 物质的量浓度为0.5mol·/L的MgCl2溶液中,含有Cl-个数为1 NA
难度: 简单查看答案及解析
-
下列反应属于四种基本反应类型,但不属于氧化还原反应的是( )
A. Fe+CuSO4═FeSO4+Cu B. CO+CuO
Cu+CO2
C. AgNO3+NaCl═AgCl↓+NaNO3 D. 2FeCl2+Cl2═2FeCl3
难度: 简单查看答案及解析
-
下列关于纯净物、混合物、电解质、非电解质的正确组合为( )
纯净物
混合物
电解质
非电解质
A
纯盐酸
水煤气
硫酸
干冰
B
蒸馏水
蔗糖溶液
氧化铝
二氧化硫
C
胆矾
盐酸
铁
碳酸钙
D
大理石
甲烷
氯化铜
碳酸钠
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
下列实验操作中错误的是( )
A. 蒸发操作时,当大部分固体析出时就停止加热,利用余热把剩下的水蒸干
B. 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C. 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D. 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
难度: 简单查看答案及解析
-
某阴离子X2﹣有m个电子,其质量数为a,则核内中子数为( )
A. m+2 B. m+5 C. a﹣m+2 D. a﹣m﹣2
难度: 中等查看答案及解析
-
下列溶液中的Cl-浓度与50mL 1mol•L﹣1MgCl2溶液中的Cl-浓度相等的是( )
A. 150 mL 1 mol•L﹣1 NaCl溶液 B. 75 mL 2 mol•L﹣1 CaCl2溶液
C. 150 mL 2 mol•L﹣1 KCl溶液 D. 75 mL 1 mol•L﹣1 AlCl3溶液
难度: 简单查看答案及解析
-
实验室保存下列物质的方法中,不正确的是
A. 少量金属钠保存在煤油里
B. 烧碱溶液盛装在用玻璃塞塞紧的试剂瓶中
C. FeSO4溶液存放在加有少量铁粉的试剂瓶中
D. 氯水应装在棕色瓶中密封避光保存
难度: 中等查看答案及解析
-
下列电离方程式中书写正确的是( )
A. NaHSO4
Na++H++SO42﹣ B. NaHCO3
Na++H++CO32﹣
C. HClO=H++ClO﹣ D. MgCl2═Mg2++2Cl﹣
难度: 简单查看答案及解析
-
下列各组离子能在溶液中大量共存的是( )
A. Na+、K+、Cl﹣、SO42﹣ B. Na+、H+、CO32﹣、Cl﹣
C. Na+、Ca2+、NO3﹣、CO32﹣ D. K+、H+、SO42﹣、OH﹣
难度: 简单查看答案及解析
-
检验下列物质的试剂、现象都正确的是( )
选项
被检验的物质
使用的试剂或方法
实验现象
A
Fe3+
KSCN溶液
溶液出现血红色沉淀
B
SO2
品红溶液
品红溶液褪色,加热不能复原
C
Na+
用铂丝蘸取少量溶液在火焰上灼烧
透过蓝色钴玻璃看到紫色火焰
D
NH4+
NaOH溶液、石蕊试纸
加入NaOH溶液后加热,产生的气体使湿润的红色石蕊试纸变蓝
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
下列说法正确的是( )
A. 常温下,浓硫酸可以用铁制槽罐存放,说明铁与浓硫酸不反应
B. 检验氯化氢中是否混有氯气,可采用湿润的有色布条
C. 镁在空气中燃烧只生成氧化镁
D. 钠可以从硫酸铜溶液中置换出金属铜
难度: 简单查看答案及解析
-
下列有关于Cl2的说法中,不正确的是( )
A. Cl2是一种黄绿色、密度比空气大的有毒气体
B. 红热的铁丝在Cl2中剧烈燃烧,产生白色烟雾
C. 工业上用Cl2和石灰乳为原料制造漂白粉
D. Cl2能与水反应生成盐酸和次氯酸
难度: 中等查看答案及解析
-
下列化学反应的离子方程式正确的是( )
A. 用小苏打治疗胃酸过多:HCO3﹣+H+=CO2↑+H2O
B. 往碳酸镁中滴加稀盐酸:CO32﹣+2H+=CO2↑+H2O
C. 往氨水中滴加氯化镁溶液:Mg2+2OH﹣=Mg(OH)2↓
D. 氢氧化钡溶液与稀硫酸反应:Ba2++SO42﹣+H++OH﹣=BaSO4↓+H2O
难度: 简单查看答案及解析
-
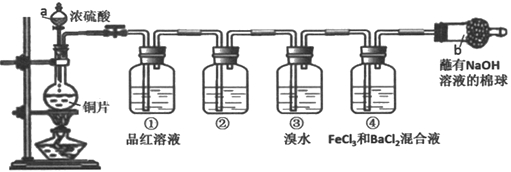
用图所示实验装置(夹持仪器己略去)探究铜丝与过量浓硫酸的反应.下列实验不合理的是( )
A. 上下移动①中铜丝可控制SO2的产生与停止
B. ②中选用品红溶液验证SO2的生成
C. ③中选用NaOH溶液吸收多余的SO2
D. 为确认有CuSO4生成,向①中加水,观察颜色
难度: 中等查看答案及解析
-
下列数字代表各元素的原子序数,则各组中相应的元素能形成XY2型离子化合物的是( )
A. 3和8 B. 1和16 C. 12和17 D. 6和16
难度: 简单查看答案及解析
-
下列有关物质性质的应用正确的是( )
A. 活泼金属与活泼非金属形成的都是离子键
B. 二氧化硅是制造太阳能电池板的主要材料
C. 二氧化硫通入酸性KMnO4溶液,溶液紫红色褪去,体现了SO2的漂白性
D. 化学反应的实质就是反应物中化学键断裂,生成物中形成新的化学键。
难度: 简单查看答案及解析
-
某物质灼烧时,焰色反应为黄色,下列判断正确的是( )
A. 该物质一定是钠的化合物 B. 该物质一定是金属钠
C. 该物质一定含钠元素 D. 该物质一定含钾元素
难度: 中等查看答案及解析
-
下列物质与其用途相符合的是( )
①N2﹣保护气 ②SiO2﹣光导纤维 ③AgI﹣人工降雨 ④碘﹣预防甲状腺肿大 ⑤MgO﹣耐高温材料 ⑥NaClO﹣消毒剂
A. ②③④⑤⑥ B. ①②③④⑤ C. ②③④⑤ D. 全部
难度: 简单查看答案及解析
-
某元素原子核外第二层是其他层电子数之和的2倍,则该元素的核电荷数为( )
A. 4 B. 8 C. 12 D. 16
难度: 简单查看答案及解析
-
X、Y、Z、W四种主族元素,若X的阳离子与Y的阴离子具有相同的电子层结构;W的阳离子的氧化性强于等电荷数的X阳离子的氧化性;Z的阴离子半径大于等电荷数的Y的阴离子半径,则四种元素的原子序数由大到小的顺序是( )
A. ZYXW B. WXYZ C. XYZW D. ZXYW
难度: 困难查看答案及解析
-
下列说法不正确的是( )
A. 铜呈紫红色.可与氯化铁溶液反应制作印刷电路板
B. 工业上用焦炭在高温下还原二氧化硅可直接得到高纯度的硅
C. 可用丁达尔效应区分胶体和溶液
D. 镁合金大量用于制造火箭、导弹和飞机的部件
难度: 简单查看答案及解析
-
短周期元素X、Y、Z在周期表中的位置如图所示,则下列说法中错误的是( )
X
Y
Z
A. X元素的最外层电子数为2 B. Y的气态氢化物的化学式为HY
C. Z的最高价氧化物的化学式为ZO2 D. X、Y、Z的单质中X单质最稳定
难度: 中等查看答案及解析
-
电子层数相同的三种元素X、Y、Z,已知其最高价氧化物对应水化物的酸性强弱为HXO4>H2YO4>H3ZO4.下列判断错误的是( )
A. 气态氢化物的稳定性:HX>H2Y>ZH3 B. 原子半径:X>Y>Z
C. 非金属性:X>Y>Z D. 单质氧化性:X>Y>Z
难度: 简单查看答案及解析