-
下列自然和生活中的事例不属于氧化还原反应的是( )
A. 动物呼吸 B. 植物光合作用 C. 金属生锈 D. 石膏点制豆腐
难度: 中等查看答案及解析
-
下列实验操作正确的是( )

A. 检验容量瓶是否漏水 B. 稀释浓硫酸 C. 蒸发 D. 过滤
难度: 简单查看答案及解析
-
下列反应中水起还原剂作用的是( )
A. CaO + H2O = Ca(OH)2 B. C+H2O(g)
CO+H2
C. 2F2 + 2H2O = 4HF + O2 D. 3NO2 + H2O = 2HNO3 + NO
难度: 简单查看答案及解析
-
符合图中阴影部分的物质是( )

A. K2SO3 B. Na2SO4 C. K2SO4 D. KCl
难度: 简单查看答案及解析
-
除去括号内杂质所用试剂和方法不正确的是( )
A. 植物油(水) —— 分液 B. Fe(OH)3胶体(HCl)—— 渗析
C. 水(NaCl) —— 蒸馏 D. CO2(HCl) —— 氢氧化钠溶液,洗气
难度: 简单查看答案及解析
-
下列电离方程式书写正确的是( )
A. CH3COONH4
CH3COO-+NH4+ B. HI = H++I-
C. H2S
2H++S2- D. NaHCO3 = Na++H++CO32-
难度: 简单查看答案及解析
-
下表中物质的分类组合完全正确的是 ( )
编号
A
B
C
D
强电解质
KNO3
H2SO4
BaSO4
HNO3
弱电解质
HF
CaCO3
HClO
NH3
非电解质
SO2
CCl4
H2O
C2H5OH
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
下列图标中警示腐蚀性物品的是( )

难度: 简单查看答案及解析
-
下列有关物质组成的说法正确的是( )
A. 物质均是由分子构成,分子均是由原子构成
B. 某物质经测定,只含有一种组成元素,则该物质一定是单质
C. 碱性氧化物均是金属氧化物,酸性氧化物可能是金属氧化物
D. 纯净的硫酸,纯净的盐酸均是纯净物
难度: 中等查看答案及解析
-
下列四类反应:①置换反应 ②复分解反应 ③只有一种元素化合价发生变化的反应 ④离子反应,其中一定不是氧化还原反应的是( )
A. 只有② B. 只有③ C. 只有②④ D. ①②③④
难度: 简单查看答案及解析
-
下列离子方程式书写正确的是( )
A. 铁跟稀硫酸反应:2Fe + 6H+ ═ 2Fe3+ + 3H2 ↑
B. 盐酸与澄清石灰水反应:H+ + OH-═ H2O
C. 碳酸钙与醋酸反应:CaCO3 +2H+ ═ Ca2+ + CO2↑ + H2O
D. 二氧化碳通入足量的氢氧化钠溶液:CO2 + OH-═ HCO3-
难度: 简单查看答案及解析
-
下列说法正确的是( )
A. 摩尔是国际单位制中的7 个基本物理量之一
B. 失去电子多的还原剂,还原性一定强
C. 根据是否有丁达尔效应将分散系分为溶液、胶体和浊液
D. “A氧化B”与“B被A氧化”,“A被B还原”表达的含义相同
难度: 简单查看答案及解析
-
在溶液中能大量共存,加入OH- 有沉淀产生,加入H+ 有气体放出的是( )
A. Na+、Cu2+、Cl-、SO42— B. Fe3+、K+、SO42-、NO3-
C. H+、Al3+、OH-、NO3- D. Na+、Ca2+、Cl-、HCO3-
难度: 困难查看答案及解析
-
配制一定物质的量浓度的NaOH溶液时,可造成所配溶液浓度偏高的是( )
A. 所用NaOH已吸潮 B. 摇匀后液面低于刻度线,不再补加水
C. 有少量NaOH溶液残留在烧杯内 D. 向容量瓶加水至时刻度线时俯视液面
难度: 简单查看答案及解析
-
将标准状况下
LHCl溶于1L水中,得到的盐酸密度为bg/cm3,则该盐酸的物质的量浓度是 ( )
A.
mo1/L B.
mo1/L
C.
mo1/L D.
mo1/L
难度: 中等查看答案及解析
-
设NA表示阿伏加德罗常数的数值,下列叙述中正确的是( )
A. 28g以任意比组成的CO与N2混合气体中含有原子数为2NA
B. 标准状况下,22.4L H2O含有的分子数为NA
C. 在H2O2 + Cl2 =2HCl + O2反应中,每生成32g氧气,则转移4NA个电子
D. 1L 1 mol/L 的盐酸中有NA 个HCl分子
难度: 简单查看答案及解析
-
已知98%的浓硫酸的物质的量浓度为18.4mol/L,则49%的硫酸的物质的量浓度 ( )
A. 等于9.2 mo1/L B. 小于 9.2 mo1/L
C. 大于 9.2 mo1/L D. 无法确定
难度: 简单查看答案及解析
-
镁、铝能够在空气中稳定存在的原因是( )
A. 性质不活泼,不与空气中的成分反应 B. 镁、铝与氧气的反应速率极慢
C. 经过了特殊工艺处理 D. 与氧气反应形成了氧化物保护膜
难度: 简单查看答案及解析
-
将钠、镁、铝0.3mol分别放入100 mL 1 mol/L的盐酸中,同温同压下产生的气体体积比是 ( )
A. 1:2:3 B. 6:3:2 C. 3:1:l D. 1:1:1
难度: 简单查看答案及解析
-
下列离子方程式正确的是( )
A. 石灰乳与过量碳酸氢钙溶液反应:HCO+Ca2++OH-===CaCO3↓+H2O
B. 向沸水中滴加饱和的FeCl3溶液制备Fe(OH)3胶体:
FeCl3+3H2O(沸水)
Fe(OH)3(胶体)+3HCl
C. 氢氧化铜与稀硫酸反应:H++OH-===H2O
D. 碳酸氢钠溶液中加入盐酸:CO32-+2H+===CO2↑+H2O
难度: 中等查看答案及解析
-
下列各项操作中,发生“先产生沉淀,然后沉淀又溶解”现象的是
①向石灰水中通入过量的CO2
②向Fe(OH)3胶体中逐滴加入过量的稀盐酸
③向Ba(OH)2溶液中逐滴加入过量的稀硫酸
④向AgCl胶体中逐滴加入过量的稀硝酸
A. ①② B. ①③ C. ①④ D. ②③
难度: 中等查看答案及解析
-
把0.05molNaOH固体分别加入到100mL下列液体中,溶液的导电能力变化最小的是( )
A. 自来水 B. 0.5 mol/L盐酸
C. 0.5 mol/L CH3COOH溶液 D. 0.5 mol/L KCl溶液
难度: 简单查看答案及解析
-
一定条件下硝酸铵受热分解的化学方程式为:5NH4NO3
2HNO3+4N2+9H2O,在反应中被氧化与被还原的氮原子数之比为 ( )
A. 5∶3 B. 5∶4 C. 1∶1 D. 3∶5
难度: 中等查看答案及解析
-
已知氧化性强弱顺序:Cl2> Br2> Fe3+>I2。下列反应不能发生的是( )
A. Br2+2I-= I2+2 Br- B. 2FeCl2+Cl2 = 2FeCl3
C. 2FeCl2+2HCl+I2 = 2FeCl3+2HI D. 2Fe3+ + 2I-= 2Fe2+ + I2
难度: 中等查看答案及解析
-
如果Fe3+、SO42-、Al3+和M四种离子以物质的量之比为2∶4∶1∶1共同存在于同一种溶液中,那么M可能是 ( )
A. Na+ B. PO43- C. CO32- D. Cl-
难度: 简单查看答案及解析
-
M2O7X-与S2- 在酸性溶液中发生如下反应:M2O7X-+3S2-+ZH+===YM3++3S↓+7H2O,则M2O7X-中M的化合价是( )
A. +4 B. +5 C. +6 D. +7
难度: 简单查看答案及解析
-
等体积、等物质的量浓度的盐酸、氢氧化钠溶液分别放在甲、乙两烧杯中,各加等质量的铝,生成氢气的体积比为5∶7,则甲、乙两烧杯中的反应情况可能分别是 ( )
A. 甲、乙中都是铝过量 B. 甲中铝过量,乙中碱过量
C. 甲中酸过量,乙中铝过量 D. 甲中酸过量,乙中碱过量
难度: 中等查看答案及解析
-
如图所示,室温下分别向密闭容器内可移动活塞的两边充入空气(已知空气体积占整个容器容积的1/4)、H2 和O2 的混合气体,若将H2、O2 的混合气体点燃引爆。活塞先左弹,恢复室温后,活塞右滑停留于容器的中央。则原来H2、O2 的物质的量之比可能为①4∶5 ② 2∶5 ③3∶8 ④7∶2
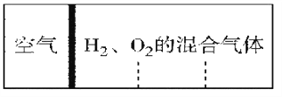
A. ①② B. ①④ C. ②③ D. ③④
难度: 困难查看答案及解析