-
采用不同的分类方法,可将非金属氧化物分为不同的类别。根据某种共性,可将CO2、P2O5、SO2、SO3、Cl2O7归为一类,下列物质中,完全符合此共性而能归为此类物质的是( )
A. CaO B. CO C. SiO2 D. H2O
难度: 简单查看答案及解析
-
反应3NO2+H2O
2HNO3+NO中,当有6 mol e-发生转移时,被氧化物质与被还原物质的物质的量之比为( )
A. 1∶1 B. 1∶2 C. 2∶1 D. 3∶1
难度: 简单查看答案及解析
-
在某未知溶液中加入硝酸银溶液,有白色沉淀生成,再加入稀硝酸,沉淀部分溶解,且有无色无味的气体生成,将气体通入澄清石灰水中,石灰水变浑浊,由此判断该未知溶液中含有( )
A. Cl-,SO42- B. Cl-,NO3-
C. Cl-,CO32- D. Cl-,OH-
难度: 简单查看答案及解析
-
下列变化没有发生电子转移的是( )
A. MnO4—-→MnO2 B. NO3—→NO2 C. Cl2→ClO3— D. SO2→SO32—
难度: 简单查看答案及解析
-
下列实验方案中,不能测定Na2CO3和NaHCO3混合物中Na2CO3质量分数的是
A. 取a克混合物充分加热,固体质量减轻b克
B. 取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体
C. 取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克
D. 取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体。
难度: 中等查看答案及解析
-
下列关于溶液和胶体的叙述,正确的是
A.溶液是电中性的,胶体是带电的
B.通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动
C.一束光线分别通过溶液和胶体时,后者会出现明显的光带,前者则没有
D.溶液中溶质粒子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动
难度: 简单查看答案及解析
-
下列说法不正确的是
A. 同温、同压下,相同质量的气体都占有相同的体积
B. 同温、同压下,相同体积的气体都含有相同数目的分子
C. 1 mol O2中含有1.204×1024个氧原子,在标准状况下占有体积22.4 L
D. 由0.2 g H2和8.8 g CO2、5.6 g CO组成混合气体,其密度是相同状况下O2密度的0.913倍
难度: 中等查看答案及解析
-
在标准状况下,将一氧化氮、二氧化氮、氧气三种气体按一定比例充满一固定容积的容器,并将该容器倒置在水槽中,充分反应后,容器中无气体剩余,所得溶液的浓度为Mmol·L-1。则M的取值范围是( )
A. 0<M<
B.
<M<
C.
<M<
D.
<M<
难度: 中等查看答案及解析
-
实验室有几瓶显酸性的溶液,4位同学选择了其中四瓶测定其中所含的较大浓度的离子,他们的结论一定错误的是( )
A. Fe3+、Al3+、Cl-、Br- B. Fe2+、Cu2+、
、
C. Na+、K+、
、Cl- D. Mg2+、Cu2+、Cl-、
难度: 中等查看答案及解析
-
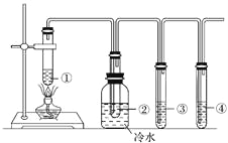
以下实验装置一般不用于分离物质的是( )
A.
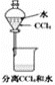 B.
B. C.
 D.
D. 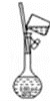
难度: 简单查看答案及解析
-
下列关于化学与生产、生活的认识错误的是
A. CO2、SO2、N2等均是造成温室效应的气体
B. 节能减排符合低碳经济的要求
C. 使用清洁能源是防止酸雨发生的重要措施之一
D. 大量焚烧田间秸秆会污染空气
难度: 简单查看答案及解析
-
诺贝尔化学奖曾授予德国化学家Gerhard Ertl,以表彰他对固体表面化学研究过程中的重大发现。使CO、NOx等在铂表面发生化学反应转变成无毒气体,以减少汽车尾气中有毒气体的排放,这是此项研究的重要应用之一。下列有关说法不正确的是( )
A. CO在铂表面被氧化生成CO2,铂起催化作用
B. 汽车尾气中NOx在铂表面发生反应的产物是N2
C. CO在铂表面可能和O2、NOx反应
D. NOx、CO、CO2均能与人体中的血红蛋白结合
难度: 中等查看答案及解析
-
浓度为0.1 mol·L-1的HCl溶液VmL,加水稀释到2VmL,取出10 mL,这10 mL溶液中含有c(H+)( )
A. 0.5 mol·L-1 B. 0.01 mol·L-1 C. 0.02 mol·L-1 D. 0.05 mol·L-1
难度: 简单查看答案及解析
-
一个氢原子由一个质子和一个电子构成,不含中子。当1个氢原子失去1个电子后,它不会变成( )
A. 质子 B. 原子核 C. 阳离子 D. 阴离子
难度: 简单查看答案及解析
-
下列关于加成反应叙述不正确的是( )
A. 反应物一定含有碳碳双键
B. 反应物一定含有不饱和键
C. 产物不一定只有一种
D. 产物一定是化合物
难度: 简单查看答案及解析
-
1997年,第一只“克隆羊”在英国诞生,“克隆羊”的关键技术之一是找到一些特殊的酶,它们能激活普通体细胞,使之像生殖细胞一样发育成个体。下列有关酶的叙述错误的是
A.酶是具有催化功能的蛋白质
B.酶的催化作用具有选择性和专一性
C.酶通常在强酸或强碱条件下发挥作用
D.高温或紫外线照射会降低酶的活性
难度: 简单查看答案及解析
-
密闭容器中发生反应2SO2(g)+O2(g)
2SO3(g)。测得某一时刻SO2、O2、SO3物质的量浓度分别为0.2 mol·L-1、0.1 mol·L-1、0.2 mol·L-1。当反应达到平衡时,下列数据可能存在的是( )
A. SO2、O2浓度分别为0.4 mol·L-1、0.2 mol·L-1
B. SO3浓度为0.25 mol·L-1
C. SO3浓度为0.4 mol·L-1
D. SO3、SO2浓度均为0.15 mol·L-1
难度: 中等查看答案及解析
-
短周期中三种元素a、b、c在周期表中的位置如图,下列有关这三种元素的叙述正确的是( )
A. a是一种活泼的非金属元素
B. c的最高价氧化物的水化物是一种弱酸
C. b的氢化物很稳定
D. b元素的最高化合价为+7价
难度: 简单查看答案及解析
-
下列反应中属于加成反应的是( )
A. CH4+Cl2
CH3Cl+HCl
B. CH2===CH2+HCl―→CH3CH2Cl
C. CH3CH2OH+HBr
CH3CH2Br+H2O
D. 2CH3CH3+7O2
4CO2+6H2O
难度: 简单查看答案及解析
-
某烷烃的一种同分异构体只能生成一种一氯代物,则该烃的分子式不可能是
A. C2H6 B. C4H10 C. C5H12 D. C8H18
难度: 中等查看答案及解析
-
下列反应中可用来设计成原电池的是( )
A. CaO +H2O===Ca(OH)2 B. NaOH+HCl===NaCl+H2O
C. 2KClO3
2KCl+3O2↑ D. Zn+2HCl===ZnCl2+H2↑
难度: 简单查看答案及解析
-
合理利用燃料减小污染符合“绿色奥运”理念,下列关于燃料的说法正确的是( )
A. “可燃冰”是将水变为油的新型燃料
B. 氢气是具有热值高、无污染等优点的燃料
C. 乙醇是比汽油更环保、不可再生的燃料
D. 石油和煤是工厂经常使用的可再生的化石燃料
难度: 简单查看答案及解析
-
枸椽酸乙胺嗪可用于驱除肠道虫病,其结构简式如下图。下列物质中不能与枸椽酸乙胺嗪反应的是( )
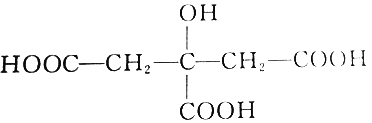 ,
,A. 乙酸 B. 乙醇 C. 碳酸钠溶液 D. 溴水
难度: 简单查看答案及解析
-
在一定条件下,动植物油脂与醇反应可制备生物柴油,化学方程式如下:
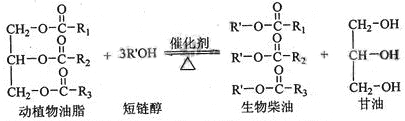
下列叙述错误的是( )
A. 生物柴油由可由再生资源制得 B. 生物柴油是不同酯组成的混合物
C. 动植物油脂是高分子化合物 D. “地沟油”可用于制备生物柴油
难度: 简单查看答案及解析
-
下列反应属于取代反应的是( )
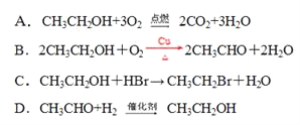
A. 答案A B. 答案B C. 答案 D. 答案D
难度: 简单查看答案及解析
-
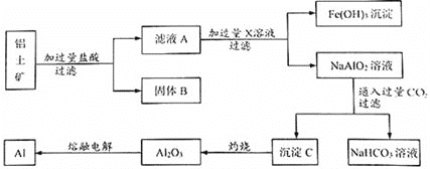
如图是两组物质之间在一定的条件下相互转化的过程.下列绿色植物通过光合作用说法不正确的是( )

A. 物质X是氧气
B. 绿色植物通过光合作用,将太阳能转化为化学能
C. C6H12O6是碳、氢、氧三种元素组成的化合物
D. C6H12O6与X反应生成二氧化碳和水属于置换反应
难度: 简单查看答案及解析
-
某物质在空气中充分燃烧生成CO2和H2O,则该物质( )
A. 只含碳元素 B. 只含氧元素
C. 只含碳、氧两种元素 D. 一定含碳、氢两种元素,可能含氧元素
难度: 简单查看答案及解析
-
甲、乙、丙、丁四种元素位于同一短周期,原子序数依次增加。下列判断正确的是
A.原子半径:甲<乙<丙
B.最外层电子数:丙>丁
C.若甲、乙、丙均是金属,则氢氧化物碱性:甲<乙<丙
D.若乙的最高价含氧酸为强酸,则丙是活泼非金属元素
难度: 中等查看答案及解析