-
在容量瓶上,无需标记的是
A. 标线
B. 温度
C. 浓度
D. 容量
难度: 简单查看答案及解析
-
将下列各组物质按单质、酸、碱、盐分类顺序排列,其中正确的是
A.氯水、盐酸、火碱、硫酸钡
B.水银、硫酸、烧碱、硫酸氢钠
C.铜、醋酸、石灰石、氯化铜
D.臭氧、硝酸、纯碱、胆矾
难度: 简单查看答案及解析
-
已知单质碘受热易升华.从海带中提取碘的实验过程中涉及下列操作,其中正确的是

A.将海带灼烧成灰
B.过滤得含I-的溶液
C.放出碘的苯溶液
D.分离碘并回收苯
难度: 中等查看答案及解析
-
氧化还原反应与四种基本反应类型的关系如图所示,则下列化学反应属于区域3的是
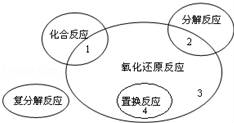
A.AgNO3+NaCl═AgCl↓+NaNO3
B.2F2+2H2O═4HF+O2
C.MgCl2(熔融)
Mg+Cl2↑
D.3CO+Fe2O3
2Fe+3CO2
难度: 中等查看答案及解析
-
下列应用或事实与胶体的性质没有关系的是
A.在河流入海口处易形成三角州
B.在饱和氯化铁溶液中逐滴加入NaOH溶液,产生红褐色沉淀
C.尿毒症患者做“血液透析”
D.用石膏或盐卤点制豆腐
难度: 中等查看答案及解析
-
下列关于钠的叙述中,不正确的是
A.钠燃烧时生成氧化钠
B.钠有很强的还原性
C.钠原子的最外层只有一个电子
D.钠燃烧时发出黄色火焰
难度: 简单查看答案及解析
-
下列说法正确的是
A.蔗糖、酒精在水溶液
中和熔融态时均不导电,所以它们是非电解质
B.SO3、NH3的水溶液均能导电,所以均是电解质
C.钢铁、石墨均导电,所以它们是电解质
D.液态硫酸、固态硫酸钡不能导电,所以二者均不是电解质
难度: 中等查看答案及解析
-
将钠投入滴有石蕊的水中,下列有关的现象叙述错误的是
A.钠浮在水面
B.水溶液变红色
C.有气体产生
D.钠熔成闪亮的小球并在水面四处游动
难度: 中等查看答案及解析
-
下列化学反应,能用离子方程式H++OH﹣=H2O来表示的是
A.硫酸和氢氧化钠溶液
B.盐酸和氢氧化铜
C.醋酸和氢氧化钡溶液
D.稀硝酸和氨水混合
难度: 中等查看答案及解析
-
同种物质中同一价态的元素部分被氧化,部分被还原的氧化
还原反应是
A.SO2+2H2S═S+2H2O
B.2NaNO32NaNO2+O2↑
C.NH4NO3N2O↑+2H2O
D.3Cl2+6KOH═5KCl+KClO3+3H2O
难度: 中等查看答案及解析
-
将6.4gSO2和8.0gSO3相比较,下列结论中错误的是
A.它们所含氧原子数目之比为2:3
B.它们的体积之比为1:1
C.它们所含原子数目之比为3:4
D.它们的分子数目之比为1:1
难度: 中等查看答案及解析
-
NA为阿伏加德罗常数,下列描述正确的是
A.含有NA个氦原子的氦气在标准状况下的体积约为11.2L
B.40gNaOH溶解在1L水中,所制得的溶液,物质的量浓度为1mol•L﹣1
C.标准状况下,11.2L四氯化碳所含分子数为0.5NA
D.常温常压下,5.6g铁与过量的盐酸反应转移电子总数为0.2NA
难度: 困难查看答案及解析
-
下列离子方程式
正确的是
A.氧化铜与硫酸溶液反应:Cu2++2H+═Cu2++H2O
B.碳酸钠溶液与盐酸反应:Na2CO3+2H+═2Na++H2O+CO2↑
C.少量CO2通入澄清石灰水中:CO2+Ca2++2OH﹣═CaCO3↓+H2O
D.钠投入到水中:Na+H2O═Na++OH﹣+H2↑
难度: 中等查看答案及解析
-
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.含0.1mol·L-1CaCl2的溶液:SO42-、Na+、NO3-、Cl-
B.使酚酞变红色的溶液:NH4+、K+、SO42-、NO3-
C.澄清透明溶液:Mg2+、Na+、Cl-、SO42-
D.在含有大量HCO3-的溶液中:Na+、NO3-、Cl-、OH-
难度: 中等查看答案及解析
-
物质的量浓度相同的硝酸钾、硫酸钾、磷酸钾(K3PO4)三种溶液中,若使钾离子的物质的量相同,则这三种溶液的体积比为
A.2:3:6
B.1:2:3
C.3:2:1
D.6:3:2
难度: 中等查看答案及解析
-
如下图两瓶体积相等的气体,在同温同压时瓶内气体的关系一定正确的是

A.气体密度相等
B.所含原子数相等
C.摩尔质量相等
D.气体质量相等
难度: 中等查看答案及解析
-
吸入人体內的氧有2%转化为氧化性极强的“活性氧”,它能加速人体衰老,被称为“生命杀手”,服用含硒元素(Se)的化合物亚硒酸钠(Na2SeO3),能消除人体內的活性氧,由此推断Na2SeO3的作用是
A.既作氧化剂又作还原剂
B.既不作氧化剂又不作还原剂
C.作还原剂
D.作氧化剂
难度: 中等查看答案及解析
-
一定条件下硝酸铵受热分解的化学方程式为:5NH4NO3=2HNO3+4N2+9H2O,在反应中被氧化与被还原的氮原子数之比为
A.5∶4
B.5∶3
C.3∶5
D.1∶1
难度: 中等查看答案及解析
-
根据下列反应的化学方程式,判断有关物质的还原性强弱
①2Fe2++Cl2═2Fe3++2Cl﹣
②I2+SO2+2H2O═H2SO4+2HI
③2Fe3++2I﹣═2Fe2++I2
A.SO2>I﹣>Fe2+>Cl﹣
B.I﹣>Fe2+>Cl﹣>SO2
C.Cl﹣>Fe2+>SO2>I﹣
D.Fe2+>I﹣>Cl﹣>SO2
难度: 中等查看答案及解析
-
12mL浓度为0.10mol・L-1的Na2SO3溶液,恰好与10mL浓度为0.04mol・L-1的K2Cr2O7溶液完全反应,已知Na2SO3能被K2Cr2O7氧化为Na2SO4,则元素C
r在还原产物中的化合价为
A.+5
B.+4
C.+3
D.+2
难度: 困难查看答案及解析
-
把500mL有BaCl2和KCl的混合溶液分
成5等份,取一份加入含amol硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含bm
ol硝酸银的溶液,恰好使氯离子完全沉淀.则原混合溶液中钾离子物质的量浓度为
A.10(2a﹣b)mol/L
B.0.1(b﹣2a)mol/L
C.10(b﹣2a)mol/L
D.10(b﹣a)mol/L
难度: 困难查看答案及解析
-
某溶液中只可能含有下列离子中的几种:K+、NO3-、SO42-、NH4+、CO32-(不考虑溶液中少量的H+和OH-),取200mL该溶液,分为两等份进行下列实验:
实验1:第一份加入足量的烧碱并加热,产生的气体在标准状况下为224mL;
实验2:第二份先加入足量的盐酸,无现象,再加入足量的BaCl2溶液,得固体2.33g。
下列说法正确的是
A.该溶液中一定不含NO3-
B.该溶液
中一定含K+,且c(K+)≥0.1mol/L
C.该溶液中可能含K+
D.该溶液中肯定含有NO3‑、SO42-、NH4+、CO32-
难度: 困难查看答案及解析