-
下列化学用语正确的是:
A .乙烯的结构式:CH2=CH2
B.Clˉ的结构示意图:

C.I—131:78 53I
D.Na2S 的电子式:
难度: 简单查看答案及解析
-
下列有关物质的分类合理的是
A.C60、HD均属于单质 B.漂白粉、明矾均属于混合物
C.氯化铵、硫酸均属于离子化合物 D.SO2、NxOy均属于酸性氧化物
难度: 简单查看答案及解析
-
下列说法正确的是
A.能自发进行的化学反应,一定是△H<0、△S>0
B.分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液
C.焰色反应是物质燃烧时火焰呈现的颜色变化,属于化学变化
D.钢铁发生电化学腐蚀时,负极的电极反应式为 Fe–3e- = Fe3+
难度: 中等查看答案及解析
-
用NA表示阿伏加德罗常数,下列叙述正确的是
A.10g46%的乙醇溶液所含氢原子数为1.2 NA
B.0.5 mol熔融的NaHSO4中含有的离子数目为1.5NA
C.标准状况下,2.24 L甲醇中含有C—H键的数目为0.3NA
D.S2和S8的混合物共38.4 g,其中所含硫原子数为1.4NA
难度: 中等查看答案及解析
-
某溶液中含有大量NH4+、Na+、HCO3ˉ、CO32ˉ、CH3COO-,加入足量的Na2O2固体后,溶液中离子浓度基本保持不变的是(假设溶液体积无变化)
A.Na+ B.CO32ˉ
C.CH3COO- D.NH4+
难度: 中等查看答案及解析
-
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.遇Fe(CN)63-生成特征蓝色沉淀的溶液:Ca2+、Clˉ、ClOˉ、Fe3+
B.遇石蕊变红的溶液:Na+、NH4+、NO3ˉ、K+
C.通有足量NO2的溶液:K+、Na+、SO32ˉ、AlO2ˉ
D.与铝反应产生大量氢气的溶液:Ba2+、HCO3ˉ、Iˉ、Fe2+
难度: 中等查看答案及解析
-
物质 R2CO3 的饱和溶液 V mL,密度为 ρ g·cm-3 ,c(R+) = P mol·L-1 ,溶质的质量分数为 a% ,溶质的相对分子量为 M,溶质的溶解度为sg。则下列表达式正确的是
A.a =
B.s =
C.P =
×2
D.V×ρ×a% =
难度: 中等查看答案及解析
-
下列表示对应化学反应的离子方程式正确的是
A.NaHSO4溶液与Ba(OH)2溶液反应至中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O
B.向FeCl2溶液中通入氯气:Fe2+ + Cl2 = Fe3+ + 2Cl-
C.向Ca(ClO)2溶液中通入过量的SO2:C1O- + SO2 + H2O=HClO + HSO3-
D.FeSO4酸性溶液中加H2O2:2Fe2++H2O2=2Fe3++2OH-
难度: 中等查看答案及解析
-
向等物质的量浓度的NaOH和Na2CO3的混合溶液中加入稀盐酸。下列离子方程式与事实不相符的是
A.OH-+CO32-+2H+ ===HCO3-+H2O
B.2OH-+CO32-+3H+ ===HCO3-+2H2O
C.2OH-+CO32-+4H+ ===CO2↑+3H2O
D.OH-+CO32-+3H+ ===CO2↑+2H2O
难度: 中等查看答案及解析
-
甲是一种常见的单质,乙、丙为中学常见的化合物,甲、乙、丙均含有元素 X 。它们有如下的转化关系(部分产物及反应条件已略去),下列判断正确的是
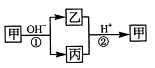
A.X 元素不一定为非金属元素 B.X元素可能为Al
C.反应①和②互为可逆反应 D.反应①和②一定为氧化还原反应
难度: 中等查看答案及解析
-
某离子反应中涉及H2O、ClO-、NH4+、H+、N2、Cl-六种微粒。其中N2的物质的量随时间变化的曲线如图所示。下列判断中正确的是

A.该反应的还原剂是Cl-
B.消耗1 mol还原剂,转移6 mol电子
C.氧化剂与还原剂的物质的量之比为2∶3
D.反应后溶液的酸性明显增强
难度: 中等查看答案及解析
-
下列有关实验装置的说法中正确的是

A.图1装置可制取干燥纯净的NH3
B.图2装置可以完成“喷泉”实验
C.图3装置可测量Cu 与浓硝酸反应产生气体的体积
D.图4装置可用于实验室制备Fe (OH)2
难度: 中等查看答案及解析
-
在常温下,将一定体积的某 NaOH 溶液分成两等分,与pH 均为2的一元酸 HA、HB恰好中和,消耗两种酸溶液的体积分别为V1、V2(V1≠V2)。则下列叙述中正确的是
A.若 Vl>V2,则说明 HA 的酸性比 HB的酸性强
B.中和后得到的两种溶液的 pH 均为 7
C.分别将两种酸溶液稀释10 倍后溶液的 pH 均为3
D.分别往等体积的两种酸溶液中加人足量锌粉,充分反应后产生的 H2的体积相等
难度: 中等查看答案及解析
-
某同学设计如下图所示装置,探究氯碱工业原理,下列说法正确的是
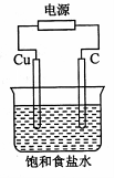
A.石墨电极与直流电源负极相连
B.用湿润KI淀粉试剂在铜电极附近检验气体,试纸变蓝色
C.氢氧化钠在石墨电极附近产生, Na+向石墨电极迁移
D.铜电极的反应式为:2H+ + 2e-= H2↑
难度: 中等查看答案及解析
-
常温下,下列各溶液的叙述中正确的是
A.NaHSO3与Na2SO3混合溶液中:3c(Na+)=c(HSO3-)+c(SO32-)
B.0.1 mol/L的醋酸钠溶液20 mL与0.1 mol/L盐酸10 mL混合后溶液显酸性:c(CH3COO-)>c(CH3COOH) >c(Cl-)>c(H+)
C.等物质的量浓度等体积的NH4HSO4和NaOH溶液混合:c(Na+)=c(SO42-)>c(NH4+)>c(H+)>c(OH-)
D.向1.00 L 0.3 mol/L NaOH溶液中缓慢通入0.2 mol CO2气体,溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+)
难度: 困难查看答案及解析
-
A由Al2O3、Fe3O4、Al、Cu中的某几种粉末混合而成,设计成份分析方案如下:
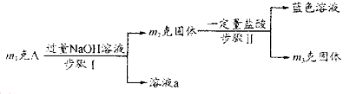
下列分析不正确的是
A.当m1>m2时,溶液a中阴离子只有1种
B.生成蓝色溶液的离子方程式为:
C.要确定混合物中是否含A1,可取A加入适量稀HC1
D.当m2-m3=2.96g,Fe3O4的质量至少为2.32 g
难度: 中等查看答案及解析