-
下列叙述正确的是( )
A.强电解质都是离子化合物,因此NaCl是离子化合物
B.醋酸溶液的导电能力可能比稀硫酸强
C.SO3溶于水,其水溶液能导电,SO3是电解质
D.硫磺是单质,不导电,因此硫磺是非电解质
难度: 中等查看答案及解析
-
俄罗斯科学家在利用回旋加速器进行的实验中,用含20个质子的钙元素的同位素反复轰击含95个质子的镅元素,结果4次成功制成4个第115号元素的原子。这4个原子在生成数微秒后衰变成第113号元素。前者的一种核素为X。下列有关叙述正确的是( )
A.X元素的核外电子数为288
B.核素X的质量数与中子数之差为173
C.113号元素属于非金属元素
D.115号元素的最高正化合价是+5
难度: 中等查看答案及解析
-
关于氢键,下列说法正确的是( )
A.甲硫醇(CH3SH)比甲醇的熔点低的原因是甲醇分子间易形成氢键
B.氯化钠易溶于水是因为形成了氢键
C.氨易液化与氨分子间存在氢键无关
D.H2O是一种非常稳定的化合物,这是由于氢键所致
难度: 中等查看答案及解析
-
下列有关反应热的叙述正确的是( )
A.已知2H2(g)+O2(g)===2H2O(g);ΔH=-483.6kJ/mol,则氢气的燃烧热为241.8kJ/mol
B.C(石墨,s)===C(金刚石,s);ΔH>0,所以金刚石比石墨稳定
C.已知碳的燃烧热为ykJ/mol,当7.2g的碳在12.8g的氧气中燃烧,至反应物耗尽并放出xkJ的热量,则可求出1mol碳与氧气反应生成一氧化碳时ΔH=(0.5y-2.5x)kJ/mol
D.己知2C(s)+2O2(g)===2CO2(g);ΔH1 2C(s)+O2(g)===2CO(g);ΔH2,则ΔH1>ΔH2
难度: 中等查看答案及解析
-
R、M、T、G、J为原子序数依次递增的同一短周期主族元素,下列说法一定正确的是(m、n均为正整数)( )
A.若M的最高正化合价为+4,则五种元素都是非金属元素
B.HnJOm为强酸,则G是位于ⅤA族以后的活泼非金属元素
C.若T的最低化合价为-3,则J的最高正化合价为+6
D.若R、M的最高价氧化物的水化物R(OH)n、M(OH)n+1均为碱,则Rn+的半径一定比M(n+1)+半径大
难度: 中等查看答案及解析
-
下面元素周期表被分成a、b、c、d四个区域,下列有关说法正确的是( )
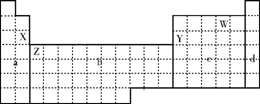
A.元素周期表中b区域全部是金属元素
B.X、Y两元素相比较,失电子能力较强的是X,可以验证该结论的实验是将在空气中放置已久的这两种元素的块状单质分别放入热水中
C.Z元素代表的是Ca元素
D.W元素是非金属元素,该元素对应的氢化物显酸性
难度: 中等查看答案及解析
-
下列叙述正确的是( )
A.O2和O2互为同位素,性质相似
B.常温下,pH=1的水溶液中Na+、NO、HCO、Fe2+可以大量共存
C.明矾和漂白粉常用于自来水的净化和杀菌消毒,两者的作用原理相同
D.硝酸铵溶于水是一个吸热过程,但常温下却能自发进行,说明ΔS>0
难度: 中等查看答案及解析
-
下列各组离子能在指定溶液中共存的是( )
①无色溶液中:K+、Cl-、Na+、H2PO、PO、SO
②使pH试纸变深蓝的溶液中:CO、NO、Na+、S2-、AlO、SO
③水电离的c(H+)=10-12mol/L的溶液中:ClO-、HCO、NO、NH、S2O
④加入Mg能放出H2的溶液中:Mg2+、NH、Cl-、Na+、SO
⑤使甲基橙变红的溶液中:MnO、NO、SO、Na+、Fe3+
⑥pH=0的溶液中:Fe2+、Al3+、NO、I-、Cl-、S2-
A.①③ B.②④⑤ C.①②⑤ D.③⑥
难度: 中等查看答案及解析
-
叠氮酸(HN3)与醋酸酸性相似,下列叙述中一定错误的是( )
A.HN3水溶液中微粒浓度大小顺序为:c(HN3)>c(H+)>c(N)>c(OH-)
B.HN3与NH3作用生成的叠氮酸铵是共价化合物
C.NaN3水溶液中离子浓度大小顺序为:c(Na+)>c(N)>c(OH-)>c(H+)
D.N与CO2含相等电子数
难度: 中等查看答案及解析
-
通常人们把拆开1mol某化学键吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可以估计化学反应的反应热(ΔH),化学反应的ΔH等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。下列是一些化学键的键能。
化学键
C—H
C—F
H—F
F—F
键能/(kJ·mol-1)
414
489
565
155
根据键能数据估算下列反应CH4(g)+4F2(g)===CF4(g)+4HF(g)的反应热ΔH为( )
A.-1940kJ·mol-1 B.1940kJ·mol-1
C.-485kJ·mol-1 D.485kJ·mol-1
难度: 中等查看答案及解析
-
中学化学课本中有大量的数据材料,下面是某学生对数据的利用,其中不正确的是( )
A.利用溶解度数据可判断煮沸Mg(HCO3)2溶液时,得到的产物是Mg(OH)2而不是MgCO3
B.利用密度数据可判断液态物质挥发性的大小
C.原子(或离子)半径数据可作为判断某些原子(或离子)的氧化性或还原性的依据
D.利用沸点数据可判断液态物质挥发性的大小
难度: 中等查看答案及解析
-
在某一容积为2L的密闭容器内,加入0.2mol的CO和0.2mol的H2O,在催化剂存在的条件下高温加热,发生如下反应:CO(g)+H2O(g)CO2(g)+H2(g);ΔH=a kJ/mol(a>0)
反应达到平衡后,测得c(CO)∶c(CO2)=3∶2。下列说法正确的是( )
A.反应放出的热量为0.2a kJ
B.平衡时H2O的转化率为40%
C.若升高温度,v(正)加快,v(逆)减慢,平衡正向移动
D.若将容器的体积压缩为1L,有利于该反应平衡正向移动
难度: 中等查看答案及解析
-
“神舟七号”所用动力燃料之一为氢化锂三兄弟:氕化锂、氘化锂、氚化锂。其中Li的核内中子数为4,有关下列叙述中正确的是( )
A.三种物质质子数之比为1∶2∶3
B.三种物质中子数之比为1∶1∶1
C.三种物质的摩尔质量之比为8∶9∶10
D.三种物质的化学性质不相同
难度: 中等查看答案及解析
-
最近发现一种O4新微粒,有关这种新微粒的说法正确的是( )
A.它是一种化合物
B.它的摩尔质量为64
C.由该微粒构成的物质是氧的一种新的同素异形体
D.它是由两个氧分子通过分子间作用力结合而成的新微粒
难度: 中等查看答案及解析
-
化学科学需要借助化学专用语言来描述,下列化学用语的书写正确的是( )
A.H
B.CCH3NH2COOH
C.H+[········]2-H+
D.CH4S的结构式CHHHSH
难度: 中等查看答案及解析
-
短周期元素A、B、C、D的原子序数依次递增,它们的原子序数之和为32,且原子最外层电子数之和为10;A、C原子的最外层电子数之和等于B原子的次外层电子数;A与C,B与D均为同主族元素。下列叙述正确的是( )
A.四种元素的原子半径:A<B<C<D
B.最高价氧化物对应的水化物的酸性:B>D
C.C元素处于元素周期表中第3周期第ⅡA族
D.C的最高价氧化物对应的水化物是强酸
难度: 中等查看答案及解析