-
“环境问题”是当今全球共同关注的焦点,在哥本哈根气候大会上中国发挥了重要的作用。下列对环境造成危害的一组首要污染物是
A.CO2、SO2、O2 B.CO2、N2、O2
C.SO2、NO2、可吸入颗粒物 D.NO2、N2、可吸入颗粒物
难度: 简单查看答案及解析
-
19世纪中叶,门捷列夫的突出贡献是
A.提出原子学说 B.发现元素周期律
C.提出分子学说 D.发现氧气
难度: 简单查看答案及解析
-
不能作为元素周期表中元素排列顺序的依据的是
A.原子的核电荷数 B.原子的核外电子数
C.原子的质子数 D.原子的中子数
难度: 简单查看答案及解析
-
某三价非金属的阴离子,核内有n个中子,质量数为A,则其该阴离子核外电子总数为
A.A-n-3 B. A-n C. A-n+3 D. A+n-3
难度: 简单查看答案及解析
-
HBr分子的电子式为
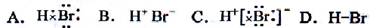
难度: 简单查看答案及解析
-
已知下列元素的半径为:
原子
N
S
O
Si
半径r/10-10m
0.75
1.02
0.74
1.17
根据以上数据,磷原子的半径可能是
A.1.10 ×10-10m B.0.80×10-10m
C.1.20×10-10m D.0.70×10-10m
难度: 简单查看答案及解析
-
已知短周期元素的离子 aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是
A.原子半径 A>B>D>C B.原子序数 d>c>b>a
C.离子半径 C>D>B>A D.单质的还原性 A>B>D>C
难度: 简单查看答案及解析
-
Te(碲)元素位于是第5周期ⅥA族,根据氧族元素的性质推断,碲不可能具有的性质是
A.Te与H2的反应比S与H2反应困难 B.H2Te比H2S稳定
C.TeO3对应的水化物是一种酸 D.有-2、+4、+6三种化合价
难度: 简单查看答案及解析
-
下列含氧酸的酸酐,不能由单质跟氧气直接化合得到的是
A.H2SO3 B.H2CO3 C.H2SO4 D.H2SiO3
难度: 简单查看答案及解析
-
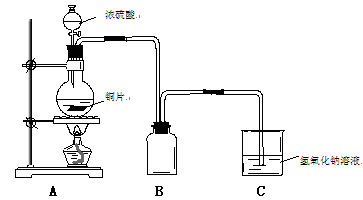
对于下列事实的解释错误的是
A.在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性
B.浓硝酸在光照下颜色变黄,说明浓硝酸不稳定
C.常温下,浓硝酸可以用铝罐贮存,说明铝与浓硝酸不反应
D.浓硝酸试剂瓶口常有白雾,说明浓硝酸有挥发性
难度: 简单查看答案及解析
-
下列各组物质间,不能发生反应的是
A.二氧化硅与氧化钙(高温) B.二氧化硅与氢氧化钠(常温)
C.二氧化硅与碳(高温) D.二氧化硅与浓HNO3(常温)
难度: 简单查看答案及解析
-
能实现下列物质间直接转化的元素是
A. 硅 B. 硫 C. 铜 D. 铁
难度: 简单查看答案及解析
-
检验SO2 气体中是否混有CO2 气体,可采用的方法是
A.通过品红溶液
B.通过澄清石灰水
C.先通过氢氧化钠溶液,再通过澄清石灰水
D.先通过酸性高锰酸钾溶液,再通过澄清石灰水
难度: 简单查看答案及解析
-
下列四种有色溶液与SO2作用,均能褪色。其实质相同的是
①品红溶液 ②酸性KMnO4溶液
③溴水 ④滴有酚酞的NaOH溶液
A.①④ B.①②③ C.②③ D.②④
难度: 简单查看答案及解析
-
在下图所示的实验装置中,实验进行一段时间后,对观察到的现象叙述不正确的是
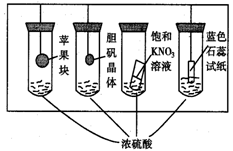
A.苹果块会干瘪
B.胆矾晶体表面有“白斑”
C.小试管内有KNO3晶体析出
D.蓝色石蕊试纸变红
难度: 简单查看答案及解析
-
下列各组离子在水溶液中可以大量共存的是
A. H+、Na+、NO
、Cl- B.SO
、H+、Ba2+、Cl-
C. NH4+、K+ 、OH-、I- D.H+、Fe2+、NO
、Cl-
难度: 简单查看答案及解析
-
在FeO 与足量HNO3的反应中,HNO3
A. 只表现氧化性 B. 只表现还原性
C. 既表现氧化性又表现酸性的是 D. 既表现氧化性又表现还原性的是
难度: 简单查看答案及解析
-
X元素最高氧化物对应的水化物为H3XO4,则它对应的气态氢化物为
A.HX B.H2X C.XH3 D.XH4
难度: 简单查看答案及解析
-
现有部分短周期元素的性质或原子结构如表:下列叙述正确的是
元素代号
元素性质或原子结构
T
M层上的电子数为6个
X
最外层电子数是次外层电子数的2倍
Y
常温下单质为双原子分子,其氢化物水溶液呈酸性
Z
元素最高正价是+7
A. 元素X的一种同位素可测定文物年代,这种同位素的符号是12C
B.元素Z的非金属性比元素T弱
C.Y和T位于同一主族
D.T、X、Y、Z四种元素的最高价氧化物水化物中化学性质明显不同于其它三种的是碳酸
难度: 简单查看答案及解析
-
下列说法不正确的是
A. 含有共价键的化合物一定是共价化合物
B. 含有离子键的化合物一定是离子化合物
C. 在离子化合物中可能存在共价键
D. 在共价化合物中不可能存在离子键
难度: 简单查看答案及解析
-
如图是进行气体性质实验的常用装置,下列对有关实验现象的说法中不正确的是
A.若水槽中是水,试管中是Br2蒸气,可看到试管中液面并未有明显上升
B.若水槽中是水,试管中是NO2,可看到试管中液面上升并充满整个试管
C.若水槽中是水(并滴有一定量酚酞),试管中是NH3,可看到液面上升并呈红色
D.若水槽中是水,试管中是NO,可看到试管中液面并未有明显上升
难度: 简单查看答案及解析