-
“3G”手机出现后,以光导纤维为基础的高速信息通道尤显重要。下列物质中用于制造光导纤维的材料是( )
A.铜合金 B.陶瓷 C.聚乙烯 D.二氧化硅
难度: 简单查看答案及解析
-
下列说法正确的是( )
①正常雨水的pH为7.0,酸雨的pH小于7.0;②严格执行机动车尾气排放标准有利于防止大气污染;③使用二氧化硫和某些含硫化合物进行增白的食品会损害人体健康;④使用氯气对自来水消毒过程中,生成的有机氯化物可能对人体有害;⑤食品厂产生的含丰富氮、磷营养素的废水可长期排向养鱼水库。
A.①②③ B.①④⑤ C.②③④ D.③④⑤
难度: 简单查看答案及解析
-
丰富多彩的颜色变化增添了化学实验的魅力,下列有关反应颜色变化的叙述中正确的是( )
①新制氯水久置后→浅黄绿色消失 ②Cl2通入石蕊试液中→先变红后褪色 ③SO2通入石蕊试液中→先变红后褪色 ④SO2通入品红溶液中→红色褪去 ⑤氨气通入酚酞溶液中→红色
A.①②③④ B.②③④⑤ C.①②④⑤ D.全部
难度: 中等查看答案及解析
-
不能用来鉴别新制氯水和长期放置的氯水的试剂是( )
A.石蕊试液 B.品红溶液 C.FeCl2溶液 D.AgNO3溶液
难度: 中等查看答案及解析
-
下列说法正确的是( )
A、SiO2与酸、碱均不反应
B、NO2溶于水时发生氧化还原反应
C、SO2具有氧化性,可用于漂白纸浆
D、Cl2、SO2均能使品红溶液褪色,说明二者均有氧化性
难度: 中等查看答案及解析
-
自来水常用Cl2消毒,某学生用这种自来水去配制下列物质的溶液,不会产生明显的药品变质问题的是( )
A.AgNO3 B.FeCl2 C.Na2SO3 D.AlCl3
难度: 中等查看答案及解析
-
下列实验装置不能达到实验目的的是( )
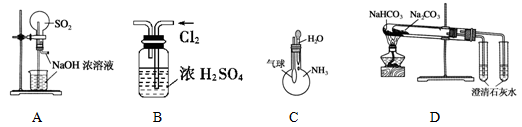
A.用SO2做喷泉实验 B.干燥氯气
C.验证NH3易溶于水 D.比较Na2CO3与NaHCO3的稳定性
难度: 简单查看答案及解析
-
下列物质间的转化能一步实现的是( )
A.SiO2 → H2SiO3 B.S → SO3 C.N2 → NO2 D.Cl2 → FeCl3
难度: 中等查看答案及解析
-
下列溶液中,不能用来区别SO2和CO2气体的是①石灰水 ②H2S溶液 ③KMnO4溶液
④紫色石蕊溶液 ⑤BaC12溶液 ⑥品红溶液( )
A.②③④ B.②④⑤ C.①④⑤ D.①⑤⑥
难度: 中等查看答案及解析
-
除去下列物质中的少量杂质(括号内的物质为杂质),所选用的试剂或方法不正确的是( )
A.CO2(SO2):饱和NaHCO3溶液 B.NO(NO2):水
C.Cl2(HCl):NaOH溶液 D.Na2CO3固体(NaHCO3):加热
难度: 中等查看答案及解析
-
下列离子在水溶液中能大量共存的是( )
A.Cl-、K+、HCO3-、Ca2+ B.OH-、NH4+、Mg2+、HCO3-
C.SO32—、H+、Cl-、NO3- D.Na+、SiO32-、H+、Cl-
难度: 中等查看答案及解析
-
下列说法正确的是( )
A、NO2与水的反应:3NO2+H2O===2NO+NO+2H+
B.氯气通入水中: Cl2 + H2O = 2H+ + Cl- + ClO-
C、向NH4HCO3溶液中加过量NaOH溶液并加热:NH4++OH-
NH3↑+H2O
D、向硅酸钠溶液中通入SO2:SiO32-+2H+=H2SiO3↓
难度: 中等查看答案及解析
-
氯气是一种重要的工业原料。工业上利用反应3Cl2+2NH3===N2+6HCl检查氯气管道是否漏气。下列说法错误的是( )
A.若管道漏气遇氨就会产生白烟 B.该反应利用了Cl2的强氧化性
C.该反应属于复分解反应 D.生成1 mol N2有6 mol电子转移
难度: 中等查看答案及解析
-
下列关于浓硝酸和浓硫酸的叙述,正确的是( )
A.常温下都用铜容器贮存
B.露置在空气中,容器内酸液的质量都减轻
C.常温下都能与铜较快反应
D.露置在空气中,容器内酸液的浓度都降低
难度: 中等查看答案及解析
-
浓硫酸有许多重要的性质,在与含有水分的蔗糖作用过程中不能显示的性质是( )
A.酸性 B.脱水性 C.强氧化性 D.吸水性
难度: 简单查看答案及解析
-
为除去镀在铝表面的铜镀层,可选用的试剂是( )
A.稀硝酸 B.浓硝酸 C.浓硫酸 D.浓盐酸
难度: 简单查看答案及解析
-
将盛满等体积NO、NO2混合气体的试管,倒置在水槽中,反应完毕后后,液面上升的高度是试管容积的 ( )
A、1/2 B、1/3 C、 2/3 D、5/6
难度: 中等查看答案及解析
-
在a L Al2(SO4)3和(NH4)2SO4的混合溶液中加入b mol BaCl2,恰好使溶液中的SO42-完全沉淀;如加入足量强碱并加热可得到c mol NH3,则原溶液中的Al3+浓度为( )
A. B.
C. D.
难度: 中等查看答案及解析
-
3.2g铜与过量硝酸(8 mol·L-1,30 mL)充分反应,硝酸的还原产物为NO2和NO,反应后溶液中含a mol H+,则此时溶液中所含NO的物质的量为( )
A.(0.2+a)mol B.(0.1+a)mol
C.(0.05+a)mol D.a mol
难度: 中等查看答案及解析
-
某溶液中含H+、SO、NO三种离子,其中H+、SO的物质的量浓度分别为7.0 mol·L-1和2.0 mol·L-1。取该溶液20 mL,加入3.2 g铜粉,加热使它们充分反应,产生的气体在标准状况下的体积约为( )
A.0.75 L B.0.336 L C.1.5 L D.0.448 L
难度: 中等查看答案及解析