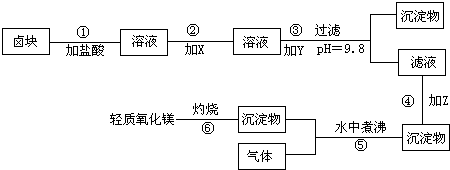
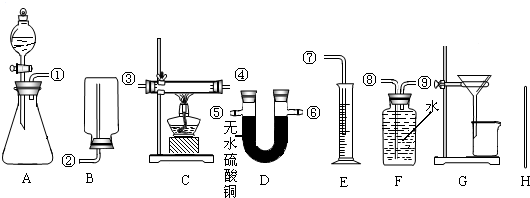
-
溶液中存在有五种离子,其中各离子个数比Cl-:SO42-:Fe3+:K+:M=2:3:1:3:1,则M为( )
A.CO32-
B.Mg2+
C.Na+
D.Ba2+难度: 中等查看答案及解析
-
金属La的活动性比锌强,它的氧化物为La2O3,其对应的碱为La(OH)3,La(OH)3难溶于水,而LaCl3可溶于水.下列各组中的物质难以直接反应而制得LaCl3的是( )
A.La+HCl
B.La2O3+HCl
C.La(OH)3+MgCl2
D.La(OH)3+HCl难度: 中等查看答案及解析
-
混有某种物质的纯碱106 g与足量的稀盐酸反应后,放出43 g二氧化碳,则下列物质中不可能混入的是( )
A.K2CO3
B.NaOH
C.MgCO3
D.CaCO3难度: 中等查看答案及解析
-
两只完全相同的烧杯,分别装有质量相等的浓盐酸和浓硫酸,将它们在空气中放置一段时间,在这过程中( )
A.浓盐酸会吸收空气中的水
B.浓硫酸会吸收空气中的水
C.浓盐酸中溶质的质量分数逐渐增大
D.浓硫酸中溶质的质量分数逐渐增大难度: 中等查看答案及解析
-
空气中含量最多的气体是( )
A.氧气
B.氮气
C.二氧化碳
D.稀有气体难度: 中等查看答案及解析
-
食醋、食盐、纯碱等均为家庭厨房中常见的物质,利用这些物质你能完成的实验是:( )
①检验自来水中是否含有氯离子 ②鉴别食盐和纯碱 ③检验鸡蛋壳能否溶于酸 ④除去热水瓶中的水垢.
A.①②
B.①③
C.①④
D.②③④难度: 中等查看答案及解析
-
如图形象地表示某反应前后反应物与生成物分子及其数目的变化,其中
分别表示A. B. C三种不同的分子.该反应的化学方程式中A. B. C前的化学计量数之比( )
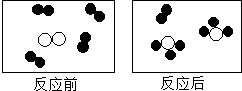
A.4:1:2
B.3:1:3
C.3:1:2
D.4:1:3难度: 中等查看答案及解析
-
研究物质的变化时可使用具有放射性的18O作为“示踪原子”.科学家希尔和尼尔研究证明,光合作用的通式应更合理地表达为:6CO2+12H218O
C6H12O6+6H2O+618O2在光照充分的环境里,将一种植物--黑藻放入含有“示踪原子”18O的水中一段时间后分析“示踪原子”,最有可能是( )
A.在植物体周围的空气中发现
B.在植物体内的葡萄糖(C6H12O6)中发现
C.在植物体内的淀粉和蛋白质中发现
D.无法确定示踪原子在什么地方出现难度: 中等查看答案及解析
-
试管内壁附着油脂,下列洗涤方法不可取的是( )
A.用洗衣粉溶液刷洗
B.用自来水刷洗
C.用热肥皂水刷洗
D.用汽油刷洗难度: 中等查看答案及解析
-
为防止煤气逸散使人中毒,常在煤气中加入少量的有特殊激性气味的乙硫醇(C2H5SH).乙硫醇在煤气燃烧过程中也可以充分燃烧,其化学方程式为:2C2H5SH+9O2
4CO2+2Ⅹ+6H2O,则X的化学式为( )
A.H2SO4
B.SO3
C.SO2
D.CO难度: 中等查看答案及解析
-
宇宙飞船可用铝粉与高氯酸铵(NH4ClO4)的固体混合物作燃料,点燃时,铝粉被氧化放热引发高氯酸铵分解,化学方程式为:2NH4ClO4=N2↑+4H2O+Cl2↑+2O2↑.下列对此反应的叙述错误的是( )
A.该反应属于分解反应
B.该反应产生大量高温气体,推动飞船飞行
C.该反应中有能量形式上的变化
D.在反应中高氯酸铵只起到氧化剂作用难度: 中等查看答案及解析
-
某物质X可发生下列变化:X
Y
Z
X,则X可能是 ( )
A.CuO
B.Fe(OH)3
C.Na2CO3
D.Fe2O3难度: 中等查看答案及解析
-
在一定温度下,某固态溶质(不含结晶水)的水溶液甲,经历如下变化:
溶液甲溶液乙
溶液丙
下列结论正确的是( )
A.溶液甲可能是饱和溶液
B.溶液乙和溶液丙中的溶质质量分数可能相等
C.溶液乙一定是不饱和溶液
D.溶液丙若再蒸发5g水,析出的晶体可能大于2g难度: 中等查看答案及解析
-
右图是收集某干燥气体并对它吸收处理的正确装置.由图中的实验装置推测出该气体的有关性质正确的一组是( )
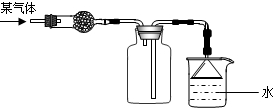
A.密度大于空气,难溶于水
B.密度大于空气,易溶于水
C.密度小于空气,易溶于水
D.密度小于空气,难溶于水难度: 中等查看答案及解析
-
氢氧化钠固体易吸收空气中的二氧化碳而变质.取4.65g已部分变质的氢氧化钠固体与36.5g 10%的盐酸恰好完全反应后,将溶液蒸干,所得固体的质量是( )
A.11.7g
B.5.85g
C.4.65g
D.8.3g难度: 中等查看答案及解析