-
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A.20mL 10mol·L-1的浓硝酸或浓硫酸与足量铜加热反应转移电子数均为0.2NA
B.0.1mol的白磷(P4)或甲烷中所含的共价键数均为0.4NA
C.在精炼铜或电镀铜的过程中,当阴极析出铜32g转移电子数均为NA
D.标准状况下,2.24L Cl2通入足量H2O或NaOH溶液中转移的电子数均为0.1NA
难度: 困难查看答案及解析
-
某工业生产中有一主要反应:CuFeS2+4Fe3+=5Fe2+ +Cu2++ 2S,其中CuFeS2中Cu为+2价。下列说法正确的是( )
A.氧化剂为Fe3+,还原剂为Cu2+和S2+
B.氧化产物是S,还原产物是Fe2+和Cu2+
C.当转移1mol电子时,有46 g CuFeS2参加反应
D.氧化剂的氧化性Fe3+>Fe2+>Cu2+
难度: 困难查看答案及解析
-
下述实验操作与预期实验目的或所得实验结论不一致的是( )
编号 实验操作 实验目的或结论
A 常温下,向饱和Na2CO3溶液中加入少量BaSO4粉末,过滤,向洗涤液中加稀盐酸,有气泡产生 说明常温下,Ksp(BaCO3)< Ksp(BaSO4)
B 向试管中加入等体积的0.005mol/L的FeCl3溶液和0.01mol/L的KSCN溶液,再滴加几滴饱和FeCl3溶液,观察颜色变化 探究增大反应物浓度,平衡移动的方向
C 将SO2通入品红溶液,褪色后加热,观察颜色能否恢复 验证SO2漂白的可逆性
D 分别测同温同物质的量浓度Na2CO3和Na2SO4水溶液的pH 探究碳和硅两元素非金属性强弱
难度: 困难查看答案及解析
-
将铝粉和四氧化三铁粉末配成的铝热剂分成两等份:一份在高温下恰好反应,再与足量稀硫酸反应,生成氢气a L;另一份直接放入足量的氢氧化钠溶液中充分反应,在相同条件下生成氢气b L,则a︰b为( )
A.1:1 B.4:3 C.3:4 D.8:9
难度: 困难查看答案及解析
-
设氨水的pH=x,某盐酸的pH=y,已知x+y=14,且x>11。将上述两溶液分别取等体积充分混合后,所得溶液中各离子浓度由大到小的顺序是( )
A.c(Cl-)>c(NH4+)>c(H+)>c(OH-) B.c(NH4+)>c(Cl-)>c(H+)>c(OH-)
C.c(NH4+)>c(Cl-)>c(OH-)>c(H+) D.c(Cl-)>c(NH4+)>c(OH-)>c(H+)
难度: 困难查看答案及解析
-
有关下图所示化合物的说法不正确的是( )
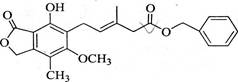
A.既可以与Br2的CCl4溶液发生加成反应,又可以在光照下与Br2发生取代反应
B.1 mol该化合物最多可以与3 mol NaOH反应
C.既可以催化加氢,又可以使酸性KMnO4溶液褪色
D.既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体
难度: 困难查看答案及解析
-
一种新型燃料电池,它以多孔镍板为电极插入KOH溶液中,然后分别向两极上通入乙烷和氧气,其电极反应式为:C2H6+18OH--14e - =2CO32-+12H2O
7H2O+7/2O2+14e -=14OH-,有关此电池的推断正确的是( )
A.通氧气的电极为负极
B.参加反应的氧气与C2H6的物质的量之比为7∶2
C.放电一段时间后,KOH的物质的量浓度不变
D.电解质溶液中CO32-向正极移动
难度: 困难查看答案及解析