-
下列叙述正确的是( )
A. 地球上的金属元素都是以化合态存在于自然界中
B. 金属阳离子被还原一定得到金属单质
C. NaHCO3比Na2CO3热稳定性强
D. 金刚石、石墨、C60都是碳元素的单质,物理性质差别很大,因为它们的结构不同
难度: 简单查看答案及解析
-
某学生运用所学知识研究钠的性质:将一粒金属钠和一块铜片分别盛在表面皿中,来研究它们在空气中的稳定性。该学生采用的研究方法是:( )
①假说法 ②实验法 ③分类法 ④比较法
A. ①② B. ①③ C. ②④ D. ①③
难度: 简单查看答案及解析
-
下列变化中,属于被氧化的是 ( )
A. CaO → Ca(OH)2 B. Cu2+ → Cu C. Fe2+ → Fe3 + D. CO2→CO
难度: 简单查看答案及解析
-
下列物质不属于同素异形体的是
A. 金刚石和石墨 B. 生石灰和熟石灰
C. 红磷和白磷 D. C60和金刚石
难度: 简单查看答案及解析
-
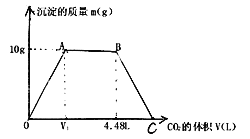
用1 L1.0mol/LNaOH溶液吸收0.8molCO2,所得溶液中的CO32-和HCO3-的物质的量浓度之比约是
A. 1:3 B. 2:1 C. 2:3 D. 3:2
难度: 简单查看答案及解析
-
以下实验装置一般不用于分离物质的是
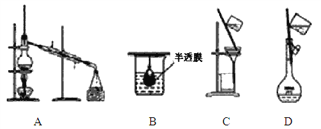
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
某同学弄清氨的喷泉实验原理后有了一个创新的设计:如果改换一下烧瓶内的气体和胶头滴管与烧杯中的液体,也能做成喷泉实验。那么下列各组中的气体和液体不符合该学生设计的一组是
A. SO2和NaOH溶液 B. CO2和NaOH溶液
C. O2和水 D. Cl2和NaOH溶液
难度: 简单查看答案及解析
-
实验室制取少量N2常利用的反应是NaNO2+NH4Cl
NaCl+N2↑+2H2O,关于该反应的说法正确的是
A.NaNO2是还原剂
B.生成1molN2时转移的电子为6mol
C.NH4Cl中的N元素被氧化
D.N2既是氧化剂又是还原剂
难度: 中等查看答案及解析
-
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
A. 1 mol N2所含有的原子数为NA
B. 标准状况下,22.4 L水中含有的水分子数为NA
C. 标准状况下,22.4 L氯化氢所含的原子数为NA
D. 24 g O2分子和24 g O3分子所含的氧原子数目相等
难度: 简单查看答案及解析
-
下列离子方程式的书写正确的是( )
A. 铁和稀硫酸反应:2Fe + 6H+ =2Fe 3+ +3H 2↑
B. NaHCO3溶液与NaOH溶液反应:OH― + HCO3―=CO32―+ H2O
C. 钠和冷水反应 Na+2H2O=Na++2OH-+H2↑
D. 少量金属钠投入到CuSO4溶液中2Na+Cu2+=2Na++Cu↓
难度: 中等查看答案及解析
-
某同学对一无色透明溶液进行分析得出该溶液中含有下列某组离子,你认为该组离子应该是
A. Al3+、NO3―、K+、SO42ˉ B. Ca2+、H+、CO32ˉ、Fe2+
C. OHˉ、SO42ˉ、NH4+、Fe3+ D. Fe3+、Mg2+、NO3ˉ、Clˉ
难度: 简单查看答案及解析
-
某盐的混合物中含有0.2 mol/L Na+、0.4 mol/L Mg2+、0.4 mol/L Clˉ,则SO42ˉ为
A. 0.1 mol/L B. 0.2 mol/L
C. 0.3 mol/L D. 0.4 mol/L
难度: 中等查看答案及解析
-
用0.1mol/L的Na2SO3溶液30mL,恰好将2×10-3mol XO4-还原,则元素X在还原产物中的化合价是( )
A. +4 B. +3 C. +2 D. +1
难度: 中等查看答案及解析
-
为了检验某溶液中是否含有常见的四种无机离子,某化学小组的同学进行了如下所示的实验操作。其中检验过程中产生的气体能使湿润的红色石蕊试纸变蓝。由该实验能得出的正确结论是( )
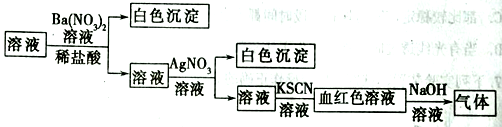
A.原溶液中一定含有SO42- B.原溶液中一定含有NH4+
C.原溶液中一定含有Cl- D.原溶液中一定含有Fe3+
难度: 中等查看答案及解析