-
某些试剂瓶上常贴有危险化学品的标志。盛装浓硫酸的试剂瓶上所贴标志应该是
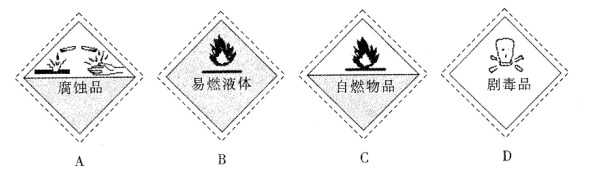
难度: 简单查看答案及解析
-
下面有关碳酸钠和碳酸氢钠说法不正确的是
A、碳酸氢钠不稳定,受热易分解
B、碳酸氢钠可以用作治疗胃酸过多的药物
C、碳酸钠溶液显碱性,所以碳酸钠是碱
D、碳酸钠既是钠盐、又是碳酸盐、还是可溶性盐
难度: 中等查看答案及解析
-
下列说法正确的是
A、盛装NaOH溶液的试剂瓶用橡胶塞,不用玻璃塞
B、水晶是无色透明的晶体,可以制成硅太阳能电池
C、将FeCl3饱和溶液滴入沸水中,可以立即得到Fe(OH)3胶体
D、不能通过丁达尔效应来鉴别Fe(OH)3胶体和CuSO4溶液
难度: 中等查看答案及解析
-
关于金属铝和铁的说法不正确的是
A、铁与热水不反应,但是可与水蒸气发生置换反应
B、铝箔在空气中受热可以熔化,剧烈燃烧,产生大量的热
C、常温下,可以用铝或铁制容器来盛装冷的浓硫酸或冷的浓硝酸
D、铝元素是地壳中含量最多的金属元素,而铁是用途最广的金属
难度: 中等查看答案及解析
-
有关氧化还原反应说法正确的是
A、置换反应一定是氧化还原反应
B、氧化剂具有氧化性、发生氧化反应
C、非金属单质在反应中只能得到电子做氧化剂
D、某元素从化合态变到游离态时,该元素一定是被还原
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数的值,下列说法正确的是
A、2g氢气所含原子数是NA
B、17g NH3所含的电子数是10NA
C、NA个氧分子和NA个氢分子的质量比等于1:1
D、2.3g金属钠全部变成钠离子时失去的电子数是0.2NA
难度: 中等查看答案及解析
-
下列各组物质中,分子数目相同的是
A、2g H2和16gO2
B、1 mol O2和18gH2O
C、22.4 L He和1mol H2
D、标准状况下,2 L H2和2 L H2O
难度: 中等查看答案及解析
-
下列各溶液中NO3-物质的量浓度最大的是
A、20 mL 2 moL/L Mg(NO3)2
B、100 mL 2.5 mot/L NaNO3
C、25 mL 1.0mol/L Al(NO3)3
D、30 mL 2.5 mol/L NH4NO3
难度: 中等查看答案及解析
-
利用下列化学反应可以查出驾驶员是否酒后驾车:
2CrO3(红色)+3C2H5OH+3H2SO4=Cr2(SO4)3(绿色)+3CH3CHO+6H2O
上述反应中的氧化剂是
A、H2SO4B、C2H5OH C、Cr2(SO4)3D、CrO3
难度: 中等查看答案及解析
-
下列各组离子能大量共存,加入NaOH溶液后有沉淀生成,加人盐酸后有气体生成的是
A、Na+、Cu2+、Cl-、CO32- B、Na+、Ca2+、Cl-、HCO3-
C、Ca2+、Al3+、Cl-、NO3- D、K+、Al3+、SO42-、Cl-
难度: 中等查看答案及解析
-
两份质量相同的铝片,分别与足量的盐酸和氢氧化钠溶液反应,在相同条件下分别产生的气体体积比是
A、1:1 B、2:3 C、3:2 D、1:6
难度: 中等查看答案及解析
-
可以用氯气对自来水进行消毒,若用这种自来水配制下列物质的溶液,不会引起药品明显变质的是
A、NaOH B、Na2CO3 C、FeCl2 D、NaCl
难度: 中等查看答案及解析
-
欲除去NaHCO3溶液中少量的Na2CO3,可选用的试剂是
A、饱和石灰水 B、NaOH溶液 C、盐酸 D、CO2
难度: 中等查看答案及解析
-
下列现象不能用于检验NH3的是
A、气体遇浓盐酸产生白烟
B、气体使湿润的蓝色石蕊试纸变红
C、气体通人酚酞溶液中,溶液变红
D、气体使湿润的红色石蕊试纸变蓝
难度: 中等查看答案及解析
-
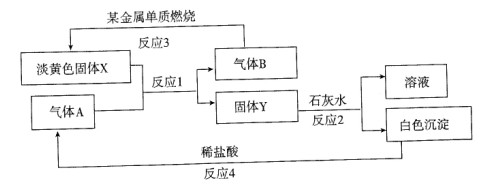
将一小块金属钠放在坩埚里加热,实验现象描述正确的是:
①钠在燃烧之前先熔化 ②钠燃烧的火焰呈紫色
③钠燃烧后得到白色固体 ④钠燃烧的火焰呈黄色
⑤钠燃烧后生成物为淡黄色固体
其中正确的是
A、只有⑤ B、只有① C、①④⑤ D、②③
难度: 简单查看答案及解析
-
下列物质①NaHCO3 ②Al(OH)3 ③K2SO4 ④AgNO3中,既能与盐酸反应、又能与氢氧化钠溶液反应的是
A、②④ B、①④ C、③④ D、①②④
难度: 中等查看答案及解析
-
硫酸亚铁溶液中若含有少量的硫酸铜和硫酸铁,为除去这两种杂质,提纯硫酸亚铁,可向溶液中加人的物质是
A、锌粉 B、镁粉 C、铁粉 D、铝粉
难度: 中等查看答案及解析
-
已知:2FeCl3+Cu=2FeCl2+CuCl2,向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,不可能出现的结果是
A、烧杯中有铜无铁
B、烧杯中有铁无铜
C、烧杯中铁、铜都有
D、烧杯中铁、铜都无
难度: 中等查看答案及解析
-
下列离子方程式不正确的是
A、将一小粒金属钠放入水中:2Na+2H2O=2Na++2OH-+H2↑
B、将氯气通入氢氧化钠溶液中:Cl2+2OH-=C1-+C1O-+H2O
C、向CuSO4溶液中加入适量Ba(OH)2溶液:Ba2++SO42-=BaSO4↓
D、向稀硝酸中加人铜片:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
难度: 中等查看答案及解析
-
某混合气体中可能含有Cl2、O2、SO2、NO、NO2中的两种或多种。若该气体为无色气体,且通过品红溶液后,品红溶液褪色,剩余气体与空气接触时,很快变为红棕色。下列判断正确的是
A、肯定只有NO
B、肯定有SO2和O2
C、可能有Cl2和O2
D、肯定没有Cl2、O2和NO2
难度: 中等查看答案及解析
-
在SiO2+3C
SiC+2CO↑反应中,氧化剂和还原剂的质量比为
A、36:30 B、60:36 C、2:1 D、1:2
难度: 中等查看答案及解析
-
高铁酸钠(Na2FeO4)是一种高效的饮用水处理剂,工业上可由下列方法制得:Fe2O3+3Na2O2
2Na2FeO4+Na2O
关于该反应说法正确的是
A、反应中Na2O2是氧化剂
B、Fe2O3可以通过铁丝在氧气中燃烧制得
C、生成1 mol Na2FeO4,有6 mol电子转移
D、在Na2FeO4中Fe为+4价,具有强氧化性,能消毒杀菌
难度: 中等查看答案及解析
-
用如图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应。下列实验不合理的是

A、上下移动①中铜丝可控制SO2的量
B、②中选用品红溶液验证SO2的生成
C、③中选用NaOH溶液吸收多余的SO2
D、为确认CuSO4生成,向①中加水,观察颜色
难度: 中等查看答案及解析
-
将8g铁片放入100 mL CuSO4溶液中,Cu2+全部被置换后,取出附有铜的铁片洗涤、干燥、称重,其质量变为8.2g,则原溶液中CuSO4的物质的量浓度是
A、0.125ol/L B、0.175mol/L C、0.25 mol/L D、0.5 mol/L
难度: 中等查看答案及解析
-
标准状况下,将充满O2和NO2混合气体的试管倒置于水中,液体完全充满试管。此时试管内溶液中溶质的物质的量浓度是
A、0.045 mol/L B、0.036 mol/L C、0.026 mol/L D、0.028 mol/L
难度: 中等查看答案及解析
-
实验室欲配制100 mL、1mol/L的NaCl溶液,请回答:
(1)不需要使用的仪器是________。
A、烧杯B、500 mL容量瓶C、量筒 D、胶头滴管 E、玻璃棒 F、100 mL容量瓶
(2)配制时用托盘天平应称取NaCl________g。
(3)配制溶液的操作顺序是(用字母表示) ________。
A、称量 B、洗涤 C、定容 D、溶解 E、摇匀 F、转移
难度: 中等查看答案及解析
-
ClO2气体是一种常用的消毒剂,我国从2000年起逐步用ClO2代替氯气对饮用水进行消毒。
(1)消毒水时,ClO2还可将水中的Fe2+、Mn2+等转化成Fe(OH)3和MnO2等难溶物除去,此过程说明ClO2具有________(填“氧化”或“还原”)性。
(2)工业上可以通过下列方法制取ClO2,请完成该反应化学方程式:2KClO3+SO2=2C1O2+ ________ 。
难度: 中等查看答案及解析