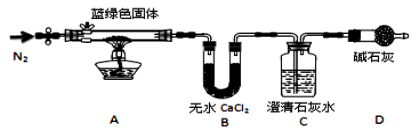-
下列实验操作正确的是
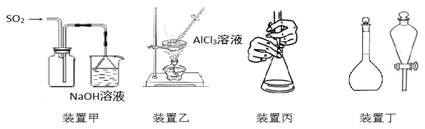
A. 用装置甲收集SO2
B. 用装置乙制备AlCl3晶体
C. 用装置丙进行中和滴定时,滴定前锥形瓶先用待装液润洗
D. 装置丁中使用分液漏斗和容量瓶时,先要检查仪器是否漏液
难度: 简单查看答案及解析
-
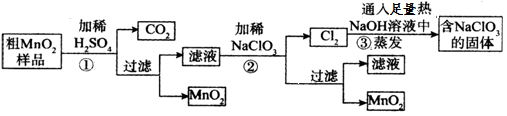
下列物质转化在给定条件下能实现的是

难度: 简单查看答案及解析
-
下图1为甲烷和O2构成的燃料电池示意图,电解质为KOH溶液,图2为电解AlCl3溶液的装置,电极材料均为石墨。用该装置进行实验,反
应开始后观察到x电极附近出现白色沉淀。下列说法正确的是
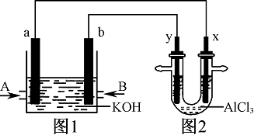
A.图1中电解质溶液的pH增大
B.图2中电解AlCl3溶液的总反应为2Cl-+2H2O
Cl2↑+H2↑+2OH-
C.A处通入的气体为CH4,电极反应式为CH4+10OH--8e-=CO32-+7H2O
D.电解池中Cl-向x极移动
难度: 简单查看答案及解析
-
下列指定反应的离子方程式正确的是
A.BaSO3与稀HNO3反应:BaSO3+2H+=Ba2++SO2↑+H2O
B.Ca(OH)2溶液与过量NaHCO3溶液反应:HCO3-+Ca2++OH-=CaCO3↓+H2O
C.酸性溶液中KIO3与KI反应生成I2:IO
3-+I-+6H+=I2+3H2O
D.向CuSO4
溶液中加入Na2O2:2Na2O2+2Cu2++2H2O=4
Na++2Cu(OH)2↓+O2↑
难度: 简单查看答案及解析
-
热激活电池可用作火箭、导弹的工作电源。一种热激活电池的基本结构如图所示,作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为:PbSO4+2LiCl+Ca = CaCl2+Li2SO4+Pb。下列有关说法正确的是
A.正极反应式:Ca + 2Cl--2e- = CaCl2
B.放电过程中,Li+向负极移动
C.常温时,在正负极间接上电流表或检流计,指针发生偏转
D.每转移0.1mol电子,理论上生成10.35 g Pb
难度: 简单查看答案及解析
-
六种短周期元素A、B、C、D、E、F的原子序数依次增大,A和D同族,C和F同族,B、C、D、E的离子均具有相同的电子层结构,E在同周期元素中离子半径最小。A和B、C、F均能形成共价型化合物,A和B形成的化合物Y在水中呈碱性,D和F形成的化合物在水中呈中性。下列说法错误的是
A. B、D离子的半径大小是B>D
B. 化合物AC的沸点比化合物AF的高
C. C的单质能将F单质从EF3的溶液中置换出来
D. 化合物AF与化合物Y可反应生成含有共价键的离子化合物
难度: 中等查看答案及解析
-
下列说法不正确的是
A.等物质的量浓度的 NH4HSO4溶液和NaOH溶液等体积混合,溶液中各离子浓度大小关系为:c(Na+)=c(SO42﹣)>c(NH4+)>c(H+)>c(OH﹣)
B.25℃ 时,将 a mo1•L﹣l 氨水与 0.01 moI•L﹣1 盐酸等体积混合,反应完全时溶液中c(NH4+)=c(C1﹣),用含a的代数
式表示NH3•H2O的电离常数Kb=
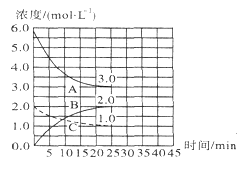
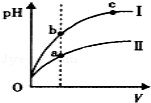
C.某温度下,相同体积、相同pH的盐酸和醋酸溶液分别加水稀释,pH随溶液体积V变化的 曲线如图所示。Ⅱ为醋酸稀释时pH的变化曲线,且a、b两点水的电离程度:a<b
D.已知298K时氢氰酸(HCN)的Ka=4.9×10﹣10、碳酸的Ka1=4.4×10﹣7,Ka2=4.7×10﹣11,据此可推测将氢氰酸加入到碳酸钠溶液中能观察到有气泡产生
难度: 简单查看答案及解析