-
0.05 mol某金属单质与足量的盐酸反应,放出1.12LH2(标准状况),并转变为具有Ar原子的电子层结构的离子,该金属元素在元素周期表中的位置是
A.第三周期第IA族 B.第四周期第IA族
C.第三周期第ⅡA族 D.第四周期第ⅡA族
难度: 简单查看答案及解析
-
通常情况下能共存且能用浓硫酸干燥的气体组是
A.SO2、Cl2、H2S B.O2、H2、SO2
C.CH4、H2、Cl2 D.HCl、CO、NH3
难度: 简单查看答案及解析
-
核外电子排布相同的离子Am+和Bn-,两种元素的质子数,前者与后者的关系是
A.大于 B.小于 C.等于 D.不能肯定
难度: 简单查看答案及解析
-
实验室贮存固体试剂可以放在广口瓶中,液体试剂放在细口瓶中,但是有些试剂必须贮存在具有橡胶塞的玻璃试剂瓶中。以下物质必须贮存在具有橡胶塞的玻璃试剂瓶中的是 ①KOH溶液 ②Na2SiO3溶液 ③盐酸 ④氢氟酸 ⑤澄清石灰水 ⑥硝酸 ⑦NaCl溶液
A.①②⑤ B.①②④⑤ C.①②④⑤⑦ D.①②⑤⑦
难度: 中等查看答案及解析
-
向50mL 18mol/L H2SO4溶液中加入足量的铜片并加热。充分反应后,被还原的H2SO4的物质的量
A.小于0.45mol B.等于0.45mol
C.在0.45mol和0.90mol之间 D.大于0.90mol
难度: 简单查看答案及解析
-
在标准状况下,将22.4 L NO2通入过量的NaHCO3溶液中,再使逸出的气体通过装有足量Na2O2颗粒的干燥管,最后收集到的气体是
A.O2 B.CO2和O2 C.NO2和O2 D.NO
难度: 中等查看答案及解析
-
下列试剂:①浓硫酸、②氯水、③硝酸银、④浓硝酸、⑤浓盐酸、⑥溴化银,其中必须用棕色试剂瓶装的有
A.①②③④⑤⑥ B.②③④⑥ C.②③⑤⑥ D.①③④⑥
难度: 简单查看答案及解析
-
下列四种有色溶液与SO2气体作用时均能褪色,其实质相同的是
①红色的品红溶液;②紫色的酸性KMnO4溶液;③橙色的溴水;④显红色(含NaOH)的酚酞溶液
A.①④ B.②③ C.①③ D.②④
难度: 中等查看答案及解析
-
将10 mL NO和NO2的混合气体通入装满水的倒立在水槽中的量筒里,充分反应后,最后剩余4mL气体,则原混合气体中NO的体积为
A、1mL B、3mL C、5mL D、7mL
难度: 中等查看答案及解析
-
下列物质与盐酸、NaOH均能反应的是
①NaHCO3 ②Al ③NH4HCO3 ④Al(OH)3 ⑤NaHSO4 ⑥Si
A.①②③④ B.②③⑤⑥ C.②③⑤ D.②③④⑤⑥
难度: 简单查看答案及解析
-
下面不能由单质直接化合而得到的化合物是
A.FeS B.Al2S3 C.FeCl2 D.Fe3O4
难度: 简单查看答案及解析
-
下列说法不正确的是
A.凡是铵盐均能与苛性钠共热产生氨气
B.向铜粉中加人稀硫酸,铜粉不溶解,再加入Cu(NO3)2固体,铜粉溶解
C.普通玻璃是由纯碱、石灰石和石英砂制成的,其熔点很高
D.将二氧化硫通人溴水,溴水褪色后加热不能恢复原色
难度: 中等查看答案及解析
-
下列推断正确的是
A.SiO2 是酸性氧化物,能与NaOH溶液反应,是制光导纤维的主要原料。
B.Na2O、Na2O2组成元素相同,与 CO2反应产物也相同
C.CO、NO、NO2都是大气污染气体,在空气中都能稳定存在
D.新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色
难度: 中等查看答案及解析
-
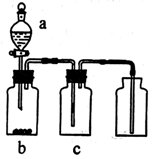
下列实验装置、选用的试剂或实验操作中,都正确的是

A.实验室用装置A制取氨气 B.用B装置吸收氨气,并防止倒吸
C.用C装置稀释浓硫酸 D.用D装置除去CO2中的HCl
难度: 中等查看答案及解析
-
在稀硫酸中加入铜粉,铜粉不溶解,再加入下列固体粉末:①FeCl2 ②Fe2O3 ③Zn ④KNO3,铜粉可溶解的是
A.①② B.②④ C.②③ D.①④
难度: 中等查看答案及解析
-
下列实验过程中,始终无明显现象的是
A.NO2通入FeSO4溶液中 B.CO2通入CaCl2溶液中
C.NH3通入AlCl3溶液中 D.SO2通入已酸化的Ba(NO3)2溶液
中
难度: 中等查看答案及解析
-
下列不属于铵盐共同性质的是
A.易溶于水 B.跟苛性钠共热生成NH3
C.都是晶体 D.受热分解都能生成NH3
难度: 简单查看答案及解析
-
同周期的X、Y、Z三元素,它们最高价氧化物对应水化物是HXO4、H2YO4、H3ZO4 ,则下列判断正确的是
A.含氧酸的酸性H3ZO4>H2YO4>HXO4
B.非金属性X>Y>Z
C.元素的负化合价的绝对值按X、Y、Z变小
D.气态氢化物的稳定性按X、Y、Z的顺序增强
难度: 中等查看答案及解析
-
短周期元素X、Y、Z在周期表中的位置关系如图所示,已知X最外层电子数为2,则下列叙述中正确的是
A.Z一定是活泼的金属元素
B.Y的最高价氧化物的水化物是一种强酸
C.1molX的单质跟足量水反应时,发生转移的电子为2mol
D.Y的氢化物稳定性大于Z的氢化物稳定性
难度: 中等查看答案及解析
-
38.4毫克铜跟适量的浓硝酸反应,铜全部作用后共收集到气体22.4毫升(标准状况),反应消耗的HNO3的物质的量可能是
A.1.0×10-3摩尔 B.1.6×10-3摩尔
C.2.2×10-3摩尔 D.2.0×10-3摩尔
难度: 中等查看答案及解析
-
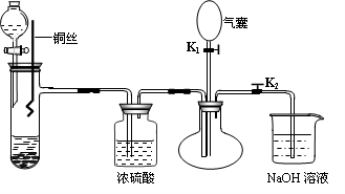
用右图装置制取、提纯并收集表中的四种气体(a、b、c表示相应仪器中加入的试剂),其中可行的是
气体
a
b
C
A
NO2
浓硝酸
铜片
NaOH溶液
B
SO2
浓硫酸
铜片
酸性高锰酸钾溶液
C
NH3
浓氨水
生石灰
碱石灰
D
CO2
稀盐酸
石灰石
浓硫酸
难度: 困难查看答案及解析
-
把含硫酸铵和硝酸铵的混合液a L分成两等份。一份加入bmol NaOH并加热,恰好把NH3全部赶出;另一份需消耗cmol BaCl2沉淀反应恰好完全,则原溶液中NO3- 的浓度为
A.
B.
C.
D.
难度: 中等查看答案及解析