-
下图所示的实验操作,不能达到相应目的的是
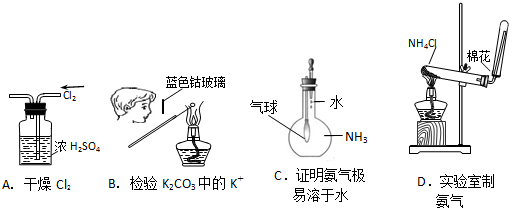
难度: 简单查看答案及解析
-
下列材料最不适宜储运浓硫酸、浓硝酸的是
A.铁 B.铜 C.陶瓷 D.铝
难度: 简单查看答案及解析
-
既有离子键又有共价键的化合物是
A.Na2O B.MgCl2 C.H2SO4 D.NH4Cl
难度: 简单查看答案及解析
-
下列有关原子结构和元素周期律的表述正确的是
①原子序数为15的元素的最高化合价为+3 ②ⅦA族元素是同周期中非金属性最强的元素 ③第二周期ⅣA族元素的原子核电荷数和中子数一定为6 ④原子序数为12的元素位于元素周期表的第三周期ⅡA族
A.①② B.①③ C.②④ D.③④
难度: 简单查看答案及解析
-
下列表示物质结构的化学用语或模型正确的是
A.8个中子的碳原子的符号:14C B.N2的电子式∶N∶∶∶N∶
C.Cl-离子的结构示意图:
D.HF的电子式:H+
难度: 简单查看答案及解析
-
如图所示是元素周期表的一部分,关于元素X、Y、Z的叙述正确的是
①X的气态氢化物与Y的最高价氧化物对应的水化物能发生反应生成盐。②Y、Z的气态氢化物的水溶液的酸性:Y<Z。③Z的单质在常温下是液体,可与铁粉反应。④Z的原子序数比Y的大19。⑤Z所在的周期中含有32种元素
A.①②③④ B.①②③④⑤ C.只有③ D.只有①③⑤
难度: 简单查看答案及解析
-
下列递变规律正确的是
A.HClO4、H2SO4、H3PO4的酸性依次增强 B.HCl、HBr 、HI的稳定性依次增强
C.钠、镁、铝的金属性依次减弱 D.N、O、F原子半径逐渐增大
难度: 简单查看答案及解析
-
一定条件下,将等体积NO和O2充入一试管,并将试管倒立于水槽中,充分反应后剩余气体的体积约为原总体积的
A.1/8 B.1/4 C.3/8 D.3/4
难度: 简单查看答案及解析
-
已知气体的摩尔质量越小,扩散速度越快。下图所示为气体扩散速度的实验,两种气体扩散相遇时形成白色烟环。下列关于甲、乙的判断正确的是
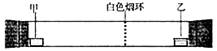
A.甲是浓氨水,乙是浓硫酸 B.甲是浓盐酸,乙是浓氨水
C.甲是浓氨水,乙是浓盐酸 D.甲是浓硝酸,乙是浓氨水
难度: 简单查看答案及解析
-
下列各组离子,在强碱性溶液中可以大量共存的是
A.K+、Na+、HSO3-、C1- B.Na+、Ba2+、A1O2-、NO3-
C.NH4+、K+、Cl-、NO3- D.K+、Na+、ClO-、S2-
难度: 简单查看答案及解析
-
能正确表示下列反应的离子方程式是
A. 向次氯酸钙溶液通入过量CO2:Ca2++2ClO-+CO2+H2O =CaCO3↓+2HClO
B. 在氯化亚铁溶液中加入稀硝酸:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O
C. 氢氧化钙溶液与碳酸氢镁溶液反应:HCO3-+Ca2++OH-=CaCO3↓+H2O
D. 向次氯酸钙溶液通入SO2:Ca2++2ClO-+SO2+H2O= CaSO3↓+2HClO
难度: 简单查看答案及解析
-
下列说法正确的是
A.全部由非金属元素组成的化合物一定是共价化合物
B.含有共价键的化合物不一定是共价化合物
C.由共价键形成的分子一定是共价化合物
D.硫酸分子中有H+和SO42-两种离子
难度: 简单查看答案及解析
-
某主族元素R的原子其电子式可用
表示。该元素组成的以下物质,其分子式肯定错误的是
A.最高价氧化物分子式为R2O5 B.含氧酸分子式为 HRO3
C.含氧酸分子式为H3RO4 D.气态氢化物分子式为RH5
难度: 简单查看答案及解析
-
在100mL某混合溶液中,c(HNO3)=0.4 mo/lL、c(H2SO4)=0.1 mol/L,向其中加入1.92gCu粉,微热充分反应后溶液中的c(Cu2+)为
A.0.15mol/L B.0.225mo1/L C.0.3mo1/L D.无法计算
难度: 简单查看答案及解析
-
将11.2g的Mg—Cu混合物完全溶解于足量的硝酸中,收集反应产生的x气体。再向所得溶液中加入适量的NaOH溶液,产生21.4g沉淀。根据题意推断气体x的成分可能是
A.0.3mol NO2 和0.3mol NO B.0.2mol NO2和0.1mol N2O4
C.0.1mol NO、0.2mol NO2和0.05mol N2O4 D.0.6mol NO
难度: 简单查看答案及解析
-
已知1~18号元素的离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,则下列叙述或表示方法正确的是
A.四种元素位于同一周期 B.氢化物的稳定性H2Y>HZ
C.离子的氧化性aW3+>bX+ D.a+3=c-2
难度: 简单查看答案及解析
-
已知a、b分别为同周期的ⅠA和ⅦA族的两种元素,它们的原子序数分别为m和n,则下列关系不可能成立的是
A.n=m+16 B.n=m+6 C.n=m+30 D.n=m+10
难度: 简单查看答案及解析
-
关于元素性质或特点的说法正确的是
A.最外层电子数≥4的元素均为非金属元素,
B.最外层电子数=2的元素均为第ⅡA族元素,
C.第m主族的非金属元素X的气态氢化物化学式为HmX,
D.在元素周期表中金属和非金属元素分界处可以找到半导体材料。
难度: 简单查看答案及解析
-
下图是元素周期表的一部分,关于图中阴影部分元素的说法中,正确的是
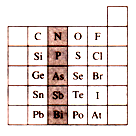
A.N元素为第一周期元素
B.PH3的稳定性比H2S强
C.该纵行元素的最高价氧化物对应的水化物化学式均为H3RO4
D.H3AsO4的酸性比H3PO4弱
难度: 简单查看答案及解析
-
已知Cu(NO3)2受热分解的化学反应方程式为:2Cu(NO3)2
2CuO+4NO2↑+O2↑,某人将少量的Cu(NO3)2固体放入试管中加热,然后用带火星的木条放入试管中,木条复燃,则下列说法正确的是:
A.NO2能支持燃烧
B.NO2不能支持燃烧
C.木条复燃是因为硝酸铜分解产生了氧气的缘故
D.木条复燃是因为硝酸铜分解产生的CuO催化作用的结果
难度: 简单查看答案及解析
-
分别处于第二、三周期的主族元素A和B,它们的离子的电子层相差2层。已知A处于第m族;B处于第n族;A只有正化合价。则A、B原子核外电子总数分别为
A、m、n B、3、7 C、m-2、10n D、m+2、n+10
难度: 简单查看答案及解析
-
已知A、B、C、D、E是核电荷数依次增大的五种短周期元素,原子半径按D、E、B、C、A顺序依次减小,B和E同主族,下列推断不正确的是
A.A、B、E一定在不同周期
B.C的最高价氧化物的水化物可能显碱性
C.C和D的单质可能化合形成离子化合物
D.A、D可能在同一主族
难度: 简单查看答案及解析