-
下列叙述正确的是( )
A. 1mol任何物质都含有6.02×1023个原子
B. 0.012kg12C含有约6.02×1023个碳原子
C. 硫酸的摩尔质量是98g
D. 常温常压下,1mol氧气的体积为22.4L
难度: 简单查看答案及解析
-
实验是研究化学的基础,下图中所示的实验方法、装置或操作完全正确的是( )
A.
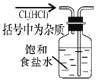 除杂 B.
除杂 B. 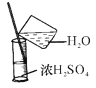 稀释
稀释C.
 制气 D.
制气 D. 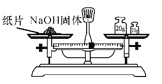 称量
称量难度: 简单查看答案及解析
-
下列反应的离子方程式书写正确的是
A.Cu与浓硝酸的反应:Cu+2H+=Cu2++H2↑
B.FeCl2溶液与Cl2的反应:Fe2++Cl2=Fe3++2Cl—
C.H2SO4溶液与KOH溶液的反应:H++OH—=H2O
D.CuCl2溶液与NaOH溶液的反应:CuCl2+2OH—=Cu(OH)2↓+2Cl—
难度: 中等查看答案及解析
-
下列各组离子,在无色透明的强酸性溶液中,能大量共存的是( )
A. Cu2+、OH- 、NO3- B. Fe3+、Cl-、SO42-
C. K+、Cl-、HCO3- D. Na+、Mg2+、SO42-
难度: 简单查看答案及解析
-
下列反应中,属于氧化还原反应的是( )
A. NaOH+HCl= NaCl+H2O B. SO3+H2O= H2SO4
C. SiO2+2NaOH=Na2SiO3+H2O D. 3NO2+H2O= 2HNO3+NO
难度: 简单查看答案及解析
-
在生物科技领域,通过追踪植物中放射性
发出的射线,来确定磷在植物中的作用部位。该核素原子内的中子数为( )
A. 15 B. 17 C. 32 D. 47
难度: 简单查看答案及解析
-
根据元素周期律判断,下列物质的性质比较,正确的是 ( )
A. 酸性:H2SO4>HClO4 B. 碱性:NaOH>KOH
C. 非金属性: P>S>Cl D. 气态氢化物稳定性:HF>HCl>H2S
难度: 简单查看答案及解析
-
下列物质只含有离子键的是( )
A. Br2 B. CO2 C. KCl D. NaOH
难度: 简单查看答案及解析
-
有关化学用语正确的是( )
A. 乙烯的最简式C2H4
B. 乙醇的结构简式C2H6O
C. 四氯化碳的电子式
D. 臭氧的分子式O3
难度: 简单查看答案及解析
-
下列说法中正确的是( )
A. 化学反应中的能量变化都表现为热量的变化
B. 需要加热才能发生的反应一定是吸热反应
C. 放热反应在常温下一定很容易发生
D. 反应物的总能量高于生成物的总能量的反应是放热反应
难度: 简单查看答案及解析
-
已知2SO2(g)+O2(g)
2SO3(g)(正反应放热)。若在500℃和催化剂的作用下,该反应在容积固定的密闭容器中进行,下列有关说法正确的是 ( )
A. 若降低温度,可以加快反应速率 B. 使用催化剂是为了加快反应速率
C. 在上述条件下,SO2能完全转化为SO3 D. 达到平衡时,SO2和SO3的浓度一定相等
难度: 中等查看答案及解析
-
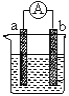
关于如图所示装置的说法中,正确的是( )
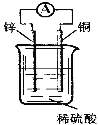
A. 铜片上发生氧化反应
B. 电子由铜片通过导线流向锌片
C. 该装置能将化学能转化为电能
D. 锌片是该装置的正极,该电极反应为Zn+2e—==Zn2+
难度: 简单查看答案及解析
-
可以用分液漏斗进行分离的混合物是( )
A. 苯和水 B. 酒精和碘水 C. 乙酸和乙醇 D. 乙酸和水
难度: 简单查看答案及解析
-
下列反应中不属于取代反应的是( )
A. 苯的硝化反应 B. 乙烯使溴水褪色
C. 苯在铁粉存在下与液溴的反应 D. 乙醇与乙酸发生酯化反应
难度: 简单查看答案及解析
-
在实验室可用如图所示装置制取少量乙酸乙酯。有关叙述不正确的是( )
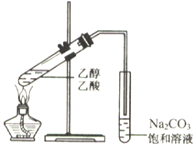
A. 长导管起冷凝、导气的作用
B. 用蒸馏法从所得混合溶液中分离出乙酸乙酯
C. Na2CO3饱和溶液的作用之一是吸收未反应的乙酸
D. 导管末端不插入饱和Na2CO3溶液中是为了防倒吸
难度: 简单查看答案及解析
-
为了维持生命和健康,人要从食物中摄取营养素,下列物质中不属于营养素的是( )
A. 葡萄糖 B. 蛋白质 C. 乙醇 D. 芝麻油
难度: 简单查看答案及解析
-
下列冶炼方法中,不能将化合物中的金属元素还原为金属单质的是( )
A. 氢气通入CuO并加热 B. 加热HgO
C. 电解NaCl溶液 D. 铝粉和Fe2O3共热
难度: 简单查看答案及解析
-
海水是一个巨大的化学资源宝库,下列有关海水综合利用的说法正确的是( )
A. 海水中含有钾元素,只需经过物理变化就可以得到钾单质
B. 海水制盐的过程中只发生了化学变化
C. 从海水中可以得到NaCl,电解熔融NaCl可制备Na
D. 利用潮汐发电是将化学能转化为电能
难度: 简单查看答案及解析
-
下列有关石油和煤的利用叙述不正确的是( )
A. 煤的干馏就是将煤隔绝空气在高温条件下使之分解,得到焦炭、煤焦油等物质的过程
B. 煤的液化就是将煤转化成甲醇、乙醇等其液态物质的过程
C. 煤的气化就是将煤在高温条件下由固态转化为气态的物理变化过程
D. 石油通过裂化和裂解,可以得到短链的烯烃和烷烃
难度: 简单查看答案及解析
-
下列实验现象或结论错误的是( )
A. 向某溶液中加入稀盐酸,无明显现象,再加BaCl2溶液,有白色沉淀生成,则原溶液中一定含有SO42-
B. 取某溶液进行焰色反应,透过蓝色钴玻璃火焰呈紫色,则原溶液中一定只含有K+
C. 向AlCl3溶液中逐滴加入NaOH溶液至过量,现象是先产生白色沉淀,后沉淀逐渐溶解
D. 向某溶液中加入NaOH溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝,则原溶液中一定含有NH4+
难度: 简单查看答案及解析