-
能使水的电离平衡右移,且水溶液显碱性的离子是( )
A.H+ B.OH- C.Al3+ D.HCO3-
难度: 简单查看答案及解析
-
某学生用碱式滴定管量取0.1 mol•L-1的NaOH溶液,开始时仰视液面读数为1.00mL,取出部分溶液后,俯视液面,读数为11.00mL,该同学在操作中实际取出的液体体积为( )
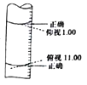
A.大于10.00mL B.小于10.00mL
C.等于10.00mL D.不能确定
难度: 简单查看答案及解析
-
对滴有酚酞试液的下列溶液,操作后颜色变深的是( )
A.明矾溶液加热
B.CH3COONa溶液加热
C.氨水中加入少量NH4Cl固体
D.小苏打溶液中加入少量NaCl固体
难度: 中等查看答案及解析
-
室温下,向10mL0.1 mol•L-1醋酸溶液中加水稀释后,下列说法正确的是( )
A.溶液中导电粒子的数目减少
B.再加CH3COONa固体促进醋酸的电离
C.醋酸的电离程度增大,c(H+)亦增大
D.溶液中
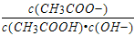 不变
不变难度: 中等查看答案及解析
-
下列四种溶液中,水的电离程度最大的是( )
A.pH=5的NH4Cl溶液 B.pH=5的NaHSO4溶液
C.pH=8的CH3COONa溶液 D.pH=8的NaOH溶液
难度: 中等查看答案及解析
-
下列水溶液一定呈中性的是( )
A.c(NH4+)=c(Cl-)的NH4Cl和氨水的混合溶液
B.c(H+)=1.0×10-7mol•L-1的溶液
C.pH=7的溶液
D.室温下将pH=3的酸与pH=11的碱等体积混合后的溶液
难度: 中等查看答案及解析
-
在25℃时,AgCl的白色悬浊液中,依次加入等浓度的KI溶液和Na2S溶液,观察到的现象是先出现黄色沉淀,最终出现黑色沉淀。已知有关物质的溶度积Ksp(25℃)如下:
AgCl
AgI
Ag2S
Ksp
1.8×10-10
8.51×10-16
6.3×10-50
下列叙述错误的是( )
A.沉淀转化的实质就是沉淀溶解平衡的移动
B.溶解度小的沉淀可以转化为溶解度更小的沉淀
C.AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶解程度相同
D.25℃时,在饱和AgCl、AgI、Ag2S溶液中,所含Ag+的浓度不同
难度: 中等查看答案及解析
-
下列关于电解质溶液的叙述正确的是( )
A.常温下,在pH=7的醋酸钠和醋酸混合溶液中:c(CH3COO-)>c(Na+)
B.稀释醋酸溶液,溶液中所有离子的浓度均降低
C.在pH=5的氯化钠和稀硝酸的混合溶液中,c(Na+)=c(Cl-)
D.0.1mol•L-1的硫化钠溶液中,c(OH-)=c(H+)+c(HS-)+c(H2S)
难度: 中等查看答案及解析
-
某同学做完Zn-Cu-H2SO4组成的原电池的实验后,在读书卡片上作了如下记录,其中合理的是( )
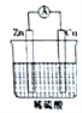

A.①②③ B.④⑤⑥ C.③④⑤ D.②③⑥
难度: 简单查看答案及解析
-
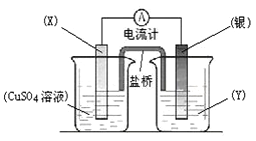
如下图所示装置中,观察到电流计指针偏转,M棒变粗,N棒变细,由此判断下表中所列M、N、P物质,其中可以成立的是( )
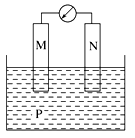
M
N
P
A
Zn
Cu
稀硫酸溶液
B
Cu
Fe
稀盐酸溶液
C
Ag
Zn
硝酸银溶液
D
Zn
Fe
硝酸铁溶液
难度: 简单查看答案及解析
-
纽扣电池可用于计算器、电子表等的电源。有一种纽扣电池,其电极分别为Zn和Ag2O,以KOH溶液为电解质溶液,电池的总反应为Zn+Ag2O=2Ag+ZnO。关于该电池的叙述不正确的是( )

A.作用时电子由Zn极经外电路流向Ag2O极,Zn是负极
B.使用时电子由Ag2O极经外电路流向Zn极,Ag2O是负极
C.正极的电极反应为Ag2O+2e-+H2O=2Ag+2OH-
D.Zn极发生氧化反应,Ag2O极发生还原反应
难度: 中等查看答案及解析
-
银锌电池广泛用作各种电子仪器的电源,它的充电和放电过程可表示为:2Ag+Zn(OH)2
Ag2O+Zn+H2O,在此电池放电时,负极上发生反应的物质是( )
A.Ag B.Zn(OH)2 C.Ag2O D.Zn
难度: 中等查看答案及解析
-
一种充电电池放电时的电极反应为H2+2OH--2e-=2H2O;NiO(OH)+H2O+e-=Ni(OH)2+OH-当为电池充电时,与外电源正极相连接的电极上发生的反应是( )
A.H2O的还原 B.NiO(OH)的还原
C.H2的氧化 D.Ni(OH)2的氧化
难度: 中等查看答案及解析
-
下图是电解CuCl2溶液的装置,其中c、d为石墨电极,则以下有关此电解池的判断正确的是( )
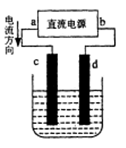
A.a为负极、b为正极
B.a为阳极、b为阴极
C.电解过程中,d电极质量增加
D.电解过程中,氯离子浓度不变
难度: 中等查看答案及解析
-
用石墨作电极,电解1 mol•L-1下列物质的溶液,则电解前后溶液的pH保持不变的是( )
A.H2SO4 B.NaOH C.Na2SO4 D.NaCl
难度: 中等查看答案及解析
-
下列关于铜电极的叙述中,正确的是( )
A.电解稀硫酸制H2、O2时铜作阳极
B.用电解法精炼粗铜时粗铜作阴极
C.在镀件上电镀铜时用金属铜作阴极
D.铜锌原电池中铜是正极
难度: 中等查看答案及解析
-
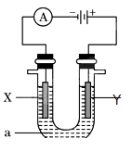
下图装置中,U形管内为红墨水,a、b试管内分别盛有食盐水和氯化铵溶液,各加入生铁块,放置一段时间,下列有关描述错误的是( )
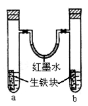
A.生铁块中的碳是原电池的正极
B.红墨水柱两边的液面变为左低右高
C.两试管中相同的电极反应式是:Fe-2e-=Fe2+
D.a试管中发生了吸氧腐蚀,b试管中发生了析氢腐蚀
难度: 困难查看答案及解析
-
关于电解饱和NaCl水溶液,下列叙述正确的是( )
A.电解时在阳极得到氯气,在阴极得到金属钠
B.若在阳极附近的溶液中滴入KI溶液,溶液呈棕色
C.若在阴极附近的溶液中滴入酚酞试液,溶液呈无色
D.电解一段时间后,将全部电解液转移到烧杯中,充分搅拌后溶液呈中性
难度: 中等查看答案及解析
-
下列有关惰性电极电解AgNO3溶液一段时间后的说法,正确的是( )
A.电解过程中阴极质量不变
B.电解过程中溶液的pH不断升高
C.此时向溶液中加入适量的Ag2O固体可使溶液恢复电解前的状况
D.电解后两极产生的气体体积比为2:1
难度: 简单查看答案及解析
-
电解CuCl2溶液时,如果阴极上有1.6g铜析出,则阳极上产生气体的体积(标准状况)约为( )
A.0.28 L B.0.56 L C.0.14 L D.11.2 L
难度: 简单查看答案及解析