-
在盛放浓硫酸的试剂瓶上应印有如下图所示警示标记中的( )
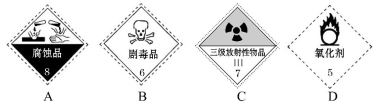
难度: 简单查看答案及解析
-
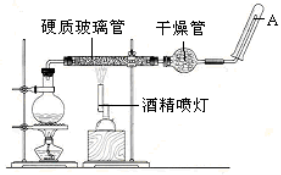
下列实验基本操作(或注意事项)中,主要是从实验安全考虑的是( )
A.实验剩余的药品一般不能放回原试剂瓶
B.可燃性气体的验纯
C.气体实验装置在实验前进行气密性检查
D.滴管不能交叉使用
难度: 中等查看答案及解析
-
已知甲和乙的某些性质如下表所示:
物质
熔点(℃)
沸点(℃)
密度(g·mL-1)
在水中的溶解性
甲
-98
37. 5
0.93
可溶
乙
-48
95
0.90
可溶
现有甲和乙的混合物,进行分离时,可采用的方法是( )
A.蒸馏 B.蒸发 C.过滤 D.萃取
难度: 中等查看答案及解析
-
能够直接鉴别BaCl2、NaCl、Na2CO3三种溶液的试剂是( )
A.AgNO3溶液 B.稀硫酸 C.稀盐酸 D.稀硝酸
难度: 中等查看答案及解析
-
下列叙述中正确的是( )
A.1 mol氢的质量是1 g
B.1 mol CO的质量为28 g·mol-1
C.阿伏加德罗常数等于6.02×1023
D.3.01×1023个SO2分子约是0.5 mol
难度: 中等查看答案及解析
-
下列物质中所含分子物质的量最多的是( )
A.44 g CO2 B.1.5 mol H2
C.64 g SO2 D.3.01×1023个硫酸分子
难度: 中等查看答案及解析
-
下列说法正确的是( )
A.在标准状况下,1 mol水的体积是22.4 L
B.1 mol H2所占的体积约为22.4 L
C.在标准状况下, 阿伏加德罗常数个分子所占的体积约为22.4 L
D.在标准状况下,1 mol NH3和CO混合气体所占的体积约为22.4 L
难度: 中等查看答案及解析
-
下列溶液中,Na+的物质的量浓度最大的是( )
A.1 mL 0.5 mol·L-1的NaNO3溶液 B.100 mL 0.01 mol·L-1的NaCl溶液
C.100 mL 0.1 mol·L-1的NaOH溶液 D.10 mL 0.1 mol·L-1的Na2SO4溶液
难度: 中等查看答案及解析
-
用NA表示阿伏加德罗常数,下列关于0.2 mol·L-1K2SO4溶液的正确说法是 ( )
A.1 L溶液中K+浓度是0.4 mol·L-1
B.溶液中含有0.4NA个K+
C.1 L溶液中所含K+、SO42-总数为0.3NA
D.2 L溶液中SO42-浓度是0.4 mol·L-1
难度: 中等查看答案及解析
-
下列物质不可能由一种元素组成的是( )
A.单质 B.混合物 C.氧化物 D.纯净物
难度: 简单查看答案及解析
-
分类是学习和研究化学的一种重要方法,下列分类合理的是( )
A.K2CO3和K2O都属于盐 B.KOH和Na2CO3都属于碱
C.H2SO4和HNO3都属于酸 D.Na2O和Na2SiO3都属于氧化物
难度: 中等查看答案及解析
-
下列实验操作中,正确的是( )
A.利用丁达尔效应可以区分溶液和胶体
B.用滤纸过滤可以除去溶液中的胶体粒子
C.向氢氧化钠溶液中边滴加饱和FeCl3溶液边振荡制备Fe(OH)3胶体
D.向Fe(OH)3胶体加入足量稀盐酸后,依然有丁达尔现象
难度: 简单查看答案及解析
-
下列叙述正确的是( )
A.固态氯化钾不导电,所以氯化钾不是电解质
B.石墨能导电,所以石墨是电解质
C.硫酸溶液能导电,所以硫酸是电解质
D.CO2溶于水能导电,所以CO2是电解质
难度: 中等查看答案及解析
-
下列两种物质的溶液混合后不能发生离子反应的是( )
A.HNO3和Na2CO3 B.NaCl和AgNO3
C.K2SO4和BaCl2 D.HNO3和BaCl2
难度: 中等查看答案及解析
-
下列化学反应,能用离子方程式H++OH-=H2O表示的是( )
A.澄清石灰水与盐酸反应 B.氢氧化钡溶液和稀硫酸反应
C.氢氧化镁和稀硝酸反应 D.氢氧化铁溶液与盐酸反应
难度: 中等查看答案及解析
-
下列各组中的离子,能在溶液中大量共存的是( )
A.K+、H+、SO42-、OH- B.Na+、K+、CO32-、NO3-
C.Na+、H+、Cl-、CO32- D.K+、Cu2+、SO42-、OH-
难度: 中等查看答案及解析
-
下列反应中,属于氧化还原反应的是( )
A.SO2+2KOH=K2SO3+H2O
B.CaCO3
CaO+CO2↑
C.Na2CO3+CaCl2=CaCO3↓+2NaCl
D.Fe+2FeCl3=3FeCl2
难度: 简单查看答案及解析
-
离子反应、复分解反应、置换反应和氧化还原反应之间可用集合关系表示,正确的是( )
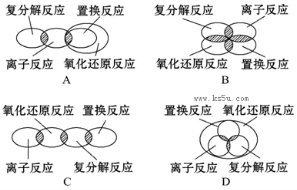
难度: 简单查看答案及解析
-
下列反应中必须加入氧化剂才能进行的是( )
A.Cl2→Cl- B.Zn2+→Zn C.H2→H2O D.CuO→CuCl2
难度: 中等查看答案及解析
-
下列有关钠的物理性质的叙述中正确的是( )
①银白色金属 ②质软,可以用小刀切割 ③熔点低
④密度比水小 ⑤热和电的良导体
①②④ B.①②③④ C.①③④ D.①②③④⑤
难度: 中等查看答案及解析
-
称取两份铝粉,第一份加入足量的盐酸,第二份加入足量的烧碱。若同温同压下放出相同体积的气体,则两份铝粉的质量比为( )
A.1:1 B.2:3 C.3:2 D.1:6
难度: 中等查看答案及解析
-
下列反应的离子方程式书写正确的是( )
A.钠和冷水反应Na+2H2O=Na++2OH-+H2↑
B.金属铝溶于氢氧化钠溶液Al+2OH-=AlO2-+H2↑
C.金属铝溶于盐酸中2Al+6H+=2Al3++3H2↑
D.铁跟稀硫酸反应2Fe+6H+=2Fe3++3H2↑
难度: 中等查看答案及解析