-
2015年12月上合组织峰会期间河南采取了多种措施保护环境、避免污染。下列气体排放到空气中,不会造成大气污染的是
A. SO2 B. NO C. O2 D. CO
难度: 简单查看答案及解析
-
下列变化中,与其他变化有根本区别的一种是
A. 粮食酿酒 B. 木炭燃烧 C. 饭菜变馊 D. 冰雪消融
难度: 简单查看答案及解析
-
实验室有许多药品需要密封保存。对下列药品密封保存的原因解释不正确的是
A. 生石灰——防止氧化 B. 氢氧化钠——防止潮解和变质
C. 浓硫酸——防止吸水 D. 浓盐酸——防止挥发
难度: 中等查看答案及解析
-
下列物质转化能实现的是
A. H2SO4
HCl B. CO
Na2CO3
C. Cu(OH)2
Na2CO3 D. NaNO3
Ba(NO3)2
难度: 中等查看答案及解析
-
下列实验方法以及对应的化学方程式均正确的是
A. 用点燃的方法除去O2中的H2:H2+O2====H2O
B. 用纯碱和石灰乳制取少量的烧碱:Na2CO3+Ca(OH)2=====CaCO3↓+2NaOH
C. 用盐酸除去Na2 SO4中的Na2CO3;2HCl+Na2 CO3====2NaCl+H2O+CO2↑
D. 用铁粉除去FeSO4中的CuSO4:2Fe+3CuSO4=====Fe2(SO4)3+3Cu
难度: 中等查看答案及解析
-
镁铝合金x g和足量的盐酸反应后可生成0.1 g H2,则x可能为
A. 0.8 B. 1 C. 1.5 D. 无法确定
难度: 中等查看答案及解析
-
质量相等的锌、铝、铁分别与足量稀盐酸反应,产生氢气的质量()
A. 锌最多,铁最少 B. 铝最多,锌最少 C. 铁最多,铝最少 D. 三者一样多
难度: 困难查看答案及解析
-
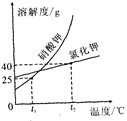
下图所示是甲、乙两种固体物质的溶解度曲线,下列说法正确的是
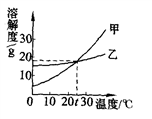
A. 甲的溶解度大于乙的溶解度
B. t℃时,甲、乙的饱和溶液中溶质的质量分数相等
C. 升高温度可以使接近饱和的甲溶液变为饱和溶液
D. 10℃时,分别用100 g水配制甲、乙的饱和溶液,所需甲的质量大于乙的质量
难度: 困难查看答案及解析
-
逻辑推理是化学学习中常用的思维方法。下列推理正确的是
A. 中和反应生成盐和水,则生成盐和水的反应一定是中和反应
B. 单质
中只含有一种元素,则只含有一种元素的物质一定是单质
C. 化合物是由不同种元素组成的纯净物,则由不同种元素组成的纯净物一定是化合物
D. 活泼金属能与稀硫酸反应放出气体,则能与稀硫酸反应放出气体的物质一定是活泼金属
难度: 困难查看答案及解析
-
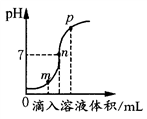
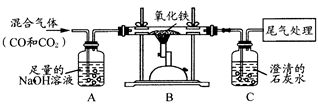
依据相关实验所作的下列图像不正确
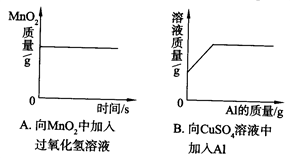
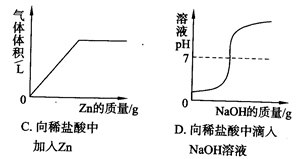
A. A B. B C. C D. D
难度: 困难查看答案及解析
-
为除去粗盐中的泥沙、CaCl2、MgCl2、Na2 SO4得到NaCl,可
将粗盐溶解于水,然后进行下列六项操作:①过滤②加适量盐酸③加过量Na2CO3溶液④加过量NaOH 液⑤加过量BaCl2溶液⑥蒸发,正确的操作顺序是
A. ①④⑤③②⑥ B. ④①③⑤②⑥ C. ⑤④③①②⑥ D. ⑤④③②①⑥
难度: 中等查看答案及解析
-
某碳酸钙和氧化钙组成的混合物中钙元素的质量分数为 60%,将50g 该混合物高温煅烧至固体质量不再改变,则生成二氧化碳的质量是
A. 6g B. 8g C. 13.2g D. 20g
难度: 简单查看答案及解析
-
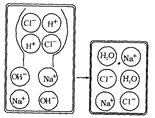
下列各组中的离子,能在溶液中大量共存的是
A. H+、K+、OH-、SO42- B. Ag+、Na+、Cl-、NO3-
C. Ca2+、Ba2+、 CO32-、NO3- D. Zn2+、Na+、SO42-、Cl-
难度: 中等查看答案及解析
-
已经调平的托盘天平两边各放一只等质量的烧杯,向杯中各加入质量相等、溶质质量分数相同的稀盐酸,然后在左边烧杯中放入镁,在右边的烧杯中放人与镁质,量相等的铝。待充分反应后,下列分析正确的是
A. 天平保持平衡,右边烧杯中,酸可能剩余,铝一定没剩余
B. 天平保持平衡,右边烧杯中,酸没有剩余,铝一定没剩余
C. 天平保持平衡,左边烧杯中,酸一定剩余,镁一定没剩余
D. 天平保持平衡,左边烧杯中,酸没有剩余,镁可能有剩余
难度: 困难查看答案及解析