-
能源是人类共同关注的重要问题。页岩气是从页岩层中开采出来的一种非常重要的天然气资源,页岩气的主要成分是甲烷,是公认的洁净能源。
(1)页岩气不仅能用作燃料,还可用于生产合成气(CO和H2)。CH4与H2O(g)通入聚焦太阳能反应器,发生反应 CH4(g)+H2O(g)=CO(g)+3H2(g)△H1
已知:①CH4、H2、CO 的燃烧热(△H)分别为-a kJ•mol-1、-b kJ•mol-1、-c kJ•mol-1;
②H2O (l) =H2O(g); △H=+dkJ•mol-1
则△H1= ___________(用含字母a、b、c、d的代数式表示)kJ•mol-1。
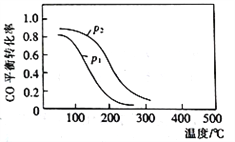
(2)用合成气生成甲醇的反应为:CO(g)+2H2(g) CH3OH(g) △H2,在10L恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如下图所示,200℃时n(H2)随时间的变化如下表所示:
CH3OH(g) △H2,在10L恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如下图所示,200℃时n(H2)随时间的变化如下表所示:
| t/min | 0 | 1 | 3 | 5 |
| n(H2)/mol | 8.0 | 5.4 | 4.0 | 4.0 |
①△H2_________ (填“>”“<”或“ = ”)0。
②下列说法正确的是____________ (填标号)。
a.温度越高,该反应的平衡常数越大
b.达平衡后再充入稀有气体,CO的转化率提高
c.容器内气体压强不再变化时,反应达到最大限度
d.图中压强p1<p2
③ 0〜3 min内用CH3OH表示的反应速率v(CH3OH)=________mol • L-1·min-1。
④ 200℃时,该反应的平衡常数K =_______。向上述200℃达到平衡的恒容密闭容器中再加入2 mol CO、2 mol H2、2 mol CH3OH,保持温度不变,则化学平衡____________(填“正向”、“逆向”或“不”)移动。
(3)甲烷、氧气和KOH溶液可组成燃料电池。标准状况下通入5.6 L甲烷,测得电路中转移1.2 mol电子,则甲烷的利用率为_________。
-
能源是人类共同关注的重要问题。页岩气是从页岩层中开采出来的一种非常重要的天然气资源,页岩气的主要成分是甲烷,是公认的洁净能源。
(1)页岩气不仅能用作燃料,还可用于生产合成气(CO和H2)。CH4与H2O(g)通入聚焦太阳能反应器,发生反应 CH4(g)+H2O(g)=CO(g)+3H2(g)△H1
已知:①CH4、H2、CO 的燃烧热(△H)分别为-a kJ•mol-1、-b kJ•mol-1、-c kJ•mol-1;
②H2O (l) =H2O(g); △H=+dkJ•mol-1
则△H1= ___________(用含字母a、b、c、d的代数式表示)kJ•mol-1。
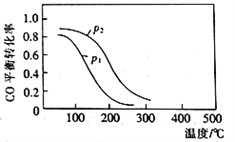
(2)用合成气生成甲醇的反应为:CO(g)+2H2(g) CH3OH(g) △H2,在10L恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如下图所示,200℃时n(H2)随时间的变化如下表所示:
CH3OH(g) △H2,在10L恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如下图所示,200℃时n(H2)随时间的变化如下表所示:
| t/min | 0 | 1 | 3 | 5 |
| n(H2)/mol | 8.0 | 5.4 | 4.0 | 4.0 |
①△H2_________ (填“>”“<”或“ = ”)0。
②下列说法正确的是____________ (填标号)。
a.温度越高,该反应的平衡常数越大
b.达平衡后再充入稀有气体,CO的转化率提高
c.容器内气体压强不再变化时,反应达到最大限度
d.图中压强p1<p2
③ 0〜3 min内用CH3OH表示的反应速率v(CH3OH)=________mol • L-1·min-1。
④ 200℃时,该反应的平衡常数K =_______。向上述200℃达到平衡的恒容密闭容器中再加入2 mol CO、2 mol H2、2 mol CH3OH,保持温度不变,则化学平衡____________(填“正向”、“逆向”或“不”)移动。
(3)甲烷、氧气和KOH溶液可组成燃料电池。标准状况下通入5.6 L甲烷,测得电路中转移1.2 mol电子,则甲烷的利用率为_________。
-
页岩气是从页岩层中开采出来的一种非常重要的天然气资源,页岩气的主要成分是甲烷,是公认的洁净能源。
(1)页岩气不仅能用作燃料,还可用于生产合成气(CO+H2)。CH4与H2O(g)通入聚焦太阳能反应器,发生反应:CH4(g)+ H2O(g)═CO(g)+3H2(g) ΔH。
已知:①CH4、H2、CO的燃烧热分别为a  、b
、b  、c
、c  (a、b、c均大于0);
(a、b、c均大于0);
②水的汽化热为+d  (d >0)。则ΔH=__________
(d >0)。则ΔH=__________ (用含a、b、c、d的代数式表示)。
(用含a、b、c、d的代数式表示)。
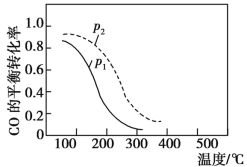
(2)用合成气制甲醇的反应为2H2(g)+CO(g) CH3OH(g) ΔH,在10 L的恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如图所示。
CH3OH(g) ΔH,在10 L的恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如图所示。
①ΔH________(填“>”“<”或“=”)0。
②写出两条可同时提高反应速率和CO的转化率的措施:_______、_____。
③下列说法正确的是___________(填序号)。
A.温度越高,该反应的平衡常数越大
B.达平衡后再充入稀有气体,CO的转化率提高
C.体系内气体压强不再变化时,反应达到平衡状态
D.图中压强p1<p2
④200 ℃时,n(H2)随时间的变化如表所示,3 min时反应刚好达到平衡状态,请利用表中的数据计算0~3 min内v(CH3OH)=_______ 。
。
| t/min | 0 | 1 | 3 | 5 |
| n(H2)/mol | 8.0 | 5.4 | 4.0 | 4.0 |
⑤200℃时该反应的平衡常数K=____________。向上述200 ℃的平衡体系中再加入2 mol CO、2 mol H2、2 mol CH3OH,保持温度不变,则平衡_______(填“正向移动”“逆向移动”或“不移动”)。
(3)甲烷、氧气和KOH溶液可组成燃料电池。标准状况下通入5.6 L甲烷时,测得电路中转移1.96 mol电子,则甲烷的利用率为________。
-
页岩气是从页岩层中开采出来的一种非常重要的天然气资源,页岩气的主要成分是甲烷,是公认的洁净能源。
(1)页岩气不仅能用作燃料,还可用于生产合成气(CO和H2)。CH4与H2O(g)通入聚焦太阳能反应器,发生反应 CH4(g) + H2O(g)==CO(g)+3H2(g) △H1
已知:
①CH4、H2、CO 的燃烧热(△H)分别为-a kJ•mol-1、-b kJ•mol-1、-c kJ•mol-1;
②H2O(l) =H2O(g) △H=+dkJ•mol-1
则△H1= ___________(用含字母a、b、c、d的代数式表示)kJ•mol-1。
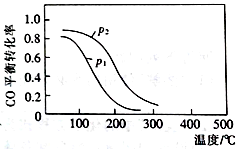
(2)用合成气生成甲醇的反应为:CO(g)+2H2(g) CH3OH(g) △H2,在10 L恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如右图所示,200℃时n(H2)随时间的变化如下表所示:
CH3OH(g) △H2,在10 L恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如右图所示,200℃时n(H2)随时间的变化如下表所示:
| t/min | 0 | 1 | 3 | 5 |
| n(H2)/mol | 8.0 | 5.4 | 4.0 | 4.0 |
①△H2_________(填“>”“<”或“ = ”)0。
②写出两条可同时提高反应速率和CO转化率的措施:________________________ 。
③下列说法正确的是____________(填标号)。
a.温度越高,该反应的平衡常数越大
b.达平衡后再充入稀有气体,CO的转化率提高
C.容器内气体压强不再变化时,反应达到最大限度
D.图中压强p12
④0〜3 min内用CH3OH表示的反应速率v(CH3OH)=_________mol • L-1·min-1。
⑤200℃时,该反应的平衡常数K =_______。向上述200℃达到平衡的恒容密闭容器中再加入2 mol CO、2 mol H2、2 mol CH3OH,保持温度不变,则化学平衡____________(填“正向”、“逆向”或“不”)移动。
(3)甲烷、氧气和KOH溶液可组成燃料电池。标准状况下通入5.6 L甲烷,测得电路中转移1.2 mol电子,则甲烷的利用率为________________。
-
页岩气是从页岩层中开采的一种非常重要的天然气资源,页岩气的主要成分是甲烷,是公认的洁净能源。
(1)页岩气不仅能用作燃料,还可用于生产合成气(CO和H2)。CH4与H2O(g)通入聚焦太阳能反应器,发生反应CH4(g)+H2O(g) = CO(g)+3H2(g) ΔH1。已知:CH4、H2、CO的燃烧热(ΔH)分别为-a kJ·mol-1、-b kJ·mol-1、-c kJ·mol-1;H2O(l)=H2O(g) ΔH=+d kJ·mol-1。
则ΔH1=______________(用含字母a、b、c、d的代数式表示)kJ·mol-1。
(2)用合成气生成甲醇的反应为CO(g)+2H2(g) CH3OH(g) ΔH2,在10 L恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如图所示:
CH3OH(g) ΔH2,在10 L恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如图所示:
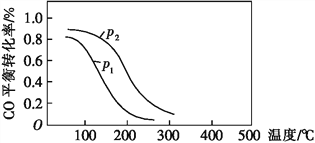
200 ℃时n(H2)随时间的变化如下表所示:
| t/min | 0 | 1 | 3 | 5 |
| n(H2)/mol | 8.0 | 5.4 | 4.0 | 4.0 |
①ΔH2____(填“>”“<”或“=”)0。
②写出两条可同时提高反应速率和CO转化率的措施:_____。
③下列说法正确的是____(填字母)。
a.温度越高,该反应的平衡常数越大
b.达平衡后再充入稀有气体,CO的转化率提高
c.容器内气体压强不再变化时,反应达到最大限度
d.图中压强:p1<p2
④0~3 min内用CH3OH表示的反应速率v(CH3OH)=____mol·L-1·min-1。
⑤200 ℃时,该反应的平衡常数K=____。向上述200 ℃达到平衡的恒容密闭容器中再加入2 mol CO、4 mol H2、2 mol CH3OH,保持温度不变,则化学平衡____(填“正向”“逆向”或“不”)移动。
(3)甲烷、氧气和KOH溶液可组成燃料电池。标准状况下充入5.6 L甲烷,测得电路中转移1.2 mol电子,则甲烷的利用率为____。
-
化学与生活、环境密切相关。下列说法不正确的是
A. 纤维素在人体内水解最终生成葡萄糖
B. 羊绒衫的主要成分是天然纤维
C. 新型能源页岩气的主要成分是甲烷
D. 用太阳能分解水制氢气可减少碳排放
-
下列说法不正确的是
A.光--电转换的途径可以不需要发生化学反应
B.天然气和沼气的主要成分都是甲烷,因此都是化石能源
C.将厨余垃圾中的油脂分离出来,可以制造肥皂和油漆等
D.人造丝、人造棉和铜氨纤维的主要化学成分都可表示为(C6H10O5)n
-
天然气既是重要的能源,也是重要的化工原料,其主要成分是甲烷。
(1)甲烷在一定条件下可生成:
A.碳正离子(CH3-) B.碳负离子(CH3-)
C.甲基(—CH3) D.碳烯( )
)
①四种微粒中,键角为120°的是________。(填序号)
②与碳负离子(CH3-)互为等电子体的一种分子的结构式为_________________________________________________________。
(2)海底富藏大量的可燃冰(甲烷的水合物),关于可燃冰的说法中正确的是________。
A.甲烷分子与水分子均是极性分子
B.可燃冰中甲烷分子与水分子间以氢键相结合
C.可燃冰属于原子晶体
D.甲烷分子与水分子中的σ键均是s—sp3电子云重叠而成的
(3)在高温下,甲烷可还原CuO得到Cu2O。
①Cu+的核外电子排布式为____________。
②Cu2O晶体的晶胞结构如图所示。其中“△”代表的离子符号为________。
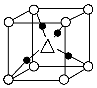
(4)一定条件下,甲烷与水蒸气可生成H2和CO。则所生成的气体中σ键总数与π键总数之比为________。
-
甲烷作为天然气、页岩气、可燃冰的主要成分,拥有最稳定的烷烃分子结构,具有高度的四面体对称性,极难在温和的条件下对其活化。因此,甲烷的选择活化和定向转化一直是世界性的难题。我国科学家经过长达6年的努力,研制成功一系列石墨烯限域的3d过渡金属中心(Mn、Fe、Co、Ni、Cu)催化剂材料,在室温条件下以H2O2为氧化剂直接将甲烷氧化成C1(只含一个C原子)含氧化合物,被业内认为是甲烷化学领域的重要突破。请回答下列问题:
(1)Cu原子基态原子的外围电子排布式为____________。
(2)石墨烯限域单原子铁能活化CH4分子中的C-H键,导致C与H之间的作用力_____(减弱”或“不变”)。铁晶体中粒子之间作用力类型是__________________。
(3)常温下,H2O2氧化CH4生成CH3OH、HCHO、 HCOOH等。
①它们的沸点分别为64.7、-195℃、100.8℃,其主要原因是_________________;
②CH4 和HCHO比较,键角较大的是_________,主要原因是_____________。
(4)配离子的颜色与d-d电子跃迁的分裂能大小有关,1个电子从较低的d轨道跃迁到较高能量的轨道所需的能量为的分裂能,用符号△表示。分裂能△[Co(H2O)62+]_____________△[Co(H2O)63+](填“>”“<”或“=”),理由是_________________。
(5)钴晶胞和白铜(铜镍合金)晶胞分别如图1、图2所示。
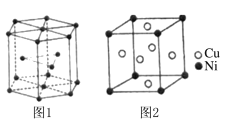
①钴晶胞堆积方式的名称为____________;
②已知白铜晶胞的密度为dg·cm-3 ,NA代表阿伏加德罗常数的值。图2晶胞中两个面心上铜原子最短核间距为_____________pm(列出计算式)。
-
天然气是一种重要的清洁能源和化工原料,其主要成分为甲烷。
 已知:
已知: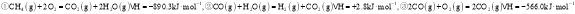 ,则反应
,则反应 ______ 。
______ 。
 天然气的一个重要用途是制取
天然气的一个重要用途是制取 ,其原理为:
,其原理为: 。一定条件下,在密闭容器中,通入物质的量浓度均为
。一定条件下,在密闭容器中,通入物质的量浓度均为 的
的 与
与 ,在发生反应时,测得
,在发生反应时,测得 的平衡转化率与温度及压强的关系如图1所示,
的平衡转化率与温度及压强的关系如图1所示,
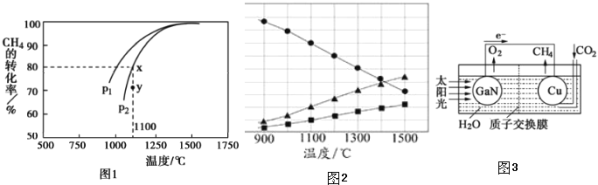
 该反应的平衡常数表达式为______ 。
该反应的平衡常数表达式为______ 。
 压强
压强 ______
______  填“大于”或“小于”
填“大于”或“小于” ;压强为
;压强为 时,在Y点:
时,在Y点: 正
正 ______
______  逆
逆 填“大于“、“小于”或“等于“
填“大于“、“小于”或“等于“ 。
。
 天然气中的少量
天然气中的少量 杂质常用氨水吸收,产物为
杂质常用氨水吸收,产物为 。一定条件下向
。一定条件下向 溶液中通入空气,得到单质硫并使吸收液再生,写出再生反应的化学方程式为______ 。
溶液中通入空气,得到单质硫并使吸收液再生,写出再生反应的化学方程式为______ 。
 工业上又常将从天然气分离出的
工业上又常将从天然气分离出的 ,在高温下分解生成硫蒸气和
,在高温下分解生成硫蒸气和 ,若反应在不同温度下达到平衡时,混合气体中各组分的体积分数如图2所示,
,若反应在不同温度下达到平衡时,混合气体中各组分的体积分数如图2所示, 在高温下分解反应的化学方程式为______ 。
在高温下分解反应的化学方程式为______ 。
 科学家用氮化镓材料与铜组装如图3的人工光合系统,利用该装置成功地实现了以
科学家用氮化镓材料与铜组装如图3的人工光合系统,利用该装置成功地实现了以 和
和 合成
合成 。
。
 写出铜电极表面的电极反应式为______ 。
写出铜电极表面的电极反应式为______ 。
 为提高该人工光合系统的工作效率,可向装置中加入少量______
为提高该人工光合系统的工作效率,可向装置中加入少量______  选填“盐酸”或“硫酸”
选填“盐酸”或“硫酸” 。
。
、b
、c
(a、b、c均大于0);
(d >0)。则ΔH=__________
(用含a、b、c、d的代数式表示)。
CH3OH(g) ΔH,在10 L的恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如图所示。

。






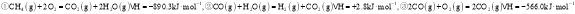 ,则反应
,则反应