-
某学习小组探究SO2与Cu(OH)2悬浊液的反应。
实验Ⅰ:向NaOH溶液中加入浓CuCl2溶液,制得含Cu(OH)2的悬浊液,测溶液pH≈13。向悬浊液中通入SO2,产生大量白色沉淀,测溶液pH≈3。推测白色沉淀中可能含有Cu+、Cu2+、Cl- 、SO42-、SO32-、HSO3-。
已知: i. Cu(NH3)42+(蓝色);Cu+ Cu(NH3)2+(无色);Cu+
Cu(NH3)2+(无色);Cu+ Cu+Cu2+
Cu+Cu2+
ii. Ag2SO4微溶于水,可溶于一定浓度的硝酸。
实验Ⅱ:
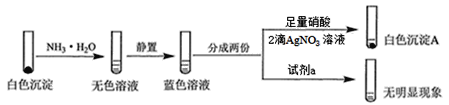
(1)①通过“白色沉淀A”确定一定存在的离子是____________________。
②判断白色沉淀中金属离子仅含有Cu+、不含Cu2+的实验证据是____________________。
③用以证实白色沉淀中无SO42-、SO32-、HSO3-的试剂a是____________________。
④生成CuCl的离子方程式是____________________。
(2)小组同学基于上述实验认为: SO2与Cu(OH)2悬浊液能发生氧化还原反应不仅基于本身的性质,还受到“生成了沉淀促进了氧化还原反应的发生”的影响。设计实验验证了此观点。
①用实验Ⅰ方法制得含Cu(OH)2的悬浊液,过滤、洗涤获取纯净的Cu(OH)2固体。检验Cu(OH)2固体是否洗涤干净的方法是____________________。
| 编号 | 实验 | 现象 |
| III | 向Cu(OH)2固体中加入一定量的水,制得悬浊液(pH≈8),向悬浊液中通入SO2 | a. 底部产生少量浅黄色沉淀,慢慢消失 b. 静置,底部产生少量红色固体 |
| IV | 向CuSO4溶液中通入SO2 | 无沉淀产生 |
②经确认浅黄色沉淀是CuOH,红色固体是Cu,证明SO2与Cu(OH)2悬浊液发生了氧化还原反应。最终生成Cu的原因是____________________。
③由实验III、IV可以得出的结论除“生成了沉淀促进了氧化还原反应的发生” 外还有____________________。
-
某实验小组探究SO2与Cu(OH)2悬浊液的反应。
(1)实验一:用如图装置(夹持装置已略,气密性已检验)制备SO2,将SO2通入Cu(OH)2悬浊液的反应中。B中出现少量红色沉淀;稍后,B中所得溶液呈绿色,与CuSO4溶液、CuCl2溶液的颜色有明显不同。
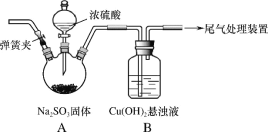
①排除装置中的空气,避免空气对反应干扰的操作是_____,关闭弹簧夹。
②打开分液漏斗旋塞,A中发生反应的方程式是_____。
(2)实验二:为确定红色固体成分,进行以下实验:
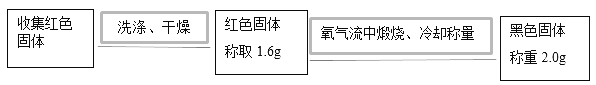
①在氧气流中煅烧红色固体的目的是_____。
②根据上述实验可得结论:该红色固体为_____。
(3)实验三:为探究B中溶液呈绿色而不是蓝色的原因,实验如下:
i.向4mL1mol/L的CuSO4溶液中通入过量SO2,未见溶液颜色发生变化。
ii.取少量B中滤液,加入少量稀盐酸,产生无色刺激性气味的气体,得到澄清的蓝色溶液。再加入BaCl2溶液,出现白色沉淀。
查阅资料:SO2在酸性条件下还原性较差。
①实验i的目的_____。
②根据上述实验可得结论:溶液显绿色的原因是溶液中含有较多Cu(HSO3)2。小组同学通过进一步实验确认了这种可能性,在少量1mol/L的CuSO4溶液中加入_____溶液,得到绿色溶液。
(4)综上实验可以得出:出现红色沉淀的原因是:_____;(用离子方程式表示)溶液呈现绿色的原因是:_____。(用化学方程式表示)
-
(15分)
某校兴趣小组对SO2与新制Cu(OH)2悬浊液的反应进行探究,实验如下:
| 装置 | 序号 | 试管中的药品 | 现象 |
| 持续通入 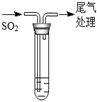
| 实验Ⅰ | 1.5 mL 1 mol·L-1 CuSO4溶液和3.5 mL 1 mol·L-1 NaOH溶液混合 | 开始时有砖红色沉淀出现,一段时间后,砖红色沉淀消失,静置,试管底部有少量紫红色固体,溶液呈绿色 |
| 实验Ⅱ | 1.5 mL 1 mol·L-1 CuCl2溶液和3.5 mL 1 mol·L-1 NaOH溶液混合 | 开始时有黄色沉淀出现,一段时间后,黄色沉淀消失,静置,生成大量白色沉淀,溶液呈绿色 |
(1)制取新制Cu(OH)2悬浊液的离子方程式为 。
(2)甲同学重新用实验II的方法制备新制Cu(OH)2悬浊液,过滤,用蒸馏水洗涤干净。向洗净后的Cu(OH)2中加入5 mL蒸馏水,再持续通入SO2气体,现象与实验I相同,此步实验证明: 。检验Cu(OH)2洗涤干净的方法是 。
(3)同学们对白色沉淀的成分继续进行探究。查阅资料如下:CuCl为白色固体,难溶于水,能溶于浓盐酸。它与氨水反应生成Cu(NH3)2+,在空气中会立即被氧化成含有蓝色Cu(NH3)42+溶液。
①甲同学向洗涤得到的白色沉淀中加入氨水,得到蓝色溶液,此过程中反应的离子方程式为:CuCl + 2NH3·H2O === Cu(NH3)2+ + Cl- + 2H2O 、 。
②乙同学用另一种方法证明了该白色沉淀为CuCl,实验方案如下:
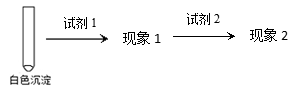
填写下表空格:
③写出实验II中由Cu(OH)2生成白色沉淀的离子方程式: 。
(4)丙同学通过实验证明:实验Ⅰ中观察到的砖红色沉淀是Cu2O。完成合理的实验方案:取少量Cu2O固体于试管中, ,则说明砖红色沉淀是Cu2O。
-
某校兴趣小组对SO2与新制Cu(OH)2悬浊液的反应进行探究,实验如下:
| 装置 | 序号 | 试管中的药品 | 现象 |
| 持续通入 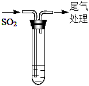
| 实验Ⅰ | 1.5 mL 1 mol·L-1 CuSO4溶液和3.5 mL 1 mol·L-1 NaOH溶液混合 | 开始时有砖红色沉淀出现,一段时间后,砖红色沉淀消失,静置,试管底部有少量紫红色固体,溶液呈绿色 |
| 实验Ⅱ | 1.5 mL 1 mol·L-1 CuCl2溶液和3.5 mL 1 mol·L-1 NaOH溶液混合 | 开始时有黄色沉淀出现,一段时间后,黄色沉淀消失,静置,生成大量白色沉淀,溶液呈绿色 |
(1)制取新制Cu(OH)2悬浊液的离子方程式为 。
(2)甲同学重新用实验II的方法制备新制Cu(OH)2悬浊液,过滤,用蒸馏水洗涤干净。向洗净后的Cu(OH)2中加入5 mL蒸馏水,再持续通入SO2气体,现象与实验I相同,此步实验证明: 。检验Cu(OH)2洗涤干净的方法是 。
(3)同学们对白色沉淀的成分继续进行探究。查阅资料如下:CuCl为白色固体,难溶于水,能溶于浓盐酸。它与氨水反应生成Cu(NH3)2+,在空气中会立即被氧化成含有蓝色Cu(NH3)42+溶液。
①甲同学向洗涤得到的白色沉淀中加入氨水,得到蓝色溶液,此过程中反应的离子方程式为:CuCl + 2NH3·H2O = Cu(NH3)2+ + Cl- + 2H2O 、 ____________ 。
②乙同学用另一种方法证明了该白色沉淀为CuCl,实验方案如下:
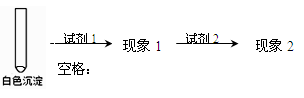
填写下表空格:
③写出实验II中由Cu(OH)2生成白色沉淀的离子方程式: 。
(4)丙同学通过实验证明实验Ⅰ中观察到的砖红色沉淀是Cu2O。完成合理的实验方案:取少量Cu2O固体于试管中, _______________ ,则说明砖红色沉淀是Cu2O。
-
某校兴趣小组对SO2与新制Cu(OH)2悬浊液的反应进行探究,实验如下:
| 装置 | 序号 | 试管中的药品 | 现象 |
| 持续通入 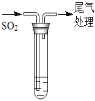
| 实验Ⅰ | 1.5 mL1 mol/L CuSO4溶液和3.5 mL 1mol/L NaOH溶液混合 | 开始时有砖红色沉淀出现,一段时间后,砖红色沉淀消失,静置,试管底部有少量紫红色固体,溶液呈绿色 |
| 实验Ⅱ | 1.5 mL1 mol/L CuCl2溶液和3.5 mL 1 mol/L NaOH溶液混合 | 开始时有黄色沉淀出现,一段时间后,黄色沉淀消失,静置,生成大量白色沉淀,溶液呈绿色 |
(1)制取新制Cu(OH)2悬浊液的离子方程式为__________________________________。
(2)甲同学重新用实验II的方法制备新制Cu(OH)2悬浊液,过滤,用蒸馏水洗涤干净。向洗净后的Cu(OH)2中加入5 mL蒸馏水,再持续通入SO2气体,现象与实验I相同,此步实验证明:__________________,检验Cu(OH)2洗涤干净的方法是____________________________________________。
(3)同学们对白色沉淀的成分继续进行探究。查阅资料如下:CuCl为白色固体,难溶于水,能溶于浓盐酸。它与氨水反应生成Cu(NH3)2+,在空气中会立即被氧化成含有蓝色Cu(NH3)42+溶液。
①甲同学向洗涤得到的白色沉淀中加入氨水,得到蓝色溶液,此过程中反应的离子方程式为:CuCl+2NH3·H2O
=Cu(NH3)2++Cl-+2H2O、____________________________。
②乙同学用另一种方法证明了该白色沉淀为CuCl,参考如下实验方案填写表格:
填写下表空格:
| 试剂1 | _________________ | 试剂2 | 蒸馏水 |
| 现象1 | _________________ | 现象2 | _________________ |
③写出实验II中由Cu(OH)2生成白色沉淀的离子方程式:_________________。
(4)丙同学通过实验证明:实验Ⅰ中观察到的砖红色沉淀是Cu2O。完成合理的实验方案:取少量Cu2O固体于试管中,_________________________________,则说明砖红色沉淀是Cu2O。
-
某兴趣小组欲探究SO2与Cu(OH)2 的反应。
| 实验 | 实验步骤 | 现象 |
| 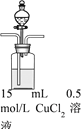
| 步骤1:打开分液漏斗,向烧瓶中加入30mL 0.5 mol/LNaOH溶液 | I. 有蓝色絮状沉淀,静置后分层。 |
| 步骤2:从左侧导管通入SO2气体 | II. 静置后分层,上层溶液为淡绿色,底部有白色沉淀 |
(1)现象I中产生蓝色沉淀的离子方程式是___________。
(2)甲为了确认现象II中白色沉淀的成分,进行如下探究。查阅资料:
| CuSO3 | CuCl | Cu2O |
| 溶解性 | 不溶于水,浅黄色沉淀 | 不溶于水,白色沉淀 | 不溶于水,砖红色沉淀 |
| 性质 | 与酸反应 | 能溶于较浓的HCl溶液 | 酸性体系中不稳定,进一步反应生成Cu和Cu2+ |
并进行如下实验:
①试剂a是___________。
②现象II中生成白色沉淀的离子方程式是___________。
(3)甲认为Cu(OH)2沉淀全部转化为CuCl,乙依据实验现象对甲的观点进行反驳,依据的实验现象是_________。
(4)丙认为实验存在干扰,欲探究纯净的Cu(OH)2 悬浊液与SO2的反应。
①丙过滤I中的蓝色沉淀,洗涤,取最后一次洗涤液于试管中,_________(填操作和现象),证明已洗涤干净。再进行如下实验:
| 实验 | 实验步骤 | 现象 |
| 
| 从左侧导管通入SO2气体 | III. 静置后分层,上层溶液为淡绿色,底部有砖红色沉淀。 |
②丙预测产物是Cu2O,取砖红色沉淀,洗涤后,_________(填操作和现象),证明产物是Cu2O。
(5)纯净的Cu(OH)2 悬浊液与SO2发生反应的化学方程式是_________。
-
某研究性学习小组用下列装置(铁架台等支撑仪器略)探究氧化铁与乙醇的反应[Cu(OH)2悬浊液用于检验反应产物]。
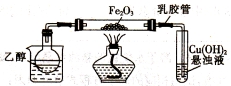
(1)组装好仪器后必须进行的操作是 。
(2)为快速得到乙醇气体,可采取的方法是 ;
若实验时小试管中的溶液已经开始发生倒吸,应采取的措施是 (填字母)。
A.取下小试管 B.移去酒精灯 C.将导管从乳胶管中取下 D.以上都可以
(3)乙醇被氧化的产物是 (写结构式)。
(4)若M的成分为FexOy,用CO还原法定量测定其化学组成。称取a g M样品进行定量测定,实验装置和步骤如下:
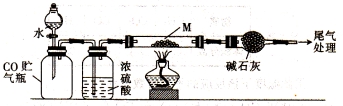
①组装仪器 ②点燃酒精灯 ③加入试剂 ④打开分液漏斗活塞 ⑤检查气密性 ⑥停止加热 ⑦关闭分液漏斗活塞 ⑧称重
ⅰ.正确的操作顺序是 (填字母)。
a.①⑤④③②⑥⑦⑧ b.①③⑤④②⑦⑥⑧
c.①⑤③④②⑥⑦⑧ d.①③⑤②④⑥⑦⑧
ⅱ.尾气处理的方法是 。
若测得碱石灰增重b g,则x:y= (用含有a、b的代数式表示)。
-
能正确 表示下列反应的离子方程式是
表示下列反应的离子方程式是
A.CuCl2溶液中加入少量氨水:Cu2++2OH-=Cu(OH)2↓
B.向酸性KMnO4溶液中通入SO2:3SO2+2MnO4-+4OH-=2MnO 2↓+3SO42-+2H2O
2↓+3SO42-+2H2O
C.向碳酸氢钙溶液中加足量澄清石灰水:HCO3-+Ca2++OH-=CaCO3↓+H2O
D.铝溶于氢氧化钠溶液:Al+2OH-+H2O=AlO2-+2H2↑
-
能正确表示下列反应的离子方程式是
A.CuCl2溶液中加入少量氨水:Cu2++2OH-=Cu(OH)2↓
B.向酸性KMnO4溶液中通入SO2:3SO2+2 MnO4-+4OH-=2MnO2↓+3 SO42-+2H2O
C.电解饱和MgCl2溶液:2Cl-+2H2O 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
D.向Na2SO3溶液中滴加足量NaClO溶液:SO32- + ClO-= SO42-+ Cl-
-
某化学学习小组在学习了Al、Fe的性质后,设计如下实验,探究Cu的常见化合物的性质。
[实验1]探究Cu(OH)2是否具有两性
药品:CuSO4溶液、浓NaOH溶液、稀H2SO4。
实验步骤:
①取少量CuSO4溶液于试管中,逐滴加入浓NaOH溶液至产生较多蓝色沉淀,静置后过滤。
②结论:Cu(OH)2具有两性。
(1)实验步骤②的内容为______
(2)能证明Cu(OH)2具有两性的实验现象为_______
[实验2]探究Cu(I)和Cu(Ⅱ)的稳定性
实验步骤:
①取98gCu(OH)2固体,加热至80~100℃时,得到80g黑色固体粉末,继续加热到1000℃以上,黑色粉末全部变成红色粉末A。
②冷却后称量,A的质量为72g。
③向A中加人适量的稀硫酸,得到蓝色溶液,同时观察到容器中还有红色固体存在。
(3)通过计算判断A的化学式为_______(不需要书写计算过程)
(4)步骤③中发生反应的离子方程式为____________
(5)根据上述实验现象得出Cu(I)和Cu(Ⅱ)的稳定性大小的结论为:固态时___________,酸性溶液中________。
[实验3]探究CuO被NH3还原的产物
该学习小组同学设计了如图所示的实验装置(夹持及尾气处理装置未面出)。实验中观察到CuO变为红色物质。查资料可知,同时生成一种无污染的气体。
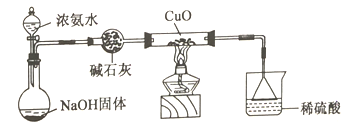
(6)反应产生的无污染气体的化学式为_______
(7)有同学认为NH3与CuO反应后生成的红色物质是Cu,也有同学认为NH3与CuO反应后生成的红色物质是Cu和A的混合物。请你设计个简单的实验方案验证红色物质中是否含有A:_____。
Cu(NH3)2+(无色);Cu+
Cu+Cu2+














