-
高铁酸钠(Na2FeO4)是具有紫色光泽的粉末,是一种高效绿色强氧化剂,碱性条件下稳定,可用于废水和生活用水的处理。实验室以石墨和铁钉为电极,以不同浓度的NaOH溶液为电解质溶液,控制一定电压电解制备高铁酸钠,电解装置和现象如下:
| c(NaOH) | 阴极现象 | 阳极现象 |
| 1 mol·L-1 | 产生无色气体 | 产生无色气体,10min内溶液颜色无明显变化 |
| 10 mol·L-1 | 产生大量无色气体 | 产生大量无色气体,3min后溶液变为浅紫红色,随后逐渐加深 |
| 15 mol·L-1 | 产生大量无色气体 | 产生大量无色气体,1min后溶液变为浅紫红色,随后逐渐加深 |
下列说法不正确的是
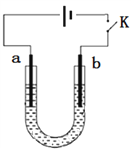
A. a为铁钉,b为石墨
B. 阴极主要发生反应:2H2O + 2e-=== H2↑+ 2OH-
C. 高浓度的NaOH溶液,有利于发生Fe-6e-+ 8OH-=== FeO42-+ 4H2O
D. 制备Na2FeO4时,若用饱和NaCl溶液,可有效避免阳极产生气体
-
高铁酸钠(Na2FeO4)是具有紫色光泽的粉末,是一种高效绿色强氧化剂,碱性条件下稳定,可用于废水和生活用水的处理。实验室以石墨和铁钉为电极,以不同浓度的NaOH溶液为电解质溶液,控制一定电压电解制备高铁酸钠,电解装置和现象如下:
| c(NaOH) | 阴极现象 | 阳极现象 |
| 1 mol·L-1 | 产生无色气体 | 产生无色气体,10min内溶液颜色无明显变化 |
| 10 mol·L-1 | 产生大量无色气体 | 产生大量无色气体,3min后溶液变为浅紫红色,随后逐渐加深 |
| 15 mol·L-1 | 产生大量无色气体 | 产生大量无色气体,1min后溶液变为浅紫红色,随后逐渐加深 |
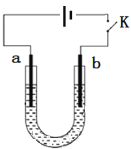
下列说法不正确的是
A. a为铁钉,b为石墨
B. 阴极主要发生反应:2H2O + 2e-=== H2↑+ 2OH-
C. 高浓度的NaOH溶液,有利于发生Fe-6e-+ 8OH-=== FeO42-+ 4H2O
D. 制备Na2FeO4时,若用饱和NaCl溶液,可有效避免阳极产生气体
-
高铁酸钠(Na2FeO4)是具有紫色光泽的粉末,是一种高效绿色强氧化剂,碱性条件下稳定,可用于废水和生活用水的处理。实验室以石墨和铁钉为电极,以不同浓度的NaOH溶液为电解质溶液,控制一定电压电解制备高铁酸钠,电解装置和现象如下:
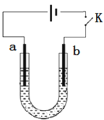
| c(NaOH) | 阴极现象 | 阳极现象 |
| 1 mol·L-1 | 产生无色气体 | 产生无色气体,10min内溶液颜色无明显变化 |
| 10 mol·L-1 | 产生大量无色气体 | 产生大量无色气体,3min后溶液变为浅紫红色,随后逐渐加深 |
| 15 mol·L-1 | 产生大量无色气体 | 产生大量无色气体,1min后溶液变为浅紫红色,随后逐渐加深 |
下列说法正确的是( )
A.a为石墨,b为铁钉
B.阴极主要发生反应 4OH--4e-== O2↑+ 2H2O
C.高浓度的NaOH溶液,有利于发生Fe-6e-+ 8OH-== FeO42-+ 4H2O
D.制备Na2FeO4时,若用饱和NaCl溶液,可有效避免阳极产生气体
-
高铁酸钠(Na2FeO4)是具有紫色光泽的粉末,是一种高效绿色强氧化剂,碱性条件下稳定,可用于废水和生活用水的处理。实验室以石墨和铁钉为电极,以不同浓度的NaOH溶液为电解质溶液,控制一定电压电解制备高铁酸钠,电解装置和现象如下:
| c(NaOH) | 阴极现象 | 阳极现象 |
| 1 mol·L-1 | 产生无色气体 | 产生无色气体,10min内溶液颜色无明显变化 |
| 10 mol·L-1 | 产生大量无色气体 | 产生大量无色气体,3min后溶液变为浅紫红色,随后逐渐加深 |
| 15 mol·L-1 | 产生大量无色气体 | 产生大量无色气体,1min后溶液变为浅紫红色,随后逐渐加深 |
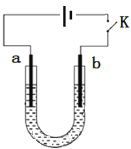
下列说法不正确的是
A. a为铁钉,b为石墨
B. 阴极主要发生反应:2H2O + 2e-=== H2↑+ 2OH-
C. 高浓度的NaOH溶液,有利于发生Fe-6e-+ 8OH-=== FeO42-+ 4H2O
D. 制备Na2FeO4时,若用饱和NaCl溶液,可有效避免阳极产生气体
-
高铁酸钠(Na2FeO4)是具有紫色光泽的粉末,是一种高效绿色强氧化剂,碱性条件下稳定,可用于废水和生活用水的处理。实验室以石墨和铁钉为电极,以不同浓度的NaOH溶液为电解质溶液,控制一定电压电解制备高铁酸钠,电解装置和现象如下:
| c(NaOH) | 阴极现象 | 阳极现象 |
| 1 mol·L-1 | 产生无色气体 | 产生无色气体,10min内溶液颜色无明显变化 |
| 10 mol·L-1 | 产生大量无色气体 | 产生大量无色气体,3min后溶液变为浅紫红色,随后逐渐加深 |
| 15 mol·L-1 | 产生大量无色气体 | 产生大量无色气体,1min后溶液变为浅紫红色,随后逐渐加深 |
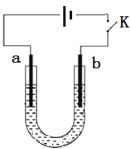
下列说法不正确的是
A. a为铁钉,b为石墨
B. 阴极主要发生反应:2H2O + 2e-=== H2↑+ 2OH-
C. 高浓度的NaOH溶液,有利于发生Fe-6e-+ 8OH-=== FeO42-+ 4H2O
D. 制备Na2FeO4时,若用饱和NaCl溶液,可有效避免阳极产生气体
-
高铁酸钠(Na2FeO4)是具有紫色光泽的粉末,是一种高效绿色强氧化剂,碱性条件下稳定,可用于废水和生活用水的处理。实验室以石墨和铁钉为电极,以不同浓度的NaOH溶液为电解质溶液,控制一定电压电解制备高铁酸钠,电解装置和现象如下:
| c(NaOH) | 阴极现象 | 阳极现象 |
| 1 mol·L-1 | 产生无色气体 | 产生无色气体,10min内溶液颜色无明显变化 |
| 10 mol·L-1 | 产生大量无色气体 | 产生大量无色气体,3min后溶液变为浅紫红色,随后逐渐加深 |
| 15 mol·L-1 | 产生大量无色气体 | 产生大量无色气体,1min后溶液变为浅紫红色,随后逐渐加深 |
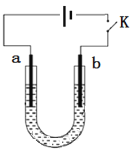
下列说法不正确的是
A. a为铁钉,b为石墨
B. 阴极主要发生反应:2H2O + 2e-=== H2↑+ 2OH-
C. 高浓度的NaOH溶液,有利于发生Fe-6e-+ 8OH-=== FeO42-+ 4H2O
D. 制备Na2FeO4时,若用饱和NaCl溶液,可有效避免阳极产生气体
-
电解高铁酸盐(如K2FeO4)是一种高效绿色氧化剂,可用于废水和生活用水的处理.从环境保护的角度看,制备高铁酸盐较好的方法为电解法:Fe+2NaOH+2H2O═Na2FeO4+H2↑.
(1)采用铁片作阳极,NaOH溶液为电解质溶液,电解制备高铁酸钠,其电流效率可达到40%.写出阳极的电极反应式:______.
(2)铁丝网电极是更理想的阳极材料,相同条件下,可将电流效率提高至70%以上,原因是______.研究亦发现,铁电极在某一电压范围内会生成Fe2O3膜而“钝化”,钝化的原因用反应式表示为______.
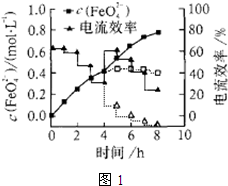
(3)FeO42-易与水反应生成絮状氢氧化铁,也会影响高铁酸盐的产率.若以铁丝网为阳极,在中间环节(对应图1中4h后)过滤掉氢氧化铁,合成过程中FeO42-浓度以及电流效率随时间的变化如图1中实线所示(图中曲线是每隔1h测得的数据).图中虚线部分对应于没有过滤氢氧化铁而连续电解的情况.下列判断正确的是______
A.过滤掉氢氧化铁有利于获得较高浓度的高铁酸盐溶液
B.过滤掉氢氧化铁对电流效率影响不大
C.实验表明氢氧化铁的存在影响高铁酸盐浓度的增加
D.实验表明不过滤掉氢氧化铁,6h后电流效率几乎为0
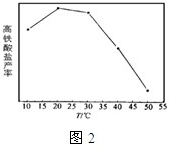
(4)碱性条件下,高铁酸盐的稳定性与温度有关(如图2).随温度升高,高铁酸盐产率先增大后减小的原因是______.
(5)人们还对用铁的氧化物作电极制备高铁酸盐进行了研究,例如以磁铁矿多孔电极制备高铁酸盐,该研究方向的价值在于______
A.将1mol Fe3O4氧化成高铁酸盐需10/3mol电子,可提高电流效率
B.以铁的氧化物为电极,可以实现变废(Fe3O4或铁锈)为宝(高铁酸盐)
C.自然界几乎没有铁单质,而有大量磁铁矿,该方法的原料来源广泛
D.磁铁矿作为多孔电极不会出现钝化现象.
-
高铁酸盐是一种高效绿色氧化剂,可用于废水和生活用水的处理。从环境保护的角度看,制备高铁酸盐较好的方法为电解法:Fe+2H2O+2OH FeO42-+3H2↑,工作原理如图所示。己知:Na2FeO4只在强碱性条件下稳定,易被H2还原。下列说法正确的是
FeO42-+3H2↑,工作原理如图所示。己知:Na2FeO4只在强碱性条件下稳定,易被H2还原。下列说法正确的是
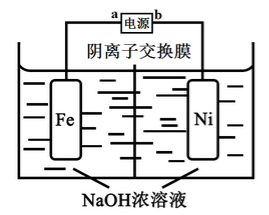
A. b是电源的正极
B. 阳极电极反应为Fe-6e-+4H2O= FeO42-+ 8H+
C. 电解过程中,需要将阴极产生的气体及时排出
D. 当电路中通过1mol电子的电量时,会有11.2L的H2生成
-
研究证明高铁酸钠 是一种“绿色环保高效”消毒剂,比目前国内外广泛使用的含氯饮用水消毒剂性能更为优良。高铁酸钠只能在碱性环境中稳定存在。下列是通过次氯酸钠氧化法制备高铁酸钠并探究其性质的实验,步骤如下:
是一种“绿色环保高效”消毒剂,比目前国内外广泛使用的含氯饮用水消毒剂性能更为优良。高铁酸钠只能在碱性环境中稳定存在。下列是通过次氯酸钠氧化法制备高铁酸钠并探究其性质的实验,步骤如下:
Ⅰ 用氯气和氢氧化钠溶液反应制备NaClO溶液
用氯气和氢氧化钠溶液反应制备NaClO溶液
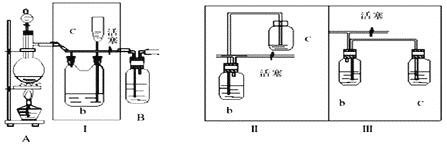
(1) 是氯气发生装置,写出实验室用此装置制取氯气的离子方程式___________。
是氯气发生装置,写出实验室用此装置制取氯气的离子方程式___________。
(2)Ⅰ装置的作用是__________。
(3)用图示的Ⅱ或Ⅲ代替Ⅰ是否可行?___________。简要说明理由_________________________。
(4)将产生的氯气通入D装置中制NaClO溶液
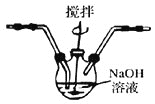
已知: 为了防止产生
为了防止产生 ,除搅拌和混入
,除搅拌和混入 稀释外,还应采取的操作是___________________________。
稀释外,还应采取的操作是___________________________。
Ⅱ 制备
制备
(1)将 溶液加入到NaOH与NaClO的混合溶液中,过滤得到粗产品,再用NaOH溶液溶解,重结晶,用有机溶剂脱碱,低温烘干得到固体样品,上述制备过程中,用NaOH溶液溶解粗产品而不用水的原因是______________________________。
溶液加入到NaOH与NaClO的混合溶液中,过滤得到粗产品,再用NaOH溶液溶解,重结晶,用有机溶剂脱碱,低温烘干得到固体样品,上述制备过程中,用NaOH溶液溶解粗产品而不用水的原因是______________________________。
(2)高铁酸钠电池是一种新型可充电电池,电解质为NaOH溶液,放电时负极材料为Zn,正极产生红褐色沉淀,写出该电池反应的化学方程式_______________________。
-
(18分)高铁酸盐(如K2FeO4)是一种高效绿色氧化剂,可用于饮用水和生活用水的处理。从环境保护的角度看,制备高铁酸盐较好的方法为电化学法。
(1)电化学法制备高铁酸钠采用铁片作阳极,NaOH溶液作为电解质溶液,其电流效率可达到40%。写出阳极产生高铁酸钠的电极反应方程式:________。
(2)铁丝网电极是更理想的阳极材料,相同条件下,可将电流效率提高至70%以上,原因是________。研究亦发现,铁电极在某一电压范围内会产生氧气使阳极表面生成Fe2O3膜而“钝化”。写出产生O2的电极反应方程式:________。
(3)FeO42—易与水4h生成絮状氢氧化铁,也会影响高铁酸盐的产率。若以铁丝网为阳极,在中间环节(对应图中4h后)过滤掉氢氧化铁,反应过程中FeO42—浓度以及电流效率随时间的变化如图1中实线所示(图中曲线是每隔1h测得的数据)。图中虚线部分对应于没有过滤氢氧化铁而连续电解的情况。下列判断正确的是________(填编号)
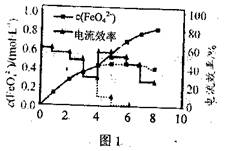
①过滤:掉氢氧化铁有利于获得较高浓度的高铁酸盐溶液
②过滤掉氢氧化铁对电流效率影响不大
③实验表明不过滤掉氢氧化铁,6h后电流效率几乎为0
(4)在相同的pH条件下,经过相同的反应时间,高铁酸盐的产率与温度关系如图2。
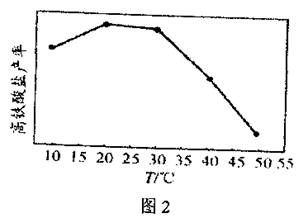
随温度升高,高铁酸盐产率先增大后减小的原因是________。
(5)人们还对用铁的氧化物作电极制备高铁酸盐进行了研究,例如以磁铁矿多孔电极制备高铁酸盐,该研究方向的价值有________(至少答一点)。












