-
对甲基苯胺可用对硝基甲苯作原料在一定条件制得。 主要反应及装置如下:
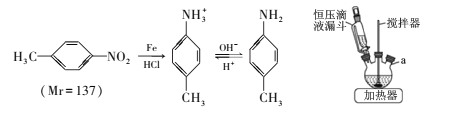
主要反应物和产物的物理性质见下表:
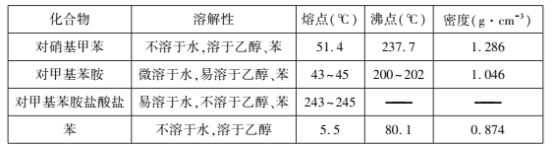
实验步骤如下:
①向三颈烧瓶中加入50mL稀盐酸、10.7mL(13.7g)对硝基甲苯和适量铁粉,维持瓶内温度在80℃左右,同时搅拌回流、使其充分反应;
②调节pH=7~8,再逐滴加入30mL苯充分混合;
③抽滤得到固体,将滤液静置、分液得液体M;
④向M中滴加盐酸,振荡、静置、分液,向下层液体中加入NaOH溶液,充分振荡、静置;
⑤抽滤得固体,将其洗涤、干燥得6.1g产品。
回答下列问题:
(1)主要反应装置如上图,a处缺少的装置是____ (填仪器名称),实验步骤③和④的分液操作中使用到下列仪器中的_____(填标号)。
a.烧杯 b.漏斗 c.玻璃棒 d.铁架台
(2)步骤②中用5%的碳酸钠溶液调pH =7~8的目的之一是使Fe3+ 转化为氢氧化铁沉淀,另一个目的是 ____。
(3)步骤③中液体M是分液时的____ 层(填“上”或“下”)液体,加入盐酸的作用是____。
(4)步骤④中加入氢氧化钠溶液后发生反应的离子方程式有____。
(5)步骤⑤中,以下洗涤剂中最合适的是____ (填标号)。
a.乙醇 b.蒸馏水 c.HCl溶液 d.NaOH溶液
(6)本实验的产率是_____%。(计算结果保留一位小数)
-
对甲基苯胺可用对硝基甲苯在酸性条件下用铁粉还原制得:
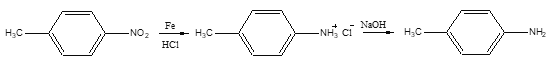
主要反应物和产物的物理性质见下表:
| 化合物 | 物质状态 | 溶解性 | 熔点(℃) | 沸点(℃) | 密度(g·cm-3) |
| 对硝基甲苯 | 浅黄色晶体 | 不溶于水,溶于乙醇、苯 | 51.4 | 237.7 | 1.286 |
| 对甲基苯胺 | 白色片状晶体 | 微溶于水,易溶于乙醇、苯 | 43~45 | 200~202 | 1.046 |
| 对甲基苯胺盐酸盐 | 白色晶体 | 易溶于水,不溶于乙醇、苯 | 243~245 | —— | —— |
| 苯 | 无色液体 | 不溶于水,溶于乙醇 | 5.5 | 80.1 | 0.874 |
实验流程如下:
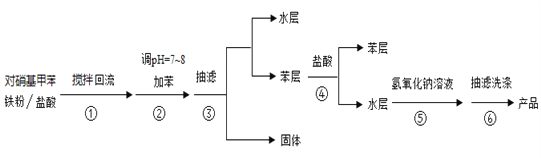
请回答下列问题:
(1)反应装置如图,a处缺少一装置_____________(填仪器名称)
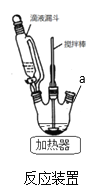
(2)步骤②中加苯的作用是_____________,步骤②中用5%碳酸钠溶液调pH=7~8的原因_________
(3)步骤③得到的固体物质为_________
(4)步骤④中加入盐酸的作用是_____________
(5)步骤⑤中通过加入氢氧化钠溶液使对甲基苯胺结晶析出的原理为_____________
(6)步骤⑥中,以下洗涤剂最合适的是_____________
A. 蒸馏水 B.乙醇 C.NaOH溶液 D.HCl溶液
-
已知: (苯胺,易被氧化)。甲苯是一种重要的有机化工原料,可用来合成多种重要的有机物。以甲苯为初始原料合成阿司匹林等有机物的转化关系图(部分产物、合成路线、反应条件略去)如下。
(苯胺,易被氧化)。甲苯是一种重要的有机化工原料,可用来合成多种重要的有机物。以甲苯为初始原料合成阿司匹林等有机物的转化关系图(部分产物、合成路线、反应条件略去)如下。
 请回答下列问题:
请回答下列问题:
(1)甲苯的1H核磁共振谱图中有________个特征峰。
(2)中间产物D与目标产物Y的关系是________。
(3)写出结构简式:A________,E________。
(4)写出所加试剂或反应条件:反应⑤________。
(5)写出反应③的化学方程式:
________。
(6)写出阿司匹林与足量的NaOH(aq)反应的化学方程式:
________。
-
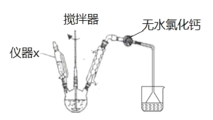
对甲基苯乙酮是重要的化工原料,某实验小组利用如图装置制备对甲基苯乙酮。
制备原理: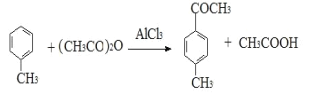 (放热反应)。 反应物和产物的相关数据列表:
(放热反应)。 反应物和产物的相关数据列表:
| 试剂名称 | 分子式 | 分子量 | 熔点/℃ | 沸点/℃ | 密度/g·mL-1 |
| 甲苯 | C7H8 | 92 | -93 | 110.6 | 0.8669 |
| 乙酸酐 | (CH3CO)2 | 102 | -73.1 | 138.6 | 1.08 |
| 对甲基苯乙酮 | C9H10O | 134 | 28 | 94(0.93kPa) | 1.0051 |
实验步骤:
步骤 1:如图所示,在 100mL 三颈烧瓶上安装搅拌器、仪器 x 和上口装有无水氯化钙的冷凝管,干燥管与一气体 吸收装置相连。
步骤 2:三颈烧瓶中快速加入研碎的催化剂和 20mL 无水甲苯,在搅拌的条件下通过仪器 x 缓慢地滴加 3.4mL 醋酸酐与 5mL 甲苯的混合液,约需 15min 滴完。
步骤 3:反应结束后,将三颈烧瓶在 95℃时加热 25~30min。
步骤 4:反应混合液冷却后转移到盛有 30mL 浓盐酸与 30mL 冰水的烧杯中(目的是将对甲基苯乙酮从其与铝的化 合物中分离出来),用分液漏斗分出有机层、水层。每次用 5mL 甲苯萃取两次,并将所有甲苯层合并,然后依次 用水、10%氢氧化钠溶液、水各 10mL 洗涤有机层,最后用无水硫酸镁处理。
步骤 5:将干燥后的溶液滤入蒸馏瓶,减压蒸馏(整套装置必须是干燥的),收集 94℃(0.93kPa)馏分,得到对甲 基苯乙酮 4.1g。
请回答下列问题:
(1)仪器 x 的名称为________。与普通的分液漏斗相比,本实验采用仪器 x 的优点为_______。
(2)本实验中的氯化铝若水解则会影响催化效率,除了使用干燥管的措施外,还应该采取哪些措施防止水解_____(答两点)。
(3)步骤③中最适宜的加热方式为 _____。
(4)步骤④中加入 10%的氢氧化钠溶液的目的为 _____,加入无水硫酸镁的目的为__________。
(5)步骤④中水层每次用 5mL 甲苯萃取两次并将所有甲苯层合并的目的为________。
(6)步骤⑤中减压蒸馏时所需的冷凝装置能否选用题给装置图中的球形冷能管_____(答“能”或“不能”)。 本实验中,对甲基苯乙酮的产率为_____(结果保留 2 位有效数字)。
-
4,7—二甲基香豆素(熔点:132.6℃)是一种重要的香料。由间甲苯酚为原料合成4,7—二甲基香豆素的反应如下:
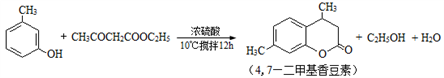
实验装置图如下:
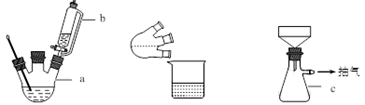
主要实验步骤:
步骤1:向装置a中加入60 mL浓硫酸,并冷却至0℃以下,搅拌下滴入间甲苯酚30 mL(0.29 mol)和乙酰乙酸乙酯26.4 mL(0.21 mol)的混合物。
步骤2:保持10℃,搅拌12 h,反应完全后,将其倒入冰水混合物中,然后抽滤、水洗得粗产品。
步骤3:粗产品用乙醇溶解并重结晶,得白色针状晶体并烘干,称得产品质量为33.0 g。
(1)简述装置b中将活塞上下部分连通的目的_____________。
(2)装置c的名称为_____________,与过滤相比,抽滤的优点是_____________。
(3)浓硫酸需要冷却至0℃以下的原因是_____________。
(4)反应需要搅拌12 h,其原因是_____________。
(5)本次实验产率为_____________。
-
(14分)4,7—二甲基香豆素(熔点:132.6℃)是一种重要的香料,广泛分布于植物界中,由间—甲苯酚为原料的合成反应如下: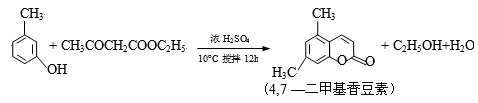
实验装置图如下:
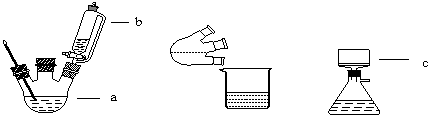
主要实验步骤:
步骤1.向装置a中加入60mL浓硫酸,并冷却至0℃以下,搅拌下滴入间—甲苯酚30mL(0.29mol)和乙酰乙酸乙酯26.4mL (0.21mol)的混合物。
步骤2.保持在10℃下,搅拌12h,反应完全后,将其倒入冰水混合物中,然后抽滤、水洗得粗产品
步骤3.粗产品用乙醇溶解并重结晶,得白色针状晶体并烘干,称得产品质量为33.0g。
(1)图中仪器名称:a 。
(2)简述装置b中将活塞上下部分连通的目的 。
(3)浓H2SO4需要冷却至0℃以下的原因是 。
(4)反应需要搅拌12h,其原因是 。
(5)本次实验产率为 。
(6)实验室制备乙酸乙酯的化学反应方程式 ,用 (填药品名称)收集粗产品,用 (填操作名称)的方法把粗产品分离。
-
4,7-二甲基香豆素(熔点:132.6℃)是一种重要的香料,广泛分布于植物界中,由间甲苯酚为原料的合成反应如下:
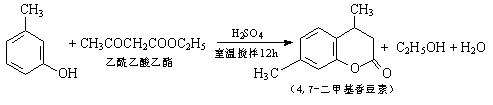
实验装置图如下:
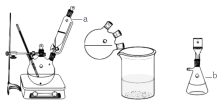
主要实验步骤:
步骤1.向三口烧瓶中加入60mL浓硫酸,并冷却至0℃以下,搅拌下滴入间甲苯酚30mL(0.29mol)和乙酰乙酸乙酯26.4mL (0.21mol)的混合物。
步骤2.保持在10℃下,搅拌12h,反应完全后,将其倒入冰水混合物中,然后抽滤、水洗得粗品
步骤3.粗品用乙醇溶解并重结晶,得白色针状晶体并烘干,称得产品质量为33.0g。
(1)图中仪品名称:a ,b 。
(2)浓H2SO4需要冷却至0℃以下的原因是 。
(3)反应需要搅拌12h,其原因是 。
(4)确定最终产品是4,7-二甲基香豆素的实验或方法是 。
(5)本次实验产率为 。
-
有机物H是一种新型大环芳酰胺的合成原料,可通过以下方法合成:
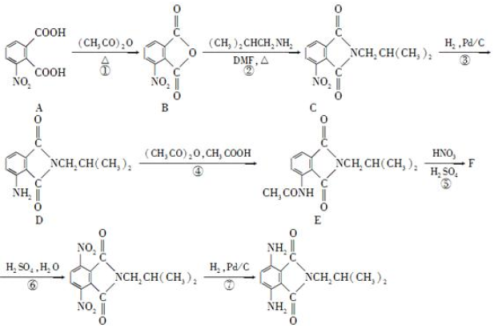
已知:①苯胺(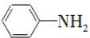 )有还原性,易被氧化;
)有还原性,易被氧化;
②硝基苯直接硝化主要产物为二硝基苯。
(1)写出A中含氧官能团的名称: 。
(2)④的反应类型为 ;F的结构简式为 。
(3)流程中设计步骤④和⑥的目的是 。
(4)写出一种符合下列条件的化合物C的同分异构体的结构简式 。
①分子中含有2个苯环;②能与FeCl3溶液发生显色反应;③分子中有3种不同化学环境的氢子。
(5)对苯二胺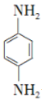 是一种重要的染料中间体。根据已有知识并结合相关信息,写出以苯、(CH3CO)2O及CH3COOH为主要有机原料制备对苯二胺的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
是一种重要的染料中间体。根据已有知识并结合相关信息,写出以苯、(CH3CO)2O及CH3COOH为主要有机原料制备对苯二胺的合成路线流程图(无机试剂任用)。合成路线流程图示例如下: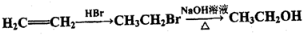
-
芳香羧酸通常用芳香烃的氧化来制备,某同学用甲苯的氧化反应制备苯甲酸。已知: +2KMnO4
+2KMnO4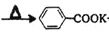 +KOH+2MnO2↓+H2O
+KOH+2MnO2↓+H2O
反应试剂、产物的物理常数:

主要实验装置和流程如下:
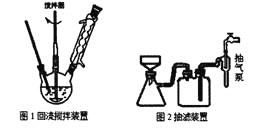
实验方法:向图1装置中依次加入2.8mL甲苯、200mL水和8.6g高锰酸钾,通冷凝水,加热至沸腾,在反应过程中,甲苯不断的被冷凝回流,反应结束后,按以下步骤操作,得到苯甲酸粗产品。

(1)图1装置中反应结束的标志是__,趁热抽滤的目的是__。
(2)写出浓盐酸酸化时的所有离子反应方程式__。
(3)下列说法正确的是__。
A.图1装置中的反应混合物抽滤时应用玻璃砂漏斗替代布氏漏斗
B.在冷却抽滤时,若有产品黏在瓶壁上,可用滤液淋洗,直到所有晶体收集到布氏漏斗中,再次抽滤
C.苯甲酸粗产品的杂质除KCl外还可能含有甲苯,均可用蒸馏水洗涤除去
D.抽滤结束,为防止倒吸,应先关闭水龙头,再拆掉抽气泵和吸滤瓶之间的橡皮管
(4)苯甲酸纯度测定:用__(填仪器名称)称取1.220g产品,加合适溶剂溶解,再用蒸馏水稀释配成100mL溶液,取25.00mL溶液,滴加几滴指示剂,用0.1000mol•L-1NaOH标准液进行滴定,平行滴定3次,平均消耗标准液体积为21.00mL
①“合适溶剂”和“指示剂”分别为__。
A.蒸馏水和酚酞 B.乙醇和甲基橙 C.四氯化碳和酚酞 D.乙醇和酚酞
②苯甲酸产品的纯度为__。
-
苯胺为无色液体,还原性强,易被氧化,有碱性,与酸反应生成盐,硝基苯与氢气制备苯胺(沸点为184℃)的反应原理如下:
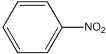 +3H2
+3H2
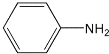 +2H2O
+2H2O
某同学设计的制备实验装置(部分夹持装置省略)如图:

下列说法正确的是( )
A.仅用上述装置图中仪器就可以完成该实验
B.用硝酸代替盐酸,反应速率更快,实验效果较好
C.点燃酒精灯前,打开K,先通一段时间的H2
D.三颈烧瓶内的反应结束后,关闭K,先在三颈烧瓶中加入浓硫酸后蒸馏





 请回答下列问题:
请回答下列问题:
 (放热反应)。 反应物和产物的相关数据列表:
(放热反应)。 反应物和产物的相关数据列表:

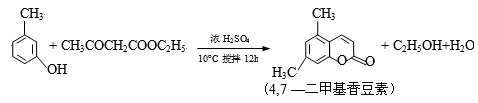




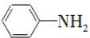 )有还原性,易被氧化;
)有还原性,易被氧化; 是一种重要的染料中间体。根据已有知识并结合相关信息,写出以苯、(CH3CO)2O及CH3COOH为主要有机原料制备对苯二胺的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
是一种重要的染料中间体。根据已有知识并结合相关信息,写出以苯、(CH3CO)2O及CH3COOH为主要有机原料制备对苯二胺的合成路线流程图(无机试剂任用)。合成路线流程图示例如下: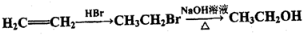
 +KOH+2MnO2↓+H2O
+KOH+2MnO2↓+H2O


 +3H2
+3H2 +2H2O
+2H2O