-
科学家预测21世纪中叶将进入“氢能经济”时代,许多化合物或合金都是具有广阔应用前景的储氢材料。回答下列问题:
(1)基态Li原子核外电子有___种不同的运动状态,占据最高能层电子的电子云轮廓图形状为__。
(2)Li的焰色反应为紫红色,很多金属元素能产生焰色反应的原因为__________。
(3)亚氨基锂(Li2NH) 中所含的元素,电负性由大到小排列的顺序是_________。
(4)咔唑(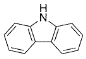 )的沸点比芴(
)的沸点比芴(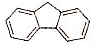 )高的主要原因是_______。
)高的主要原因是_______。
(5)NH3BH3 (氨硼烷,熔点104℃)与______(写出一种分子)互为等电子体。可通过红外光谱测定该分子的立体构型,NH3BH3中B的杂化轨道类型为________。
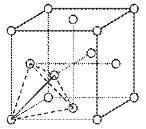
(6)一种储氢合金的晶胞结构如图所示。在晶胞中Cu原子处于面心,Au原子处于顶点位置。该晶体中,原子之间的作用力是_______。实现储氢功能时,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中心(如图),若所有四面体空隙都填满,该晶体储氢后的化学式为______。
-
盐X由三种元素组成,其具有良好的热电性能,在热电转换领域具有广阔的应用前景。为研究它的组成和性质,现取12.30g化合物X进行如下实验:
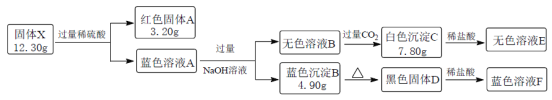
试根据以上内容回答下列问题:
(1)X的化学式为_____________。
(2)无色溶液B中通入过量CO2产生白色沉淀的离子方程式为______________。
(3)蓝色溶液F中通入中SO2气体会产生白色沉淀,该沉淀中氯元素质量分数为35.7%,其离子方程式为____________。
(4)白色沉淀C煅烧的固体产物与D高温反应可生成化合物X,其化学方程式为__________。
-
碳纳米管、石墨烯、C60等新型碳材料具有广阔的应用前景。下列说法正确的是

A. 碳纳米管属于胶体
B. 石墨烯属于有机化合物
C. C60与金刚石互为同素异形体
D. 均具有相同的熔点
-
碳纳米管、石墨烯、C60等新型碳材料具有广阔的应用前景。下列说法正确的是

A. 碳纳米管属于胶体
B. 石墨烯属于有机化合物
C. C60与金刚石互为同素异形体
D. 均具有相同的熔点
-
甲烷和甲醇可以做燃料电池,具有广阔的开发和应用前景,回答下列问题
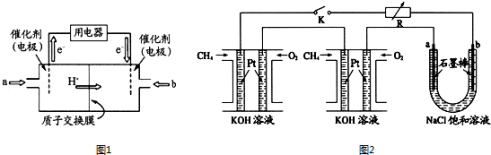
(1)甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注.DMFC工作原理如图1所示:通入a气体的电极是原电池的 极(填“正”“负”),其电极反应式为 .
(2)某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图2所示U形管中氯化钠溶液的体积为800ml.闭合K后,若每个电池甲烷用量均为0.224L(标况),且反应完全,则理论上通过电解池的电量为 (法拉第常数F=9.65×104C/mol),若产生的气体全部逸出,电解后溶液混合均匀,电解后U形管中溶液的pH为 .
-
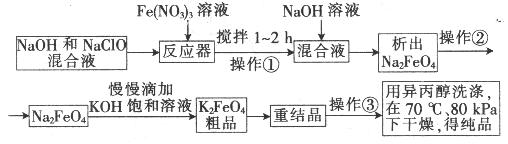
高铁酸钾是一种高效的多功能水处理剂,具有氧化、吸附、絮凝、、助凝、杀菌、除臭等作用,高铁酸钾的开发和利用正日益显示出其广阔的应用前景。其制备流程如下:
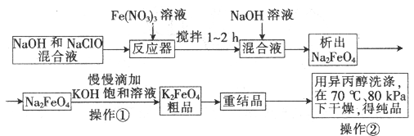
试回答下列问题
(1)反应器中,NaOH、NaClO、Fe(NO3)3发生反应生成Na2FeO4,完成并配平下列离子反应方程式:
□Fe3++□ClO─+□OH─ ==□FeO42─+□Cl─+□___________
(2)次氯酸钠浓度对高铁酸钾产率有一定影响,当NaClO浓度为298g/L时,高铁酸钠的产率最高,此时NaClO的物质的量浓度为_______________。
(3)你认为操作①能够发生转化的原因是__________,慢慢滴加的原因的是___________。
(4)操作②如果温度过高会造成高铁酸钾的分解,高铁酸钾受热分解时生成金属氧化物和氧气,该反应的化学方程式为__________________。
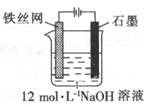
(5)可以用电化学法制取Na2FeO4,其装置如图所示,则阳极的电极反应式为________;
阴极的电极反应式为______________;电解一段时间后溶OH─的浓度会_________(填“升高”、“降低”
或“不变”)。
-
甲醇是一种可再生能源,具有开发和应用的广阔前景,请回答下列问题:
(1)一定温度下,在一恒容的密闭容器中,由CO和H2合成甲醇:CO (g) + 2H2 (g) ═ CH3OH (g).下列情形不能说明该反应已达到平衡状态的是 (填序号)
A.每消耗1mol CO的同时生成2molH2
B.混合气体的平均摩尔质量不再变化
C.生成CH3OH的速率与消耗CO的速率相等
D.容器的总压强不再发生变化
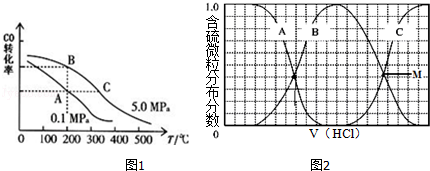
(2)CO的平衡转化率(α)与温度、压强的关系如图1所示,B、C两点的平衡常数K(B) K(C)(填“>”、“=”或“<”),你判断的理由是 ,要在提高CO平衡转化率的同时加快反应速率,可采取的措施是 (任写一条).
(3)向等物质的量浓度Na2S、NaOH混合溶液中滴加稀盐酸至过量.其中H2S、HS﹣、S2﹣的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与滴加盐酸体积的关系如图2所示(忽略滴加过程H2S气体的逸出).试分析:
①B曲线代表 的分布分数变化;滴加过程中,溶液中一定成立:c(Na+)= .(用溶液中的相关微粒浓度表示)
②若M点溶液pH约为7,则H2S第一步的电离平衡常数Ka= .
-
应对雾霾污染、改善空气质量需要从多方面入手,如开发利用清洁能源.甲醇是一种可再生的清洁能源,具有广阔的开发和应用前景.回答下列问题:
(1) 与
与 合成甲醇:
合成甲醇: 但是找到合适的催化剂是制约该方法的瓶颈.目前主要使用贵金属催化剂,但是贵金属储量稀少,成本高昂,难以大规模应用,且使用中存在环境污染的风险.最近采用真空封管法制备磷化硼纳米颗粒,在发展非金属催化剂实现
但是找到合适的催化剂是制约该方法的瓶颈.目前主要使用贵金属催化剂,但是贵金属储量稀少,成本高昂,难以大规模应用,且使用中存在环境污染的风险.最近采用真空封管法制备磷化硼纳米颗粒,在发展非金属催化剂实现 电催化还原制备甲醇方向取得重要进展,该反应历程如图所示.
电催化还原制备甲醇方向取得重要进展,该反应历程如图所示.
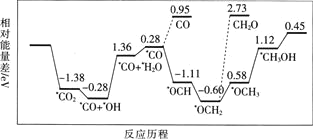
容易得到的副产物有CO和 ,其中相对较多的副产物为________________;上述合成甲醇的反应速率较慢,要使反应速率加快,主要降低下列变化中________
,其中相对较多的副产物为________________;上述合成甲醇的反应速率较慢,要使反应速率加快,主要降低下列变化中________ 填字母
填字母 的能量变化.
的能量变化.
A. B.
B.
C. D.
D.
(2)恒压 容器的容积可变
容器的容积可变 下,
下, 与
与 在催化剂作用下发生反应
在催化剂作用下发生反应
 ,
, 的平衡转化率与温度、压强的关系如图所示.
的平衡转化率与温度、压强的关系如图所示.
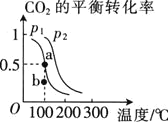
①压强 ________
________ 填“
填“ ”或“
”或“ ”
” .
.
②在 、
、 条件下,b点时
条件下,b点时 ________
________ 填“
填“ ”或“
”或“ ”
” .
.
③已知:反应速率 ,
, 、
、 分别为正、逆反应速率常数,x为物质的量分数,若b点对应的坐标参数为
分别为正、逆反应速率常数,x为物质的量分数,若b点对应的坐标参数为 ,计算b处的
,计算b处的 ________
________ 保留3位有效数字
保留3位有效数字 .
.
(3)焦炭与水蒸气在恒容密闭容器中反应制合成气的主要反应 Ⅰ
Ⅰ 、
、 Ⅱ
Ⅱ 的
的 为以分压表示的平衡常数
为以分压表示的平衡常数 与T的关系如下图所示.
与T的关系如下图所示.
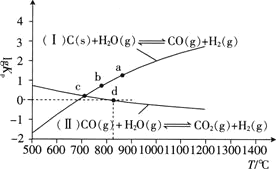
①反应 Ⅱ
Ⅱ 的
的 ________
________ 填“大于”“等于”或“小于”
填“大于”“等于”或“小于” .
.
② 点时,反应
点时,反应 的
的 ________
________ 填数值
填数值 .
.
③在恒容密闭容器中充入 、
、 只发生反应
只发生反应 Ⅱ
Ⅱ ,图中d点处达到平衡时,CO的转化率为________;达到平衡时,向容器中再充入
,图中d点处达到平衡时,CO的转化率为________;达到平衡时,向容器中再充入 、
、 ,重新达到平衡时,CO的平衡转化率________
,重新达到平衡时,CO的平衡转化率________ 填“增大”“减小”或“不变”
填“增大”“减小”或“不变” .
.
-
高铁酸钾是一种高效的多功能水处理剂,具有氧化、吸附、絮凝、、助凝、杀菌、除臭等作用,高铁酸钾的开发和利用正日益显示出其广阔的应用前景。其制备路线如下:
试回答下列问题
(1)操作①搅拌的目的是:________。
(2)操作②与操作③相同,该操作名称是:___________________。
(3)反应器中, NaOH、NaClO及Fe(NO3)3反应的离子方程式为: _______________________。
(4)次氯酸钠浓度对高铁酸钾产率有一定影响,当高铁酸钾产率最高时,NaClO的物质的量浓度约为_________。(计算结果保留一位小数)
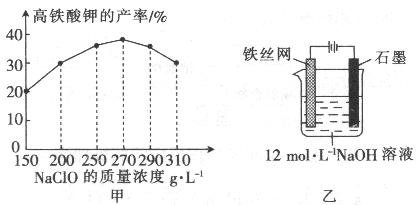
(5)从环境保护的角度看,制备中间产物Na2FeO4较好的方法为电化学法,其装置如图乙所示,则阳极的电极反应式为________。
-
高铁酸钾是一种高效的多功能水处理剂,具有氧化、吸附、絮凝、、助凝、杀菌、除臭等作用,高铁酸钾的开发和利用正日益显示出其广阔的应用前景。其制备路线如下:
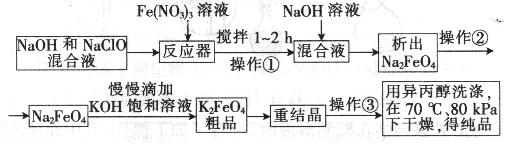
试回答下列问题
(1)操作①后的混合液中加入NaOH溶液的作用是:________。
最后用异丙醇洗涤产品的目的是________。
(2) 操作②与操作③相同,该操作名称是:___________________。
(3)反应器中,NaOH、NaClO及Fe(NO3)3反应的离子方程式为: _____________________。
(4)次氯酸钠浓度对高铁酸钾产率有一定影响(下图甲),当高铁酸钾产率最高时,NaClO的物质的量浓度约为_________。(计算结果保留一位小数)
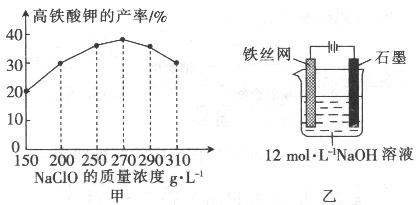
(5)从环境保护的角度看,制备中间产物Na2FeO4较好的方法为电化学法,其装置如图乙所示,则阳极的电极反应式为________。
 )的沸点比芴(
)的沸点比芴( )高的主要原因是_______。
)高的主要原因是_______。













