-
将 SO2 分别通入无氧、有氧的浓度均为 0.1 mol·L-1的 BaCl2 溶液和 Ba(NO3)2 溶液中,除 BaCl2 溶液(无氧)外,都产生白色沉淀。实验测得各溶液 pH 变化曲线如图:
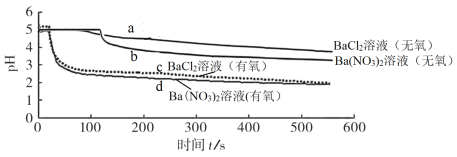
下列说法正确的是
A.曲线a所示溶液pH降低的原因:SO2+H2O H2SO3
H2SO3 H++HSO
H++HSO
B.依据曲线b可推知0.2 mol·L-1KNO3溶液(无氧)能氧化SO2
C.曲线c所示溶液中发生反应的离子方程式为:Ba2++SO2+O2=BaSO4↓
D.曲线d所表示的过程中NO 是氧化SO2的主要微粒
是氧化SO2的主要微粒
-
把少量CO2分别通入到浓度均为0.1mol/L的①Ba(NO3)2溶液;②Ba(OH)2溶液;③溶有氨的BaCl2溶液中;④Na2CO3溶液,预计可能观察到白色沉淀的溶液是
A.①、②和④ B.只有② C.②和③ D.②和④
-
下列7种溶液中,通入足量的SO2气体,溶液变浑浊的有
①NazS溶液②Na2SiO3溶液③澄清石灰水④0.1mol/L Ca(ClO)2溶液⑤Ba(NO3)2溶液 ⑥BaCl2溶液⑦酸性KMnO4溶液
A. 3种 B. 4种 C. 5种 D. 6种
-
下列7种溶液中,通入足量的SO2气体,溶液变浑浊的有
①NazS溶液②Na2SiO3溶液③澄清石灰水④0.1mol/L Ca(ClO)2溶液⑤Ba(NO3)2溶液 ⑥BaCl2溶液⑦酸性KMnO4溶液
A.3种 B.4种 C.5种 D.6种
-
某学习小组在实验室研究SO2与Ba(NO3)2溶液的反应:
实验:向盛有2mL 0.1mol/L Ba(NO3)2 溶液的试管中,缓慢通入SO2气体,试管内有白色沉淀产生,液面上方略显浅棕色。
探究1:白色沉淀产生的原因。
(1)白色沉淀是 。
(2)分析白色沉淀产生的原因,甲同学认为是NO3-氧化了SO2,乙同学认为是溶液中溶解的O2氧化了SO2。
① 支持甲同学观点的实验证据是 。
② 依据甲的推断,请写出Ba(NO3)2溶液与SO2反应的离子方程式 。
③ 乙同学通过下列实验证明了自己的推测正确,请完成实验方案:
| 实验操作 | 实验现象 |
| 向2mL mol/L 溶液(填化学式)中通入SO2 | |
探究2:在氧化SO2的过程中,NO3-和O2哪种微粒起到了主要作用。
| 实验操作 | 实验数据 |
| 向烧杯中加入煮沸了的0.1mol/L的BaCl2溶液25mL,再加入25mL植物油,冷却至室温,用pH传感器测定溶液pH随时间(t)的变化曲线 | 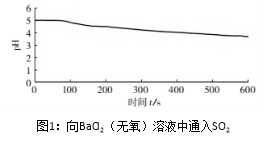
|
| 向烧杯中分别加入25mL 0.1mol/L的BaCl2溶液、Ba(NO3)2溶液,通入SO2 ,用pH传感器分别测定溶液pH随时间(t)变化的曲线。 | 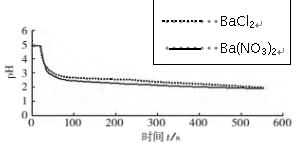 
|
(3)图1,在无氧条件下,BaCl2溶液pH下降的原因是_________。
(4)图2,BaCl2溶液中发生反应的离子方程式为__________。
(5)依据上述图像你得出的结论是 ,说明理由 。
-
(14分)某研究小组将纯净的SO2气体通入0.1mol·L-1的Ba(NO3)2溶液中,得到了BaSO4沉淀,为探究上述溶液中何种微粒能氧化通入的SO2,该小组突出了如下假设:
假设一:溶液中的NO3-
假设二:溶液中溶解的O2
(1)验证假设一
该小组涉及实验验证了假设一,请在下表空白处填写相关实验现象
| 实验步骤 | 实验现象 | 结论 |
| 实验1:在盛有不含O2的25ml0.1mol/LBaCl2溶液的烧杯中,缓慢通入纯净的SO2气体 | | 假设一成立 |
| 实验2:在盛有不含O2的25ml0.1mol/LBa(NO3)2溶液的烧杯中,缓慢通入纯净的SO2气体 | |
(2)为深入研究该反应,该小组还测得上述两个实验中溶液的pH随通入SO2体积的变化曲线入下图
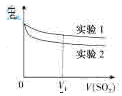
实验1中溶液pH变小的原因是____;V1时,实验2中溶液pH小于实验1的原因是(用离子方程式表示)_________。
(3)验证假设二
请设计实验验证假设二,写出实验步骤,预期现象和结论。
(4)若假设二成立,请预测:在相同条件下,分别通入足量的O2和KNO3,氧化相同的H2SO3溶液(溶液体积变化忽略不计),充分反映后两溶液的pH前者_______(填大于或小于)后者,理由是________
-
某研究小组将纯净的SO2气体通入0.1mol•L﹣1的Ba(NO3)2溶液中,得到了BaSO4沉淀。为探究上述溶液中何种微粒能氧化通入的SO2,该小组提出了如下假设:
假设一:溶液中的NO3-
假设二:溶液中溶解的O2;
(1)验证假设一
该小组设计实验验证了假设一,请在下表空白处填写相关实验现象.
| 实验步骤 | 实验现象 | 结论 |
| 实验1:在盛有不含O2的25mL0.1mol•L﹣1BaCl2溶液的烧杯中,缓慢通入纯净的SO2气体 | _______ | 假设一成立 |
| 实验2:在盛有不含O2的25mL0.1mol•L﹣1Ba(NO3)2溶液的烧杯中,缓慢通入纯净的SO2气体 | ________ |
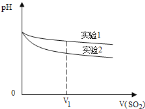
为深入研究该反应,该小组还测得上述两个实验中溶液pH随通入SO2体积的变化曲线如图。实验1中溶液pH变小的原因是____________;V1时,实验2中溶液pH小于实验1的原因是__________。(用离子方程式表示)
(2)验证假设二
请设计实验验证假设二,写出实验步骤、预期现象和结论:
| 实验步骤 | 实验现象 | 结论 |
| __________________ | ______________ | 假设二成立 |
(3)若假设二成立,请预测:在相同条件下,分别用足量的O2和KNO3氧化相同的H2SO3溶液(溶液体积变化忽略不计),充分反应后两溶液的pH前者_____________(填“大于”或“小于”)后者,理由是__________________________。
-
将5mL0.4mol/L的AgNO3溶液与10mL0.3mol/L的BaCl2溶液混合,反应后溶液中离子浓度最大的是
A.Ag+ B.NO3- C.Cl- D.Ba2+
-
下列说法正确的是
A.检验某酸性溶液中Cl-和SO42-,选用试剂及顺序是BaCl2溶液、AgNO3溶液
B.将CO2和SO2混合气体分别通入BaCl2溶液、Ba(NO3)2溶液中,最终都有沉淀生成
C.将铁粉加入FeCl3、CuCl2混合溶液中,充分反应后剩余的固体中不一定有铁
D.用加热分解的方法可将NH4Cl固体和Ca(OH)2固体的混合物分离
-
室温下,下列各组粒子在指定溶液中能大量共存的是
A.Ba(NO3)2 溶液中:SO2、Na+、NH4+、CH3COO-
B.Kw/c(H+)=0.1mol/L的溶液中:K+、Ba2+、C1-、HCO—
C.FeCl2溶液中:H2O2、Mg2+、H+、Cl-
D.含苯酚的水溶液中用::Al3+、NH4+、Br-、SO42-

H2SO3
H++HSO
是氧化SO2的主要微粒



