H2是一种绿色能源,如图装置电解水(添加少量烧碱)制备H2和O2。下列说法错误的是
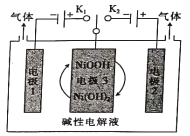
A.关闭K1时,电极1收集H2且电极1附近NaOH溶液浓度减小;
B.关闭K2时,阴极反应为NiOOH+H2O+e-=Ni(OH)2+OH-
C.NaOH增强导电性,可以用稀硫酸(或盐酸)替代烧碱
D.若电极2收集到11200 mL气体(标准状况),则转移2 mol电子
高三化学单选题困难题
H2是一种绿色能源,如图装置电解水(添加少量烧碱)制备H2和O2。下列说法错误的是

A.关闭K1时,电极1收集H2且电极1附近NaOH溶液浓度减小;
B.关闭K2时,阴极反应为NiOOH+H2O+e-=Ni(OH)2+OH-
C.NaOH增强导电性,可以用稀硫酸(或盐酸)替代烧碱
D.若电极2收集到11200 mL气体(标准状况),则转移2 mol电子
高三化学单选题困难题
H2是一种绿色能源,如图装置电解水(添加少量烧碱)制备H2和O2。下列说法错误的是

A.关闭K1时,电极1收集H2且电极1附近NaOH溶液浓度减小;
B.关闭K2时,阴极反应为NiOOH+H2O+e-=Ni(OH)2+OH-
C.NaOH增强导电性,可以用稀硫酸(或盐酸)替代烧碱
D.若电极2收集到11200 mL气体(标准状况),则转移2 mol电子
高三化学单选题困难题查看答案及解析
利用膜技术原理和电化学原理制备少量硫酸和绿色硝化剂N2O5,装置如图所示,下列说法正确的是( )
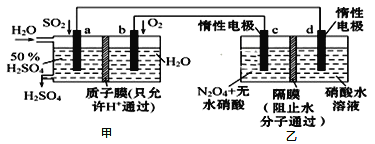
A.电极b反应式是O2+4e-+2H2O=4OH-
B.电解后乙装置d电极附近溶液的pH不变
C.c电极上的电极反应式为N2O4-2e-+H2O=N2O5+2H+
D.甲中每消耗1mol SO2,乙装置中有1mol H+通过隔膜
高三化学单选题中等难度题查看答案及解析
利用膜技术原理和电化学原理制备少量硫酸和绿色硝化剂N2O5,装置如图所示,下列说法正确的是( )
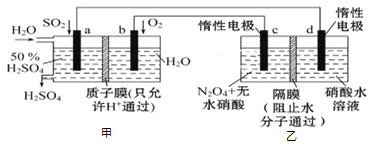
A. 电极b反应式是O2+4e-+2H2O=4OH-
B. 电解后乙装置d电极附近溶液的pH不变
C. c电极上的电极反应式为N2O4-2e-+H2O=N2O5+2H+
D. 甲中每消耗1mol SO2,乙装置中有1mol H+通过隔膜
高三化学单选题中等难度题查看答案及解析
有人设想利用电化学原理制备少量硫酸和绿色硝化剂N2O5,所用装置如图所示,下列说法正确的是
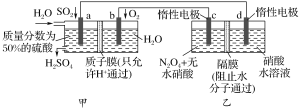
A.图中的甲池为电解池,乙池为原电池
B.a极发生的电极反应为SO2-2e-+2H2O===SO42-+4H+
C.N2O5在c极上产生,c极的电极反应为N2O4-2e-+H2O===N2O5+2H+
D.当消耗标况下2.24 L SO2时,若要维持硫酸的浓度不变则应补充水11.6 mL
高三化学单选题中等难度题查看答案及解析
膜技术原理在化工生产中有着广泛的应用,有人设想利用电化学原理制备少量硫酸和绿色硝化剂N2O5,装置图如下。下列说法不正确的是
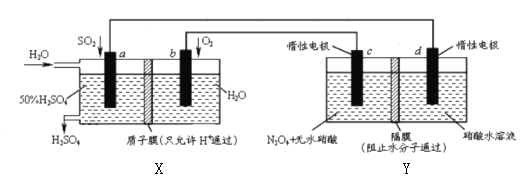
A. X是原电池,能够生产硫酸;Y是电解池,能够生产N2O5
B. C电极的电极反应方程式为N2O4+2HNO3-2e-=2N2O5+2H+
C. 当电路中通过2mole,X、Y中各有2molH+从左边迁移到右边
D. 电路中电子流向为ad
c
b
a形成闭合回路
高三化学单选题中等难度题查看答案及解析
以二甲醚(CH3OCH3)酸性燃料电池为电源,电解饱和食盐水制备氯气和烧碱,设计装置如图所示。已知:a电扱的反应式为O2+4H++4e-=2H2O,下列说法不正确的是
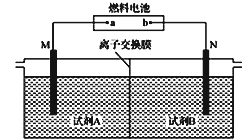
A. b电极的反应式为CH3OCH3+3H2O-12e-==2CO2↑+12H+
B. 试剂A为饱和食盐水,试刑B为NaOH稀溶液
C. 阳极生成1 mol气体时,有1mol离子通过离子交换膜
D. 阴极生成1 mol气体时,理论上导线中流过2 mol e-
高三化学单选题中等难度题查看答案及解析
以二甲醚(CH3OCH3)酸性燃料电池为电源,电解饱和食盐水制备氯气和烧碱,设计装置如图所示。已知:a电扱的反应式为O2+4H++4e-=2H2O,下列说法不正确的是
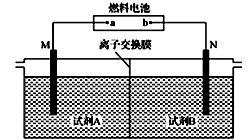
A. b电极的反应式为CH3OCH3+3H2O-12e-==2CO2↑+12H+
B. 试剂A为饱和食盐水,试刑B为NaOH稀溶液
C. 阳极生成1 mol气体时,有1mol离子通过离子交换膜
D. 阴极生成1 mol气体时,理论上导线中流过2 mol e-
高三化学选择题中等难度题查看答案及解析
利用膜技术原理和电化学原理制备少量硫酸和绿色硝化剂N2O5,装置如图所示,下列说法正确的是
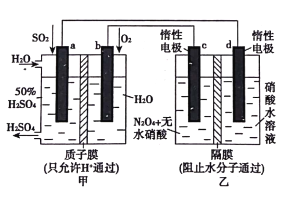
A. 电极b反应式是O2+4e-+2H2O=4OH-
B. 乙装置d电极附近溶液的pH增大
C. c电极上的电极反应式为N2O4-2e-+H2O=N2O5+2H+
D. 每转移2mole-生成2molN2O5和1molH2SO4
高三化学单选题困难题查看答案及解析
高铁酸盐在能源环保领域有广泛用途。用镍 (Ni)、铁作电极电解浓NaOH溶液制备高铁酸钠(Na2FeO4)的装置如图所示。下列说法正确的是( )
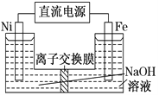
A. 铁是阳极,电极反应为Fe-2e-+2OH-===Fe(OH)2↓
B. 电解一段时间后,镍电极附近溶液的pH减小
C. 每制得1 mol Na2FeO4,理论上可以产生67.2L气体
D. 若离子交换膜为阴离子交换膜,则电解结束后左侧溶液中含有FeO42-
高三化学单选题中等难度题查看答案及解析
高铁酸盐在能源环保领域有广泛用途。用镍 (Ni)、铁作电极电解浓NaOH溶液制备高铁酸钠(Na2FeO4)的装置如图所示。下列说法正确的是
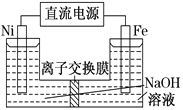
A. 铁是阳极,电极反应为Fe-2e-+2OH-===Fe(OH)2↓
B. 电解一段时间后,镍电极附近溶液的pH减小
C. 每制得1 mol Na2FeO4,理论上可以产生67.2L气体
D. 若离子交换膜为阴离子交换膜,则电解结束后左侧溶液中含有FeO
高三化学单选题中等难度题查看答案及解析