-
CS(NH2)2(硫脲,白色而有光泽的晶体,溶于水,20℃时溶解度为13.6g;在150 ℃时转变成NH4SCN)是用于制造药物、染料、金属矿物的浮选剂等的原料。某化学实验小组同学用Ca(HS)2与CaCN2(石灰氮)合成硫脲并探究其性质。
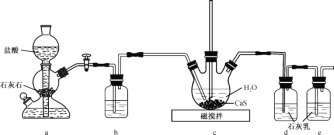
(1)制备Ca(HS)2溶液,所用装置如图(已知酸性:H2CO3>H2S):
①装置a中反应发生的操作为 _________;装置b中盛放的试剂是________ 。
②装置c中的长直导管的作用是________。
(2)制备硫脲:将CaCN2与Ca(HS)2溶液混合,加热至80℃时,可合成硫脲,同时生成一种常见的碱,合适的加热方式是__________;该反应的化学方程式为____________________。
(3)探究硫脲的性质:①取少量硫脲溶于水并加热,验证有NH4SCN生成,可用的试剂是_____(填化学式,下同)
②向盛有少量硫脲的试管中加入NaOH溶液,有NH3放出,检验该气体的方法为 ______。
③可用酸性KMnO4溶液滴定硫脲,已知MnO 被还原为Mn2+,CS(NH2)2被反应为CO2、N2及SO
被还原为Mn2+,CS(NH2)2被反应为CO2、N2及SO ,该反应中氧化剂与还原剂的物质的量之比为_____。
,该反应中氧化剂与还原剂的物质的量之比为_____。
-
硫脲(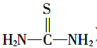 )是一种白色而有光泽的晶体,味苦,可用于制造树脂,也用作橡胶的硫化促进剂以及金属矿物的浮选剂等。回答下列问题:
)是一种白色而有光泽的晶体,味苦,可用于制造树脂,也用作橡胶的硫化促进剂以及金属矿物的浮选剂等。回答下列问题:
(1)硫脲中硫的化合价为_______;与硫脲互为同分异构且能与FeCl3溶液发生显色反应的化合物的化学式为_______
(2)可用H2NCN(氨基腈)与C2H5SH (乙硫醇)反应制备硫脲。氨基腈的电子式为_____
(3)制取氨基腈的传统工艺流程如下:
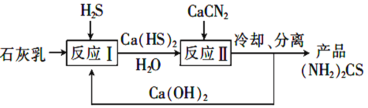
①反应Ⅱ的化学方程式为______
②测定硫脲含量的方法如下:
步骤1 :准确称取a g产品,经溶解等步骤最后在500 mL容量瓶中定容。
步骤2:准确量取20.00 mL配制好的溶液注入碘量瓶中,加入V1 mL c1 mol/L I2的标
准溶液及适量的NaOH溶液,于暗处放置10 min(2NaOH+I2=NaIO+NaI+H2O,
4NaIO+(NH2)2CS+H2O =(NH2)2CO+4NaI+H2SO2)。
步骤3:加水及适量的盐酸,摇匀。
步骤4:用c2 mol/L标准Na2S2O2溶液滴定剩余的I2( I2+2Na2S2O2=2NaI+Na2S4O6) ,加入淀粉溶液,滴定至终点时消耗Na2S2O2溶液V2mL。
“步骤3”加入盐酸的目的_________(用离子方程式说明)。
“步骤4”滴定至终点时的颜色变化是________。
③产品中(NH2)2CS的质量分数为_______ (列出计算式)。
-
硫脲[SC(NH2)2]别名硫代尿素,是一种白色固体,熔点182℃。硫脲可代替氰化物用于提炼金的新工艺。酸性条件下,硫脲在氧化剂(如Fe3+、H2O2、O2)存在下能溶解金,形成配离子Au[SC(NH2)2] 。
。
回答下列问题:
(1)C、N、S三种元素中第一电离能最大的是___(填元素符号)。
(2)Au与Cu同族,价电子排布式为5d106s1,Au位于元素周期表的___区,Au+的价电子排布式为___。
(3)硫脲分子中碳原子的杂化方式为___,σ键和π键数目之比为___。
(4)写出硫脲在硫酸铁存在下溶解金的离子方程式___。
(5)硫脲加热到150℃时可转变成硫氰酸铵(NH4SCN),SCN-的空间构型为___形。
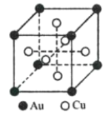
(6)一种铜金合金晶体具有面心立方最密堆积的结构,其晶胞如图所示,则该合金中Au原子与Cu原子个数之比为___。若铜和金的半径分别为apm和bpm,相对原子质量分别为MA和MB,阿伏加德罗常数的值为NA,计算晶体的密度为___g/cm3。
-
用石灰乳、石灰氮(CaCN2)和炼厂气(含H2S)反应,既能净化尾气,又能获得应用广泛的CS(NH2)2(硫脲),其部分工艺流程如下:
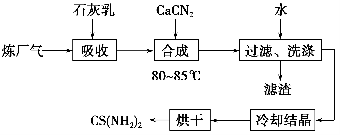
(1)高温下,H2S存在下列反应:2H2S(g)2H2(g)+S2(g),其平衡常数表达式为K=________________。
(2)用石灰乳吸收H2S制取Ca(HS)2需要在低温下进行,其原因是_____________________________________________________;
过滤得到的滤渣可再利用,滤渣的主要成分是________(填化学式)。
(3)合成硫脲需长时间搅拌,并在较高温度(80~85 ℃)下进行,其目的是_______________________________________。
Ca(HS)2与CaCN2在水溶液中合成硫脲的化学方程式为________________________________。
(4)化合物X与硫脲互为同分异构体,X加入FeCl3溶液中,溶液显红色,X的化学式为________________。
-
用石灰乳、石灰氮(CaCN2)和炼厂气(含H2S)反应,既能净化尾气,又能获得应用广泛的CS(NH2)2(硫脲),其部分工艺流程如下:
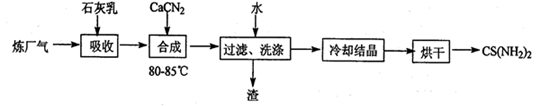
(1)高温下,H2S存在下列反应:2H2S(g)  2H2(g)+S2(g),其平衡常数表达式为K=。
2H2(g)+S2(g),其平衡常数表达式为K=。
(2)用石灰乳吸收H2S制取Ca(HS)2需要在低温下进行,其原因是 ________;过滤得到的滤渣可再利用,滤渣的主要成分是 ________(填化学式)。
(3)合成硫脲需长时间搅拌,并在较高温度(80℃-85℃)下进行,其目的是 ________。
Ca(HS)2与CaCN2在水溶液中合成硫脉的化学方程式为 。
(4)化合物X与硫脲互为同分异构体,X加入FeCl3溶液中,溶液显红色,X的化学式为 ________。
-
某学习小组在实验室模拟工业制备硫氰化钾(KSCN)。实验装置如图:
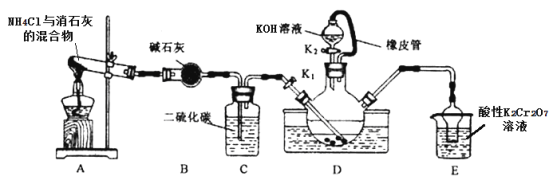
已知:①CS2不溶于水,比水重;NH3 不溶于CS2;②三颈烧瓶内盛放有CS2、水和催化剂。
实验步骤如下:
(1)制备NH4SCN溶液:CS2+3NH3 NH4SCN+ NH4HS(该反应比较缓慢)
NH4SCN+ NH4HS(该反应比较缓慢)
①实验前,经检验装置的气密性良好。三颈烧瓶的下层CS2液体必须浸没导气管口,目的是_____。
②实验开始时打开K1,加热装置A、D,使A中产生的气体缓缓通入D中,至CS2消失。
则:装置A中反应的化学方程式是_____;装置C的作用是______。
(2)制备KSCN溶液:熄灭A处的酒精灯,关闭K1,移开水浴,将装置D继续加热至105℃,当NH4HS完全分解后(NH4HS= H2S↑ + 3NH3↑),打开K2,再缓缓滴加入适量的KOH溶液,发生反应:NH4SCN + KOH= KSCN + NH3↑ +H2O。
小组讨论后认为:实验中滴加入相同浓度的K2CO3溶液比KOH溶液更好,理由是_____。
(3)制备硫氰化钾晶体:先滤去三颈烧瓶中的固体催化剂,再减压蒸发浓缩,冷却结晶______,干燥,得到硫氰化钾晶体。
(4)测定晶体中KSCN的含量:称取10.0g样品配成1000mL溶液量取20.00mL于锥形瓶中,加入适量稀硝酸,再加入几滴Fe(NO3)3溶液做指示剂,用0.1000mol/LAgNO3标准溶液滴定,达到滴定终点时消耗AgNO3标准溶液20.00mL。
①滴定时发生的反应:SCN- + Ag+= AgSCN↓(白色)。则判断达到终点时的方法是____。
②晶体中KSCN的质量分数为____。
-
某校化学兴趣小组在实验室模拟工业制备硫氰化钾(KSCN),实验装置如图所示。
实验步驟如下:
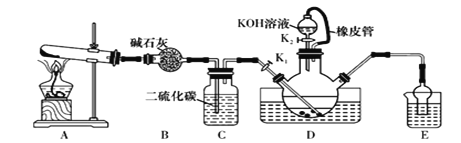
(1)制备NH4SCN溶液:CS2+2NH3 NH4SCN+H2S,该反应进行的比较缓慢,NH3不溶于CS2
NH4SCN+H2S,该反应进行的比较缓慢,NH3不溶于CS2
①实验前,应进行的操作是________________________。三颈烧瓶内盛放有一定量的CS2、水和催化剂,三颈烧瓶的下层CS2液体必须浸没导气管口,目的是_____________________。
②实验开始时打开K1,加热装置A、D,缓慢地向装置D中充入气体。装置A中发生反应的化学方程式是______________________________,装置C的作用可能是_______________。
(2)制备KSCN溶液:移去装置A处的酒精灯,关闭K1,打开K2,利用耐碱分液漏斗边加液边加热,则此时装置D中发生反应的化学方程式是____________________。
(3)制备KSCN晶体:先滤去三颈烧瓶中的固体催化剂,再减压蒸发浓缩,冷却结晶,__________________,得到硫氰化钾晶体。
(4)测定KSCN的含量:称取10.00g样品配成1000mL溶液,量取20.00mL溶液于锥形瓶中,并加入几滴Fe(NO3)3溶液,用0.1000 mol/L AgNO3标准溶液滴定,达到滴定终点时消耗AgNO3标准溶液20.00mL。
①滴定时发生的离子反应为SCN-+Ag+= AgSCN↓,则终点时的现象是________________。
②KSCN的质量分数为______________________。
-
硫氰化钾可用于农药、医药、电镀、化学试剂、检定铁离子、铜和银等。某兴趣小组同学在实验室模拟工业制备硫氰化钾(KSCN),实验装置如图所示。
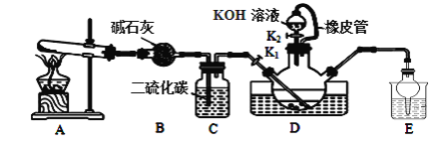
实验步骤如下:
(1)制备NH4SCN溶液:CS2+2NH3 NH4SCN+H2S,该反应进行的比较缓慢,NH3不溶于CS2。
NH4SCN+H2S,该反应进行的比较缓慢,NH3不溶于CS2。
①实验前,应进行的操作是__;三颈烧瓶内盛放有一定量的CS2、水和催化剂。三颈烧瓶的下层CS2液体必须浸没导气管口,目的是__。
②实验开始时打开K1,加热装置A、D,缓慢地向装置D中充入气体。装置A中发生反应的化学方程式是__,装置C的作用可能是__。
(2)制备KSCN溶液:移去装置A处的酒精灯,关闭K1,打开K2,利用耐碱分液漏斗边加液边加热,则此时装置D中发生反应的化学方程式是__。
(3)制备KSCN晶体:先滤去三颈烧瓶中的固体催化剂,再减压蒸发浓缩,冷却结晶,___,得到硫氰化钾晶体。
(4)测定KSCN的含量:称取10.00g样品配成1000mL溶液,量取25.00mL溶液于锥形瓶中,并加入几滴Fe(NO3)3溶液,用0.1000mol·L-1AgNO3标准溶液滴定。经过3次平行试验,达到滴定终点时,消耗AgNO3标准溶液的体积平均为20.00mL。滴定反应的离子方程式为SCN-+Ag+=AgSCN↓。
①判断达到滴定终点的方法是__。
②样品中KSCN的质量分数为__(KSCN的摩尔质量为97g·mol-1,保留4位有效数字)。
-
Ba(NO3)2为无色或白色有光泽的立方晶体,微具吸湿性,有强氧化性,助燃,有毒,可用于生产烟花、信号弹、炸药、陶瓷釉药等。一种利用重晶石(BaSO4)制硝酸钡的工艺流程如下:
I.制BaS
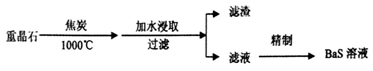
(1)BaS溶液显碱性的原因是__________________(用离子方程式表示);
(2)重晶石与焦炭在高温锻烧时会产生一种还原性气体,此反应中氧化剂与还原剂的物质的量之比为________,每有lmol BaSO4反应,转移的电子数目为________;
II.制Ba(NO3)2
① 取340g50%精制的BaS溶液,置于装有搅拌器、温度计和导气管的三颈烧瓶中
② 在不断搅拌下,慢慢加入浓度为65%的硝酸200g,控制温度为70℃ ,并维持三颈烧瓶内大约100mmHg 的低压,反应30min,结束。请回答:
(3)反应温度控制在70℃ 左右,不宜过高的原因是____________;
(4)三颈烧瓶内维持低压的目的是__________,导出的H2S气体经NaOH溶液吸收可以获得重要的工业原材料硫化碱(Na2S), Na2S极易水解而变质,实验室配制Na2S溶液时,需在配好的溶液里加人少量的__________;
(5)依据下表中Ba(NO3)2的溶解度数据,所得溶液经_______、________,过滤、冰水洗涤、干燥后可获得纯净的Ba(NO3)2晶体。

-
已知草酸晶体(H2C2O4·nH2O)在101 ℃时开始熔化,150 ℃时开始升华,175 ℃时开始分解;草酸钙和草酸氢钙均为白色不溶物。某研究性学习小组的同学选用下面的某些仪器(夹持装置略去)进行“草酸晶体受热分解的部分产物的验证”的实验:

(1)仪器X的名称是________,实验中X的作用是____________________,甲同学进行实验时仪器的接口顺序为:________。
①若B中溶液变浑浊,则证明分解的产物中有________;若F中的固体由黑色变成红色,则说明分解产物中有________。
②彻底处理掉本实验中的尾气的最好方法是______________________。
③假若上述现象均已发生,则草酸晶体分解的化学方程式为__________________________________________________。
(2)乙同学进行实验时仪器的接口连接顺序为abcdef,实验过程中发现D中有黑色固体生成,经查阅资料知此固体为金属单质,则D中反应的化学方程式为______________________________________________________。
(3)丙同学待甲同学的实验结束后,将烧瓶内的液体与B中的沉淀混合在一起,结果发现有无色无味的气体及新的固体生成,由此他认为烧瓶中还存在没有分解的草酸且草酸是强酸,请对他的结论进行评价___________。
(4)设计一种方案确定草酸钙中是否含有碳酸钙:_________________。

被还原为Mn2+,CS(NH2)2被反应为CO2、N2及SO
,该反应中氧化剂与还原剂的物质的量之比为_____。
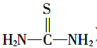 )是一种白色而有光泽的晶体,味苦,可用于制造树脂,也用作橡胶的硫化促进剂以及金属矿物的浮选剂等。回答下列问题:
)是一种白色而有光泽的晶体,味苦,可用于制造树脂,也用作橡胶的硫化促进剂以及金属矿物的浮选剂等。回答下列问题:








