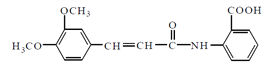-
硫代硫酸钠( )是一种解毒药,用于氰化物、砷、汞、铅、铋、碘等中毒,临床常用于治疗荨麻疹,皮肤瘙痒等病症。硫代硫酸钠在中性或碱性环境中稳定,在酸性溶液中分解产生
)是一种解毒药,用于氰化物、砷、汞、铅、铋、碘等中毒,临床常用于治疗荨麻疹,皮肤瘙痒等病症。硫代硫酸钠在中性或碱性环境中稳定,在酸性溶液中分解产生 和
和 。
。
实验Ⅰ. 的制备。工业上可用反应:
的制备。工业上可用反应: 制得,实验室模拟该工业过程的装置如图所示。
制得,实验室模拟该工业过程的装置如图所示。
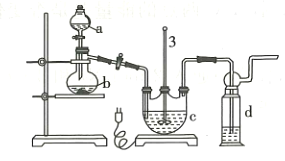
(1)仪器a的名称是__________,仪器b的名称是_____________。b中利用质量分数为70%~80%的 溶液与
溶液与 固体反应制备
固体反应制备 反应的化学方程式为_______________________。c中试剂为________。
反应的化学方程式为_______________________。c中试剂为________。
(2)实验中要控制 的生成速率,可以采取的措施有_________________________(写出一条)。
的生成速率,可以采取的措施有_________________________(写出一条)。
(3)为了保证硫代硫酸钠的产量,实验中通入的 不能过量,原因是_________________________。
不能过量,原因是_________________________。
实验Ⅱ.探究 与金属阳离子的氧化还原反应。
与金属阳离子的氧化还原反应。
资料: (紫黑色)
(紫黑色)
| 装置 | 试剂X | 实验现象 |
| 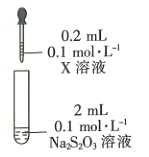
|  溶液 溶液
| 混合后溶液先变成紫黑色,30s后溶液几乎变为无色 |
(4)根据上述实验现象,初步判断最终 被
被 还原为
还原为 ,通过________________________(填操作、试剂和现象),进一步证实生成了
,通过________________________(填操作、试剂和现象),进一步证实生成了 。
。
-
硫代硫酸钠(Na2S2O3)是一种解毒药,用于氟化物、砷、汞、铅、锡、碘等中毒,临床常用于治疗荨麻疹,皮肤瘙痒等病症.硫代硫酸钠在中性或碱性环境中稳定,在酸性溶液中分解产生S和SO2
实验I:Na2S2O3的制备。工业上可用反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2制得,实验室模拟该工业过程的装置如图所示:
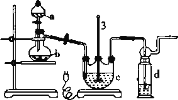
(1)仪器a的名称是_______,仪器b的名称是_______。b中利用质量分数为70%〜80%的H2SO4溶液与Na2SO3固体反应制备SO2反应的化学方程式为_______。c中试剂为_______
(2)实验中要控制SO2的生成速率,可以采取的措施有_______ (写出一条)
(3)为了保证硫代硫酸钠的产量,实验中通入的SO2不能过量,原因是_______
实验Ⅱ:探究Na2S2O3与金属阳离子的氧化还原反应。
资料:Fe3++3S2O32-⇌Fe(S2O3)33-(紫黑色)
| 装置 | 试剂X | 实验现象 |
| 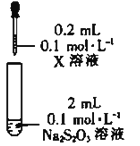
| Fe2(SO4)3溶液 | 混合后溶液先变成紫黑色,30s后几乎变为无色 |
(4)根据上述实验现象,初步判断最终Fe3+被S2O32-还原为Fe2+,通过_______(填操作、试剂和现象),进一步证实生成了Fe2+。从化学反应速率和平衡的角度解释实验Ⅱ的现象:_______
实验Ⅲ:标定Na2S2O3溶液的浓度
(5)称取一定质量的产品配制成硫代硫酸钠溶液,并用间接碘量法标定该溶液的浓度:用分析天平准确称取基准物质K2Cr2O7(摩尔质量为294g∙mol-1)0.5880g。平均分成3份,分别放入3个锥形瓶中,加水配成溶液,并加入过量的KI并酸化,发生下列反应:6I-+Cr2O72-+14H+ = 3I2+2Cr3++7H2O,再加入几滴淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应I2+2S2O32- = 2I- + S4O62-,三次消耗 Na2S2O3溶液的平均体积为25.00 mL,则所标定的硫代硫酸钠溶液的浓度为_______mol∙L-1
-
硫代硫酸钠(Na2S2O3)是一种解毒药,用于氟化物、砷、汞、铅、锡、碘等中毒,临床常用于治疗荨麻疹,皮肤瘙痒等病症.硫代硫酸钠在中性或碱性环境中稳定,在酸性溶液中分解产生S和SO2
实验I:Na2S2O3的制备。工业上可用反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2制得,实验室模拟该工业过程的装置如图所示:
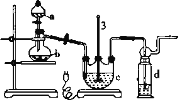
(1)仪器a的名称是_______,仪器b的名称是_______。b中利用质量分数为70%〜80%的H2SO4溶液与Na2SO3固体反应制备SO2反应的化学方程式为_______。c中试剂为_______
(2)实验中要控制SO2的生成速率,可以采取的措施有_______ (写出一条)
(3)为了保证硫代硫酸钠的产量,实验中通入的SO2不能过量,原因是_______
实验Ⅱ:探究Na2S2O3与金属阳离子的氧化还原反应。
资料:Fe3++3S2O32-⇌Fe(S2O3)33-(紫黑色)
| 装置 | 试剂X | 实验现象 |
| 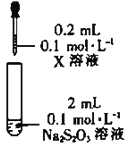
| Fe2(SO4)3溶液 | 混合后溶液先变成紫黑色,30s后几乎变为无色 |
(4)根据上述实验现象,初步判断最终Fe3+被S2O32-还原为Fe2+,通过_______(填操作、试剂和现象),进一步证实生成了Fe2+。从化学反应速率和平衡的角度解释实验Ⅱ的现象:_______
实验Ⅲ:标定Na2S2O3溶液的浓度
(5)称取一定质量的产品配制成硫代硫酸钠溶液,并用间接碘量法标定该溶液的浓度:用分析天平准确称取基准物质K2Cr2O7(摩尔质量为294g∙mol-1)0.5880g。平均分成3份,分别放入3个锥形瓶中,加水配成溶液,并加入过量的KI并酸化,发生下列反应:6I-+Cr2O72-+14H+ = 3I2+2Cr3++7H2O,再加入几滴淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应I2+2S2O32- = 2I- + S4O62-,三次消耗 Na2S2O3溶液的平均体积为25.00 mL,则所标定的硫代硫酸钠溶液的浓度为_______mol∙L-1
-
药物利喘贝(结构如下)主要用于荨麻疹、皮肤瘙痒等病症的治疗,下列关于该有机物的说法不正确的是
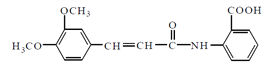
A. 分子式是C18H17O5N B. 一定存在顺反异构体
C. 一定能发生聚合反应 D. 一定能发生银镜反应
-
化学与生产、 生活密切相关。下列说法正确的是
A. 砒霜的主要成分是三硫化二砷
B. 氢氧化铝和碳酸钠均可用于治疗胃酸过多
C. 过量服用阿司匹林引起酸中毒后,可用静脉注射NaHCO3溶液的方法解毒
D. 铜单质制成的“纳米铜”在空气中能燃烧,说明“纳米铜”的金属性比铜片强
-
化学与生产、 生活密切相关。下列说法正确的是
A.砒霜的主要成分是三硫化二砷
B.氢氧化铝和碳酸钠均可用于治疗胃酸过多
C.过量服用阿司匹林引起酸中毒后,可用静脉注射NaHCO3溶液的方法解毒
D.铜单质制成的“纳米铜”在空气中能燃烧,说明“纳米铜”的金属性比铜片强
-
(15分)硫代硫酸钠俗称保险粉,又名“大苏打”。可用于照相业作定影剂、纸浆漂白作脱氯剂,也可用于氰化物、砷、汞、铅、铋、碘等中毒的治疗,也是一种常用的实验试剂。
I.已知:Na2S2O3 + H2SO4 = Na2SO4 + S↓+ SO2 + H2O,某研究小组依据该反应探究外界条件对反应速率的影响,设计实验如下:
| 实验 编号 | 实验温度 /℃ | Na2S2O3 | H2SO4 | 蒸馏水体积 /mL |
| 体积/mL | 浓度/ mol·L-1 | 体积/mL | 浓度/ mol·L-1 |
| ① | 25 | 10 | 0.1 | 10 | 0.1 | 0 |
| ② | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
| ③ | 25 | 5 | 0.2 | 10 | 0.2 | 5 |
| ④ | 50 | 5 | 0.1 | 10 | 0.1 | 5 |
| ⑤ | 50 | 10 | 0.2 | 5 | 0.2 | 5 |
| | | | | | |
下列有关说法正确的是
A.实验①和②探究其他条件不变时Na2S2O3浓度对相关反应速率的影响
B.实验①和③溶液变浑浊的时间相同
C.其他条件不变时,探究温度对化学反应速率的影响,应选择实验③和⑤
D.该同学在实验中采用的研究方法是实验比较法
II.实验室用SO2通入Na2S和Na2CO3的混合溶液中来制备硫代硫酸钠。反应原理为:
2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2
本实验对Na2S纯度要求较高,利用图1所示的装置可将工业级的Na2S提纯。已知Na2S常温下微溶于酒精,加热时溶解度迅速增大,杂质不溶于酒精。提纯过程为:将已称量好的工业级Na2S放入圆底烧瓶中,加入一定质量的酒精和少量水。按图1所示装配所需仪器,向冷凝管通入冷却水,同时水浴加热。待烧瓶中固体不再减少时,停止加热。将烧瓶取下,立即趁热过滤,再冷却结晶,过滤。将所得固体洗涤、干燥,得到Na2S·9H2O晶体。
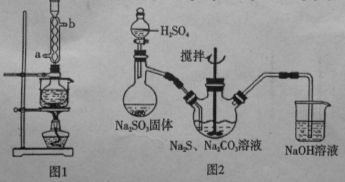
(1)在提纯过程中“趁热过滤”操作的目的是 ;
(2)用图2所示装置制取Na2S2O3,其中盛放Na2SO3固体的玻璃仪器名称是 ,NaOH溶液的作用是 。
(3)保险粉样品中Na2S2O3·5H2O的纯度(质量分数)可通过氧化还原滴定法测定,相关反应方程式为
2Na2S2O3+I2=2NaI+Na2S4O6。
准确称取W g样品于锥形瓶中,用适量蒸馏水溶解,并滴加淀粉溶液作指示剂。用0.1000 mol•L¯1碘的标准溶液进行滴定。
请回答:
①到达滴定终点的标志 ;
②滴定起始和终点的液面位置如图,则消耗碘的标准溶液体积为 mL,产品的纯度为 (设Na2S2O3•5H2O相对分子质量为M)。
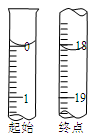
③若滴定时振荡不充分,刚看到溶液局部变色就停止滴定,则会使样品中Na2S2O3·5H2O的纯度的测量结果 (填“偏高”、“偏低”或“不变”)。
-
下列有关化学与生活的说法错误的是( )
A.用可溶性的铝盐和铁盐对水进行杀菌消毒
B.用石灰、碳酸钠等碱性物质处理废水中的酸
C.牛奶、鸡蛋清均可用于重金属中毒解毒
D.碘酒、双氧水均可用于伤口消毒
-
下列说法正确的是
A.发酵粉中主要含有氢氧化钠,能使焙制出的糕点疏松多孔
B.碘盐中的碘可以直接用淀粉检验
C.碳酸氢钠、碳酸钙、碳酸镁、氢氧化铝等可用于治疗胃酸过多
D.硫酸氢钠属于盐类,其水溶液显中性
-
Na2S2O3可用作氰化物中毒的解毒剂,易溶于水,几乎不溶于乙醇。取Na2SO3(s)、S、蒸馏水于烧杯中,在105℃左右反应后过滤Ⅰ,将滤液Ⅰ浓缩、冷却,待晶体析出后过滤Ⅱ、洗涤,低温干燥可得Na2S2O3·5H2O晶体。下列说法错误的是
A.采用酒精灯加热时需使用外焰加热
B.将滤液Ⅰ浓缩至溶液变浑浊,再冷却可析出晶体
C.反应原理为Na2SO3+S=Na2S2O3
D.过滤Ⅱ后得到的晶体先浓硝酸洗后水洗
)是一种解毒药,用于氰化物、砷、汞、铅、铋、碘等中毒,临床常用于治疗荨麻疹,皮肤瘙痒等病症。硫代硫酸钠在中性或碱性环境中稳定,在酸性溶液中分解产生
和
。
的制备。工业上可用反应:
制得,实验室模拟该工业过程的装置如图所示。

溶液与
固体反应制备
反应的化学方程式为_______________________。c中试剂为________。
的生成速率,可以采取的措施有_________________________(写出一条)。
不能过量,原因是_________________________。
与金属阳离子的氧化还原反应。
(紫黑色)
被
还原为
,通过________________________(填操作、试剂和现象),进一步证实生成了
。