-
硼是一种奇特的元素,它来自超新星爆发和宇宙射线的散列辐射。
(1)写出BF3电子式___________,B与F形成共价键时,共用电子对偏向_____原子,判断依据是_________________。
(2)硼酸(H3BO3)在水中电离出阴离子[B(OH)4]-,请写出硼酸的电离方程式___________。
高三化学填空题简单题查看答案及解析
-
下列说法中正确的是
A. CO2、NH3、BF3中,所有原子都满足最外层8电子的稳定结构
B. 在元素周期表中金属和非金属交界处可以找到半导体材料
C. 由非金属元素组成的化合物一定是共价化合物
D. 第ⅠA族元素和第ⅦA 族元素的原子之间都能形成离子键
高三化学单选题简单题查看答案及解析
-
如图为元素周期表短周期的一部分,下列有关A、B、C、D四种元素的叙述中不正确的是( )

A.A、C两元素形成的化合物都为共价化合物
B.AD2的电子式为
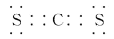
C.B、C形成的化合物BC中所含化学键为非极性共价键
D.B2的结构式为N≡N
高三化学选择题中等难度题查看答案及解析
-
2011年3月日本福岛核电站发生泄漏,产生的核辐射部分来自
。下列说法正确的是
A.
与
互为同素异形体
B.
的中子数与电子数的差值是78
C.在我国加碘食盐中加的是碘酸钾
D.碘元素位于元素周期表第四周期第ⅦA族
高三化学选择题中等难度题查看答案及解析
-
下列说法正确的是
A.BF3和NCl3中,每个原子的最外层都具有8电子稳定结构
B.金刚石和石英晶体的熔点差别大的主要原因是共价键键长不同
C.NaOH熔化的过程中,既破坏了离子键又破坏了共价键
D.常温常压下,H2O是液态,H2S是气态,说明H2O的热稳定性更好
高三化学单选题中等难度题查看答案及解析
-
下列说法正确的是
A. 水气化和水分解两个变化过程中都需破坏共价键
B. 在O2、CO2和SiO2中,都存在共价键,它们均由分子构成
C. CCl4、BF3分子中每个原子的最外层都具有8电子稳定结构
D. H2和Cl2在光照条件反应生成HCl,一定有共价键的断裂和形成
高三化学单选题中等难度题查看答案及解析
-
科学家分析,地球原始大气中的COS(羰基硫)对氨基酸缩合形成多肽的反应有催化作用,对生命起源起到重要作用。
(1)写出COS的电子式________,C与O形成共价键时,共用电子对会偏向____原子,判断依据是___________。
(2)已知 COS(g)+ H2O(g)
H2S(g)+ CO2(g) ΔH1 = - 34kJ/mol
CO(g)+ H2O(g)
H2(g)+ CO2(g) ΔH2 = - 41kJ/mol
写出H2S与CO反应生成 COS 的热化学方程式:_________;100℃ 时将CO与H2S按物质的量比为 1:1 充入反应器中,达平衡后CO的转化率α = 33.3%,此时反应的平衡常数K =______。
(3)在充有催化剂的恒压密闭容器中进行反应。 设起始充入的 n(CO):n(H2S)=m,相同时间内测得H2S转化率与m和温度(T)的关系如图所示。
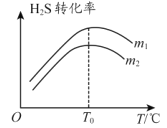
①m1________m2。(填“ > ”、“ < ”或“ = ”)
②温度高于 T0时,H2S 转化率减小的可能原因为________。
A 反应停止了
B 反应的 ΔH 变大
C 反应达到平衡
D 催化剂活性降低
高三化学综合题中等难度题查看答案及解析
-
四种短周期元素W、R、P、Q的原子序数依次增大,W的一种核素没有中子,R、Q同主族.R元素原子的最外层电子数是内层电子数的3倍,P元素与R元素形成的常见化合物中既含有离子键又含有非极性共价键。下列说法不正确的是( )
A. Q元素形成的酸一定是强酸
B. P 与R形成化合物中,阴、阳离子个数比一定为l:2
C. 原子半径:W < R < Q < P
D. 沸点:W2R > W2Q
高三化学选择题简单题查看答案及解析
-
四种短周期元素W、R、P、Q的原子序数依次增大,W的一种核素没有中子,R、Q同主族,R元素原子的最外层电子数是内层电子数的3倍,P元素与R元素形成的常见化合物中既含离子键又含非极性共价键。下列说法不正确的是
A.沸点:W2R>W2Q B.P与R形成化合物中,阴、阳离子个数比一定为1:2
C.原子半径:W<R<Q<P D.Q元素形成的酸一定是强酸
高三化学选择题中等难度题查看答案及解析
-
四种短周期元素W、R、P、Q的原子序数依次增大,W的一种核素没有中子,R、Q同主族,R元素原子的最外层电子数是内层电子数的3倍,P元素与R元素形成的常见化合物中既含离子键又含非极性共价键。下列说法不正确的是( )
A. Q元素形成的酸一定是强酸
B. P与R形成化合物中,阴、阳离子个数比一定为1:2
C. 原子半径:W<R<Q<P
D. 沸点:W2R>W2Q
高三化学单选题中等难度题查看答案及解析