-
臭氧(O3)主要分布在大气层的平流层中,能够吸收紫外线,被称为地球的保护伞。回答下列问题:
(1)NOx对臭氧层的破坏作用极大,已知:①NO+O3=NO2+O2 K1;NO2+O2=NO+O3; K2;③O2+O=O3 K3,反应2O3=3O2的平衡常数K=_______ (用K1、K2、K3表示),写出一种保护臭氧层的措施:__________。
(2)用臭氧氧化烟气中的SO2的主要反应为SO2(g)+O3(g)=SO3(g)+O2(g) △H,已知①2SO2(g)+O2(g)=2SO3(g) △H1=-198kJ/mol,②2O3(g)=3O2(g) △H2=+284.2kJ/mol
①上述反应中△H= ____kJ•mol-1。
②一定温度下,向2L固定容积的密闭容器中加入2molO3和2molSO2发生上述反应,5min后达到平衡,测得容器中含有0.4mol•L-1SO3,此时SO2的转化率为_______,欲提高O3的利用率可采取的措施有_______(填字母)。
a.适当增大压强 b.升高温度 c.使用优质催化剂 d.及时分离出SO3
(3)工业上用CaSO3悬浊液吸收上述转化生成的SO3可制备石膏。已知:298K时Ksp(CaSO4)=9.0×10-6,Ksp(CaSO3)=1.5×10-7,向1LCaSO3悬浊液中加入Na2SO4,若有0.1molCaSO3参与反应,则需加入_______molNa2SO4。
 ,
,
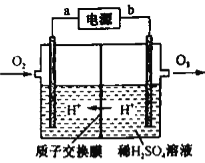
(4)工业上可采用惰性电极电极电解稀硫酸的方法制备O3,反应装置如上图所示,电源的a极为_____极,通入O2的电极反应式为_______。
-
某商品的广告词是“臭氧,世界上最强大的消毒剂”。下列有关叙述正
确的是( )
A.臭氧与氧气是同分异构体,二者的转化属于化学变化
B.大气平流层中的臭氧吸收紫外线,保护地球上的生物
C.臭氧有毒,所以不能用于水的净化
D.因为臭氧分解生成氧气,所以空气中臭氧的含量越高越好
-
根据以下叙述,回答1~2小题.
1995年诺贝尔化学奖授予致力于研究臭氧层被破坏问题的三位环境化学家.大气中的臭氧层可滤除大量的紫外光,保护地球上的生物.氟利昂(如CCl2F2可在光的作用下分解,产生Cl原子,Cl原子会对臭氧层产生长久的破坏作用(臭氧的分子式为O3).有关反应为:O3 O2+O Cl+O3→ClO+O2 ClO+O→O2 总反应 2O3→3O2在上述臭氧变成氧气的反应过程中,Cl是( )
O2+O Cl+O3→ClO+O2 ClO+O→O2 总反应 2O3→3O2在上述臭氧变成氧气的反应过程中,Cl是( )
A.反应物
B.生成物
C.中间产物
D.催化剂
-
运用化学知识判断,下列说法正确的是
A.地沟油的主要成分是高级脂肪酸甘油酯,可食用
B.NOx、SO2、CO2、PM2.5颗粒都会导致酸雨
C.高空臭氧层吸收太阳紫外线,保护地球生物;低空过量臭氧是污染气体,对人体有害
D.石油化工中的分馏、裂化、裂解都是通过化学反应来获得轻质油、气态烯烃
-
空气质量高低直接影响着人类的生产和生活。《空气质量日报》中空气污染指数的项目有SO2、 CO、NOx、O3和可吸入颗粒物等。下列说法不正确的是 ( )
A.大气中的臭氧层对地球有很好的保护作用,所以大气中含有大量O3对人体有益
B.在催化剂作用下,CO和NOx可转化为无毒物质
C.血红蛋白中含有Fe2+,NO、CO容易与血红蛋白结合成稳定物质而使人中毒
D.SO2、NOx的大量排放会导致酸雨的产生
-
臭氧(O3)集中在离地面20~25 km以上的大气平流层。臭氧可使人类和生物免受太阳紫外线辐射的伤害,但目前臭氧层正受到破坏。以下因素中:①喷气式飞机的尾气排放 ②冷冻剂——氟利昂的泄漏 ③可燃物燃烧产生大量CO2,其中可能危害臭氧层的是( )
A.①②③ B.①③
C.②③ D.①②
-
1995年诺贝尔化学奖授予致力研究臭氧层被破坏问题的三位环境化学家,大气中的臭氧层可滤除大量的紫外光,保护地球上的生物。氟利昂可在光的作用下分解,产生Cl原子,CL原子会对臭氧层产生长久的破坏作用(臭氧层为O3)
(1)在上述反应中,Cl是( )
A、反应物 B、生成物 C、中间产物 D、催化剂
(2)O3和O2是( )
A、同分异构体 B、同系物 C、氧的同素异行体 D、氧的同位素
-
氟氯烃对大气臭氧层有破坏作用。据报道南极上空的臭氧空洞已有三个中国的面积!科学家们呼吁人类要保护臭氧层。大气层中,臭氧的作用是( )
A.吸收CO2 B.补充O2
C.吸收红外线 D.吸收紫外线
-
1995年诺贝尔化学奖授予致力于研究臭氢层被破坏问题的三位环境化学家。大气中的臭氧层可滤除大量的紫外线,保护地球上的生物。氟里昂(如CCl2F2)可在光的作用下分解,产生Cl原子,Cl原子会对臭氧层产生长久的破坏作用(臭氧的分子式为O3)。有关反应为:O3 O2+O Cl+O3―→ClO+O2 ClO+O―→Cl+O2 总反应:2O3―→3O2
O2+O Cl+O3―→ClO+O2 ClO+O―→Cl+O2 总反应:2O3―→3O2
(1)在上述臭氧变成氧气的反应过程中,Cl是( )
A.反应物 B.生成物 C.中间产物 D.催化剂
(2)O3和O2是( )
A.同分异构体 B.同系物
C. 氧的同素异形体 D.氧的同位素
-
氮氧化物NOx(主要指NO和NO2)会形成酸雨、光化学烟雾,破坏臭氧层,是大气主要污染物之一,有效去除大气中的NOx是环境保护的重要课题。
(1)研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s) NaNO3(s)+ClNO(g) K1 ΔH1<0 (Ⅰ)
NaNO3(s)+ClNO(g) K1 ΔH1<0 (Ⅰ)
2NO(g)+Cl2(g) 2ClNO(g) K2 ΔH2<0 (Ⅱ)
2ClNO(g) K2 ΔH2<0 (Ⅱ)
①4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=____(用K1、K2表示)。
2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=____(用K1、K2表示)。
②为研究不同条件对反应(Ⅱ)的影响,在恒温条件下,向2 L恒容密闭容器中加入0.2 mol NO和0.1 mol Cl2,10 min时反应(Ⅱ)达到平衡。测得10 min内υ(ClNO)=7.5×10-3mol·L-1·min-1,则平衡后NO的转化率α1=____。其他条件保持不变,反应(Ⅱ)在恒压条件下进行,平衡时NO的转化率α2____α1(填“>”“<”或“=”),平衡常数K2____(填“增大”“减小”或“不变”)。
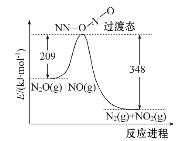
(2)NO能与N2O反应生成N2和NO2,反应的能量变化如下图所示,若生成1 mol N2,其ΔH=____kJ·mol-1。
(3)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图甲所示。
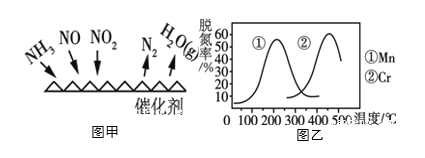
①由图甲可知,SCR技术中的氧化剂为_____________。当NO2与NO的物质的量之比为1:1时,与足量氨气在一定条件下发生脱氮反应。该反应的化学方程式为______________。
②图乙是不同催化剂Mn和Cr在不同温度下对应的脱氮率,由图可知工业选取的最佳催化剂为________。
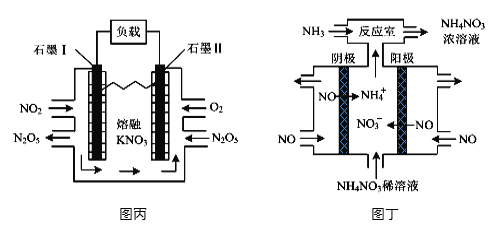
(4)利用电化学装置可消除氮氧化物污染,变废为宝。图丙装置实现的能量转化形式是_______。图丁为电解NO制备NH4NO3的装置,该装置中阳极的电极反应式为___________________。
 ,
,

