-
对铁及铁的化合物颜色描述错误的是( )
A. 还原铁粉——银白色 B. Fe(OH)3——红褐色
C. Fe(SCN)3溶液——血红色 D. FeSO4溶液——浅绿色
难度: 简单查看答案及解析
-
常温下,Fe、Al在浓硫酸中钝化,浓硫酸表现了( )
A. 难挥发性 B. 吸水性 C. 脱水性 D. 强氧化性
难度: 简单查看答案及解析
-
与“用自来水制取蒸馏水”的原理相似的是( )
A. 石油裂化 B. 石油分馏 C. 煤干馏 D. 纸层析
难度: 简单查看答案及解析
-
下图喷泉实验的现象与下列性质无关的是( )

A. 氨易溶于水 B. 氨能与水反应
C. 氨水显碱性 D. 氨易液化
难度: 简单查看答案及解析
-
常温下,表面能自然形成氧化层且使金属不被继续氧化的是( )
A. Au B. Na C. Al D. Fe
难度: 简单查看答案及解析
-
下列有关乙炔的说法,错误的是( )
A. 工业上制备炭黑的原料 B. 含极性键的非极性分子
C. 能发生氧化反应 D. 分子中所有原子共直线
难度: 简单查看答案及解析
-
对碳原子核外两个未成对电子的描述,正确的是( )
A. 电子云形状不同 B. 自旋方向相同
C. 能量不同 D. 在同一轨道
难度: 简单查看答案及解析
-
共价化合物不可能( )
A. 硬度很大 B. 常温下为气态
C. 由一种原子直接构成 D. 溶于水产生阴阳离子
难度: 简单查看答案及解析
-
属于人工固氮的是( )
A.
B.
C.
D.
难度: 简单查看答案及解析
-
下列反应中的能量变化与图示一致的是( )
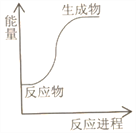
A. 盐酸和NaOH溶液混合
B. CH4在空气中燃烧
C. Al与Fe2O3反应
D. 电解水得到H2和O2
难度: 简单查看答案及解析
-
涉及到Al(OH)3弱酸性的是( )
A. Al溶于强碱溶液 B. Al溶于强酸溶液
C. AlCl3溶液和氨水混合 D. Al(OH)3受热分解
难度: 中等查看答案及解析
-
对C2H6和C5H12的分析错误的是( )
A. 互为同系物
B. C2H6失去1个H得到的乙基只有一种结构
C. C5H12的一氯代物可能只有一种
D. 2,2-二甲基丙烷的沸点高于其同分异构体的沸点
难度: 简单查看答案及解析
-
实验室制备乙酸丁酯的装置如图所示,下列分析错误的是( )
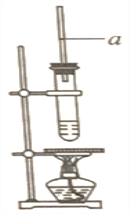
A. 导气管
起到冷凝回流的作用
B. 反应后生成的乙酸丁酯仍在试管中
C. 充分反应后在试管中得到纯净的乙酸丁酯
D. 制乙酸丁酯的反应温度超过100℃不能用水浴加热
难度: 简单查看答案及解析
-
侯氏制碱法,向母液中通入NH3,其目的不是为了( )
A. 增大
浓度 B. 生成NaHCO3
C. 析出NH4Cl晶体 D. 降低
浓度
难度: 中等查看答案及解析
-
有机物M:
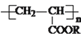 可用作涂料。对M的分析错误的是( )
可用作涂料。对M的分析错误的是( )A. M中含酯基 B. M可通过加聚反应制得
C.
个M水解得到
个RCOOH D. M的水解产物中仍有高分子化合物
难度: 简单查看答案及解析
-
用图中所示装置进行实验,实验现象与预测不一致的是( )

①中的物质
②中的物质
预测现象
A
饱和亚硫酸
蓝色石蕊试液
②中溶液先变红色又褪色
B
饱和氯水
湿润红纸条
②中红纸条褪色
C
浓双氧水
H2S溶液
②中有淡黄色沉淀
D
浓氨水
浓盐酸
③中有白烟
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
84消毒液是一种高效消毒剂,其主要成分是NaClO。对84消毒液的叙述错误的是( )
A.
能转化为具有杀菌消毒能力的HClO
B. 加少量NaOH可提高其杀菌效果
C. 应低温、避光、密封保存
D. 使用时空气中的CO2会参与反应
难度: 简单查看答案及解析
-
实验室用浓硫酸和乙醇制乙烯的装置如图所示,对下列操作或现象描述正确的是( )

A. 圆底烧瓶中先加浓硫酸再加入乙醇
B. 实验得到的气体能使溴水褪色说明有乙烯生成
C. 反应中圆底烧瓶内会产生黑色固体
D. 用排水法或向下排空气法收集乙烯
难度: 简单查看答案及解析
-
对金属腐蚀及防护的表述正确的是( )
A. 金属腐蚀的本质:金属失电子发生还原反应
B. 牺牲阳极的阴极保护法:被保护的金属应做负极
C. 外加电流阴极保护法:被保护的金属应与电源正极相连
D. 金属表面涂油漆:可避免金属与电解质溶液接触
难度: 简单查看答案及解析
-
25℃,有两种盐的稀溶液,分别是
mol/L NaX溶液和
mol/L NaY溶液,下列判断错误的是( )
A. 若
,测得
,则溶液中的
B. 若
,测得
,则溶液中的
C. 若
,且
,则酸性:
D. 若
,并测得
,则HX是强酸,HY是弱酸
难度: 困难查看答案及解析

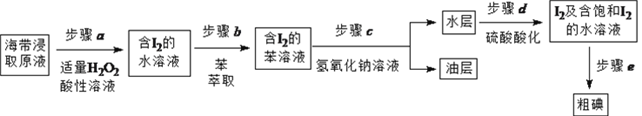

 中的溴元素?____________________________________。
中的溴元素?____________________________________。 也可表示为
也可表示为 也可表示为
也可表示为