-
化学与科学、技术、社会和环境密切相关。下列有关说法正确的是
A.煤的气化和液化是物理变化,煤的干馏是化学变化
B.乙醇、过氧化氢、次氯酸钠等消毒液均可以将病毒氧化而达到消毒的目的
C.氢氧燃料电池发电,比氢气直接在空气中燃烧发电能量转换率高
D.合成氨反应N2(g) +3H2(g)
2NH3(g) OH<0,加入催化剂能加快反应速率并提高转化率
难度: 简单查看答案及解析
-
设NA为阿伏加德罗常数的值.下列叙述正确的是
A.标准状况下,11.2 L乙醇中含有的碳氢键数为2.5NA
B.标准状况下电解硫酸铜溶液时,阳极每生成气体3.36 L,转移电子数为0.6NA
C.标准状况下,30gNO和16gO2混合所生成的气体分子数为NA
D.1mol氯气参加氧化还原反应,转移的电子数一定为2NA
难度: 中等查看答案及解析
-
下列有关化学用语,正确的是
A.食盐中阴离子的结构示意图为
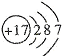
B.氧化亚铁溶于足量稀硝酸的离子方程式: FeO+2H+=Fe2++H2O
C.NaHS水解的离子方程式:HS-十H2O
H3O++S2-
D.用惰性电极电解氯化钠溶液,阳极电极反应式: 2Cl--2e-=Cl2↑
难度: 简单查看答案及解析
-
龙胆酸甲醋(结构如图所示)是制备抗心律失常药物氟卡尼的中间体。下列有关龙胆酸甲醋的说法。正确的是
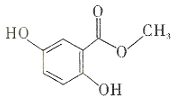
A.分子式为C8H6O4
B.所有的碳原子可能在同一平面内
C.能发生消去反应
D.能通过加聚反应生成高分子化合物
难度: 中等查看答案及解析
-
下列有关物质的组成、性质、用途的说法。正确的是
①Na2O2中的阳离子和阴离子个数比为1:1
②常温下铝制容器可储运浓硫酸或浓硝酸
③盐酸既有氧化性又有还原性
④NO2,Fe(OH)3,FeC12都能直接通过化合反应制备
⑤H2S能使酸性高锰酸钾溶液褪色。所以它具有漂白性
A.②③④ B.①②③ C.①②③④ D. ①②③⑤
难度: 中等查看答案及解析
-
化学平衡常数(K)、电离常数(Ka,Kb)、溶度积常数(Ksp)等常数是表示判断物质性质的重要常数。下列关于这些常数的说法。不正确的是
A.化学平衡常数的大小只与温度有关,与浓度、压强、催化剂无关
B.相同温度时,Ka (HCN) < Ka (CH3COOH),说明物质的量浓度相同时,氢氰酸的酸性比醋酸弱
C.向氯化钡溶液中加入同浓度的碳酸钠和硫酸钠溶液,先产生BaSO4沉淀,则Ksp ( BaSO4) > Ksp(BaCO3)
D.当温度升高时,Ka (CH3COOH)变大
难度: 中等查看答案及解析
-
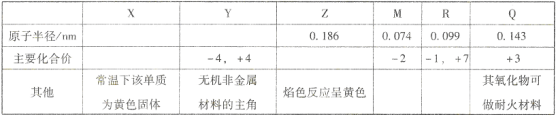
如图为元素周期表的一部分,下列有关短周期元素X,Y,Z,R的叙述正确的是
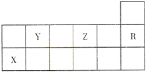
A.热稳定性:Y的气态氢化物>Z的气态氢化物
B.Z的最高价氧化物对应水化物的分子式为H2ZO4
C.X元素的单质能与所有强酸发生反应放出H2
D.R的核外电子数与OH-的核外电子数相同
难度: 中等查看答案及解析