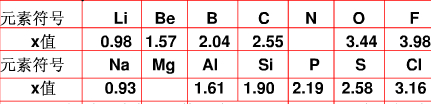
-
某元素原子R的阴离子Rn-核外有X个电子,其核内的中子数为m,则R的质量数是( )
A.x-11
B.m+x+n
C.m+x-n
D.x+n难度: 中等查看答案及解析
-
已知短周期元素的离子.aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
A.原子半径A>B>D>C
B.a-c=1
C.离子半径C>D>B>A
D.单质的还原性A>B>D>C难度: 中等查看答案及解析
-
NA表示阿伏伽德罗常数,下列判断正确的是( )
A.在18g18O2中含有NA个氧原子
B.标准状况下,22.4L空气含有NA个单质分子
C.1molCl2参加反应转移电子数一定为2NA
D.含NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为1mol•L-1难度: 中等查看答案及解析
-
材料与化学密切相关,表中对应关系错误的是( )
材料 主要化学成分 A 刚玉、金刚石 三氧化二铝 B 大理石、石灰石 碳酸钙 C 普通水泥、普通玻璃 硅酸盐 D 沙子、石英 二氧化硅
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
下列表示物质结构的化学用语或模型正确的是( )
A.8个中子的碳原子的核素符号:12C
B.HF的电子式:
C.Cl-离子的结构示意图:
D.CH4分子的比例模型:难度: 中等查看答案及解析
-
下列化合物中所有化学键都是共价键的是( )
A.Na2O2
B.NaOH
C.H2S04
D.BaCl2难度: 中等查看答案及解析
-
为了说明影响化学反应快慢的因素,甲、乙、丙、丁4位同学分别没计了如下4个试验,你认为结论不正确的是( )
A.将形状、大小均相同的镁条和铝条与相同浓度的盐酸反应时,两者速率一样大
B.在相同条件下,等质量的大理石块和大理石粉末与相同浓度的盐酸反应,大理石粉末反应快
C.将浓硝酸分别放在冷暗处和强光照射下,会发现光照可以加快浓硝酸的分解
D.两只试管中分别加入相同质量的氯酸钾,其中一只试管中再加入少量二氧化锰,同时加热,产生氧气的快慢不同难度: 中等查看答案及解析
-
实验是研究化学的基础,下图中所示的实验方法、装置或操作完全正确的是( )
A.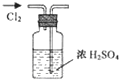
干燥Cl2
B.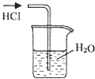
吸收HCl
C.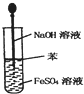
制取Fe(OH)2沉淀
D.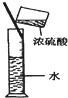
稀释浓H2S04难度: 中等查看答案及解析
-
在用Zn片、Cu片和稀硫酸组成的原电池装置中,工作一段时间后,下列说法正确的是( )
A.锌片是正极,铜片上有气泡产生
B.电流方向是从锌片流向铜片
C.将铜片换成石墨,现象不变
D.电解质溶液的pH保持不变难度: 中等查看答案及解析
-
可逆反应2NO2⇌2NO+O2在体积固定的密闭容器中达到平衡状态的标志是( )
①单位时间内生成n mol O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时生成2n mol NO
③混合气体的颜色不再改变的状态
④混合气体的密度不再改变的状态
⑤混合气体的压强不再改变的状态.
A.①③⑤
B.②⑤
C.①③④⑤
D.全部难度: 中等查看答案及解析
-
下列说法正确的是( )
A.苯分子是一个由6个碳原子以单双键交替结合而成的六元环
B.从形式上看,酯化反应也属于取代反应
C.油脂的相对分子质量都较大,所以属于高分子化含物
D.乙烯能使酸性高锰酸钾溶液和溴水褪色,二者反成原理相同难度: 中等查看答案及解析
-
下列各组离子在溶液中能大量共存,且能与铝反应放出H2的是( )
A.Na+、H+、Ba2+、NO3-
B.K+、Mg2+、Cl-、0H-
C.H+、Mg2+、HCO3-、SO42-
D.Ba2+、Cl-、NO3-、0H-难度: 中等查看答案及解析
-
有下列物质:①NaOH固体:②浓硫酸;③NH4N03晶体;④CaO固体.现将它们分别装入有水的锥形瓶里,立即塞紧带U形管的塞子,发现U形管内滴有红墨水的水血.呈形如图所示状态,判断加入的物质可能是( )

A.①②③④
B.①②④
C.②③④
D.①②③难度: 中等查看答案及解析
-
同周期的X、Y、Z三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序是:HZ04>H2Y04>H3X04,下列判断正确的是
①阴离子的还原性按X、Y、Z顺序减弱 ②单质的氧化性按X、Y、Z顺序增强③非金属性按X、Y、Z顺序增强 ④气态氢化物的稳定性按X、Y、Z顺序减弱( )
A.①②④
B.②③
C.①②③
D.①②③④难度: 中等查看答案及解析
-
下列方程式正确的是( )
A.将铁片投入稀盐酸中:2Fe+6H+=2Fe3++3H2↑
B.将醋酸滴入纯碱溶液:2H++CO32-=H2O+CO2↑
C.甲烷和氯气混合光照:CH4+2Cl2=CCl4+2H2
D.聚氯乙烯塑料的制备:nCH2=CHCl
难度: 中等查看答案及解析
-
酯类物质广泛存在于香蕉、梨等水果中.某实验小组先从梨中分离出一种酯,然后将分离出的酯水解,得到了乙酸和另一种化学式为C6H13OH的物质.对于此过程,以下分析不正确的是( )
A.实验小组分离出的酯可表示为CH3COOC6H13
B.不需要催化剂,这种酯在水中加热即可大量水解
C.C6H13OH分子中含有羟基
D.C6H13OH可以和金属钠反应难度: 中等查看答案及解析